名校
1 . Cr2O 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是
 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是| A.氧化剂和还原剂的计量数之比为3:1 | B.Cr3+是氧化反应的产物 |
C. 发生还原反应 发生还原反应 | D.消耗5 molH+时转移6mol电子 |
您最近一年使用:0次
解题方法
2 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是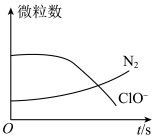
| A.该反应中Cl-为氧化产物 | B.消耗1mol还原剂微粒,转移6mol电子 |
C. 被ClO-氧化成N2 被ClO-氧化成N2 | D.该反应为非氧化还原反应 |
您最近一年使用:0次
解题方法
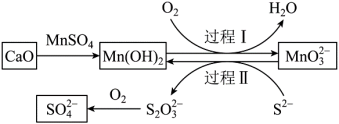
3 . 如图,是工业生产中除去电石渣浆(含CaO)中的 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
A.碱性条件下,氧化性: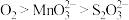 |
| B.过程Ⅰ中氧化剂和还原剂物质的量之比为1∶2 |
C.过程Ⅰ中,反应的离子方程式为 |
D.将1mol  转化为 转化为 理论上需要 理论上需要 的体积为22.4L(标准状况) 的体积为22.4L(标准状况) |
您最近一年使用:0次
解题方法
4 . 下列方程式错误的是
A.在弱碱性条件下,FeS与 反应: 反应: |
B.将少量浓氨水滴入盛有CaO的烧瓶制备 : : |
C.小苏打与明矾共溶于水,产生大量气泡: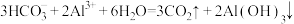 |
D.铅酸蓄电池正极反应: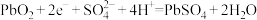 |
您最近一年使用:0次
解题方法
5 . 下列离子方程式与实验对应正确的是
| 选项 | 实验 | 离子方程式 |
| A | 向Na2S2O3溶液中加入稀硝酸 | S2 +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
| B | 用K3[Fe(CN)6]溶液检测FeCl2溶液中的Fe2+ | 2[Fe(CN)6]3-+3Fe2+=Fe3[Fe(CN)6]2↓ |
| C | 向NH4Al(SO4)2溶液中滴加过量NaOH溶液 | N +Al3++4OH-=NH3·H2O+Al(OH)3↓ +Al3++4OH-=NH3·H2O+Al(OH)3↓ |
| D | 向K2MnO4溶液(墨绿色)中加入适量醋酸 溶液变为紫色且有黑色沉淀生成 | 3Mn +4H+=2Mn +4H+=2Mn +MnO2↓+2H2O +MnO2↓+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 肼(联氨)是一种常用的还原剂,下列说法不正确的是
A.碱性: |
B.键角( ): ): |
C. 和 和 均可用于处理高压锅炉水中的氧,防止锅炉被腐蚀,使用联氨的优点是 均可用于处理高压锅炉水中的氧,防止锅炉被腐蚀,使用联氨的优点是 的用量少,且不产生其他杂质 的用量少,且不产生其他杂质 |
D.向装有少量AgBr的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为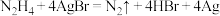 |
您最近一年使用:0次
名校
解题方法
7 . 某反应体系中有七种物质: 和
和 ,在反应过程中,氧化剂、还原剂的物质的量与时间关系如图所示:
,在反应过程中,氧化剂、还原剂的物质的量与时间关系如图所示:

下列叙述正确的是
 和
和 ,在反应过程中,氧化剂、还原剂的物质的量与时间关系如图所示:
,在反应过程中,氧化剂、还原剂的物质的量与时间关系如图所示:
下列叙述正确的是
A.氧化剂 是 是 | B.氧化产物、还原产物的物质的量之比为 |
C.每生成 ,转移 ,转移 电子 电子 | D.随着反应的进行,溶液变为紫红色 |
您最近一年使用:0次
名校
8 . 将标准状况下的22.4LSO2通入含3molNaOH的溶液中,下列用来解释事实的方程式中不合理的是(已知室温下饱和Na2SO3溶液的pH约为8.3)
A.上述反应后所得溶液的pH约为12,原因是 +H2O +H2O  +OH- +OH- |
B.标准状况下的22.4LSO2通入含3molNaOH的溶液,涉及反应:2OH-+SO2= +H2O +H2O |
C.向上述反应后所得溶液中,通入氯气,pH下降:SO3+Cl2+2OH-= +2Cl-+H2O +2Cl-+H2O |
D.向上述反应后所得溶液中,滴加少量H2O2和BaCl2溶液的混合液,产生白色沉淀: +Ba2++H2O2=BaSO4↓+H2O +Ba2++H2O2=BaSO4↓+H2O |
您最近一年使用:0次
名校
解题方法
9 . 硒( )常用作油漆、搪瓷、玻璃和墨水中的颜色、塑料,在电子工业中可用作光电管、太阳能电池等。工业上从含硒阳极泥(硒主要以
)常用作油漆、搪瓷、玻璃和墨水中的颜色、塑料,在电子工业中可用作光电管、太阳能电池等。工业上从含硒阳极泥(硒主要以 和
和 形式存在)中提取硒的流程如下:
形式存在)中提取硒的流程如下:

下列说法错误的是
 )常用作油漆、搪瓷、玻璃和墨水中的颜色、塑料,在电子工业中可用作光电管、太阳能电池等。工业上从含硒阳极泥(硒主要以
)常用作油漆、搪瓷、玻璃和墨水中的颜色、塑料,在电子工业中可用作光电管、太阳能电池等。工业上从含硒阳极泥(硒主要以 和
和 形式存在)中提取硒的流程如下:
形式存在)中提取硒的流程如下:
下列说法错误的是
| A.该生产过程中生成的物质A可用于除铁锈 |
B.“培烧”时, 反应的化学方程式为 反应的化学方程式为 |
C.“焙烧”过程中,反应每转移 电子,生成标准状况下 电子,生成标准状况下 可能小于 可能小于 |
D.“还原”时,氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式能正确表示该化学反应过程的是
A.将硫化钠溶液和亚硫酸溶液混合: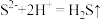 |
B.硫酸亚铁酸性溶液在空气中变黄色: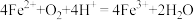 |
C.实验室用稀硝酸溶解银镜: |
D.浓度相同的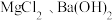 、盐酸三种溶液等体积混合: 、盐酸三种溶液等体积混合: |
您最近一年使用:0次



