名校
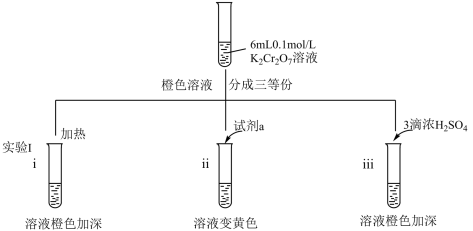
1 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法错误的是
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。 ②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。 
A.i 可证明反应 Cr2O +H2O +H2O 2CrO 2CrO +2H+的正反应放热 +2H+的正反应放热 |
| B.ii 是验证“只降低生成物的浓度,该平衡正向移动”,试剂 a 可以是 NaOH |
| C.iii 平衡逆向移动仅仅是因为增大了生成物的浓度 |
| D.向 iii 所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
您最近一年使用:0次
2023-08-26更新
|
402次组卷
|
4卷引用:湖北省新高考联盟2023-2024学年高二上学期8月开学联考化学试题
2 . 某小组同学探究溶液中的 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:
①在干燥试管中加入绿豆大小的金属钠,逐滴滴加 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。
②向 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。
③向 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。
下列说法不正确 的是
 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:①在干燥试管中加入绿豆大小的金属钠,逐滴滴加
 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。②向
 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。③向
 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。下列说法
| A.实验①中还可能观察到钠块浮在溶液表面,剧烈燃烧,发出黄色火焰 |
| B.实验②中的现象说明实验①中溶液变色的原因与产生的气体无关 |
C.实验③中的现象说明实验①中可能发生的反应: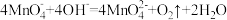 |
D.上述实验能证明溶液中的 可以被金属钠还原 可以被金属钠还原 |
您最近一年使用:0次
2023-05-07更新
|
1675次组卷
|
7卷引用:湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题(已下线)T12-化学反应及限度(已下线)第4讲 钠及其重要化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题(已下线)选择题11-14(已下线)选择题6-10
名校
3 . 硅是大数据时代的关键材料。工业上常在1800—2000℃时,用碳单质还原的方法制取单质硅。涉及反应的相关数据如表所示。下列相关说法正确的是
| 反应 | △H/(kJ•mol-1) | △S/(J•K-1•mol-1) |
| 反应(1):SiO2(s)+2C(s)=Si(s)+2CO(g) | 687.27 | 359.04 |
| 反应(2):SiO2(s)+C(s)=Si(s)+CO2(g) | 514.85 | 183.35 |
| A.反应(1)可证明Si的还原性大于C |
| B.生活中利用单晶硅良好的导光性能做光导纤维 |
| C.工业生产条件下反应(2)无法自发进行发生 |
| D.C(s)+CO2(g)=2CO(g) △H=-172.42kJ·mol-1 |
您最近一年使用:0次
2022-01-08更新
|
1342次组卷
|
6卷引用:河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题
河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题河南省郑州市2022届高三上学期第一次质量预测(1月)化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)
4 . 某同学为验证Fe3+的氧化性进行了如下实验:
已知相同条件下AgCl的溶解度小于Ag2SO4.下列说法不正确的是
| 序号 | 操作 | 现象 |
| 实验I | 将2 mL 2 mol∙L−1Fe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验II | 将2 mL1 mol∙L−1 Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验III | 将2mL2 mol∙L−1FeCl3溶液加入有银镜的试管中 | 银镜消失 |
| 实验IV | 将2mL 1 mol∙L−1 AgNO3溶液加入到1 mL 1 mol∙L−1 FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| A.实验I不能说明Fe3+氧化了Ag |
B.实验II和III说明溶液中存在平衡: Fe3++Ag Fe2++ Ag+ Fe2++ Ag+ |
| C.实验IV中产生白色沉淀,说明Ag+氧化了Fe2+ |
| D.欲证明实验IV中产生了Fe3+,可以取上层清液滴加KSCN溶液 |
您最近一年使用:0次
5 . 某研究性学习小组探究FeSO4的化学性质和用途。回答下列问题:
(1)探究FeSO4溶液的酸碱性:取少量FeSO4固体,利用石蕊溶液测定FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和_______(填字母)。
(2)利用如图装置探究FeSO4的稳定性。
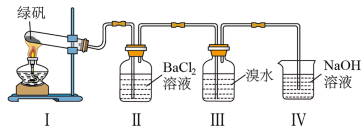
①Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是_______ (填字母)。
A.Fe2O3、SO3、H2O
B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
②Ⅲ中溴水是用来检验是否有SO2气体生成,若有SO2生成,溴水将褪色。实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是_______ 。
③NaOH的作用是吸收SO2气体,请写出用少量NaOH溶液吸收SO2气体的化学方程式:_______ 。
(3)探究FeSO4中Fe2+的还原性:证明FeSO4有较强的还原性,完成下表。
(4)硫酸亚铁用途探究:缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外层包有一层特殊的糖衣,其作用是_______ 。
(1)探究FeSO4溶液的酸碱性:取少量FeSO4固体,利用石蕊溶液测定FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和_______(填字母)。
| A.玻璃棒 | B.试管 | C.天平 | D.量筒 |
(2)利用如图装置探究FeSO4的稳定性。

①Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是
A.Fe2O3、SO3、H2O
B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
②Ⅲ中溴水是用来检验是否有SO2气体生成,若有SO2生成,溴水将褪色。实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是
③NaOH的作用是吸收SO2气体,请写出用少量NaOH溶液吸收SO2气体的化学方程式:
(3)探究FeSO4中Fe2+的还原性:证明FeSO4有较强的还原性,完成下表。
| 实验步骤 | 实验预期现象及结论 |
| 步骤一:取少量的FeSO4固体于试管中,加入一定量水溶解 | |
| 步骤二:滴加 | 当溶液中出现 |
(4)硫酸亚铁用途探究:缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外层包有一层特殊的糖衣,其作用是
您最近一年使用:0次
名校
解题方法
6 . 资料显示, 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。
实验:将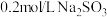 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:
(1)用化学用语解释 溶液呈碱性的原因
溶液呈碱性的原因___________ 。
(2)经检验,I中白色沉淀是 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是___________ 。
(3)重新设计实验(III),证实了: 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
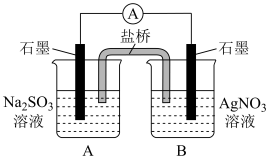
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,___________ (填操作和现象),证明白色固体中含有Ag。
(4)经检验,II中的棕黄色沉淀不含 ,含有
,含有 、
、 和
和 。
。
资料: ,
, 。
。
①用稀 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有___________ 。
②通过下列实验证实,沉淀中含有 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
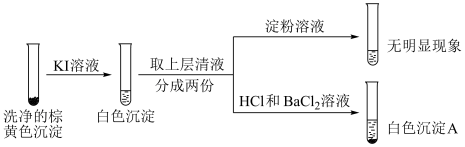
i.白色沉淀A是 。
。
ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将 氧化的微粒是
氧化的微粒是___________ 。
原因二:KI被氧化,由于___________ (用离子方程式表示),所以无明显现象。
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因___________ 。
小结:I中: 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。实验:将
 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:| 序号 | 装置 | 物质a | 现象 |
| I |  2 mL 物质a | 饱和 溶液 溶液 | 产生白色沉淀 |
| II | 0.2 mol/L  溶液 溶液 | 溶液变绿,继续滴加产生棕黄色沉淀 |
(1)用化学用语解释
 溶液呈碱性的原因
溶液呈碱性的原因(2)经检验,I中白色沉淀是
 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是(3)重新设计实验(III),证实了:
 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,
(4)经检验,II中的棕黄色沉淀不含
 ,含有
,含有 、
、 和
和 。
。资料:
 ,
, 。
。①用稀
 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有②通过下列实验证实,沉淀中含有
 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
i.白色沉淀A是
 。
。ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将
 氧化的微粒是
氧化的微粒是原因二:KI被氧化,由于
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了
 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因小结:I中:
 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
您最近一年使用:0次
7 . 下列由实验现象所得结论错误的是
A.向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性 具有氧化性 |
| B.向酸性KMnO4溶液中加入Fe3O4粉末,紫色褪去,证明Fe3O4中含Fe(Ⅱ) |
| C.向5mL 0.2mol/L的FeCl3溶液中加入几滴同浓度的KI溶液,再加入几滴KSCN溶液,溶液显血红色,则FeCl3与KI的反应是可逆反应 |
| D.向碘水中加入等体积CCl4,振荡后静置,上层接近无色, 下层显紫红色,说明I2在CCl4中的溶解度大于在水中的溶解度 |
您最近一年使用:0次
解题方法
8 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行实验。
已知: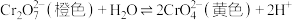
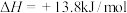 ,+6价格盐在一定条件下可被还原为
,+6价格盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。
实验一:

(1)试管c和b对比,推测试管c的现象是_______ 。
(2)试管a和b对比,a中溶液橙色加深,甲认为温度也会影响平衡的移动,橙色加深不一定是 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?_______ (“是”或“否”),理由是_______ 。
(3)对比试管a、b、c的实验现象,可以得到的结论是_______ 。
实验二:取试管c完成如下实验。
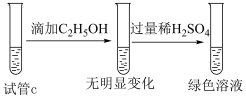
(4)试管c中溶液变为绿色时,发生的氧化还原反应的离子方程式是_______ (乙醇转化为乙酸)。
(5)由实验二中实验现象,可以得出的结论是_______ 。
(6)丙同学欲通过+6价铬盐与KI反应,验证(5)中结论,他的实验方案是_______ 。
已知:
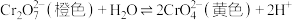
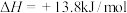 ,+6价格盐在一定条件下可被还原为
,+6价格盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。实验一:

(1)试管c和b对比,推测试管c的现象是
(2)试管a和b对比,a中溶液橙色加深,甲认为温度也会影响平衡的移动,橙色加深不一定是
 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?(3)对比试管a、b、c的实验现象,可以得到的结论是
实验二:取试管c完成如下实验。

(4)试管c中溶液变为绿色时,发生的氧化还原反应的离子方程式是
(5)由实验二中实验现象,可以得出的结论是
(6)丙同学欲通过+6价铬盐与KI反应,验证(5)中结论,他的实验方案是
您最近一年使用:0次
名校
解题方法
9 . 某小组在验证反应“ ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。
向硝酸酸化的 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
(1)检测到滤液中含有 ,可以选用的试剂为
,可以选用的试剂为___________ (填化学式)溶液。 产生的原因可能有以下几种。
产生的原因可能有以下几种。
假设a:可能是铁粉表面有氧化层,能产生 。
。
假设b:空气中存在 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
假设c:酸性溶液中的 具有氧化性,可产生
具有氧化性,可产生 。
。
(2)某同学证明上面假设c不成立,向硝酸酸化的___________ 硝酸钠溶液中加入过量铁粉,搅拌后静置,一段时间后,上层清液未变黄色,经检验无 。
。
(3)取过滤后的黑色固体,洗涤后,___________ (填操作和现象),证明黑色固体中含有Ag。
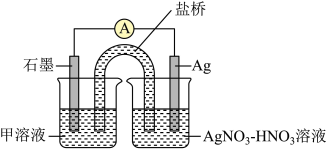
(4)某同学利用原电池证明 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为___________ 。写出石墨电极上发生的电极反应式:___________ 。电流表指针不再偏转后,向左侧烧杯中加入 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为___________ (填“正极”或“负极”),银电极的电极反应式为___________ 。
 ”,实验探究过程如下。结合探究过程回答下列问题。
”,实验探究过程如下。结合探究过程回答下列问题。向硝酸酸化的
 硝酸银溶液中(忽略
硝酸银溶液中(忽略 的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。
的水解)加入过量铁粉,搅拌后静置,一段时间后,将烧杯底部黑色固体过滤,滤液呈黄色。(1)检测到滤液中含有
 ,可以选用的试剂为
,可以选用的试剂为 产生的原因可能有以下几种。
产生的原因可能有以下几种。假设a:可能是铁粉表面有氧化层,能产生
 。
。假设b:空气中存在
 ,
, 被氧化为
被氧化为 ,写出反应的离子方程式:
,写出反应的离子方程式:假设c:酸性溶液中的
 具有氧化性,可产生
具有氧化性,可产生 。
。(2)某同学证明上面假设c不成立,向硝酸酸化的
 。
。(3)取过滤后的黑色固体,洗涤后,
(4)某同学利用原电池证明
 可以将
可以将 氧化为
氧化为 ,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除
,设计了如图所示的原电池装置。连接装置后,电流表中有电流通过,一段时间后电流表不再偏转(所用溶液均已去除 )。甲溶液中的溶质为
)。甲溶液中的溶质为 固体,发现电流表指针反向偏转,此时石墨电极为
固体,发现电流表指针反向偏转,此时石墨电极为
您最近一年使用:0次
2023-10-26更新
|
611次组卷
|
7卷引用:湖南省娄底市新化县2023-2024学年高二上学期期末考试化学试题
10 . 为验证化学反应“2Fe3++2I-=2Fe2++I2”是可逆反应,并探究平衡移动与物质的浓度、性质的关系,甲、乙两同学进行如下实验。
已知:a.含I2的溶液呈黄色或棕黄色。
b.利用色度计可测定溶液的透光率,通常溶液颜色越深,透光率数值越小。
I.甲同学设计下列实验进行相关探究,实验如图1所示。
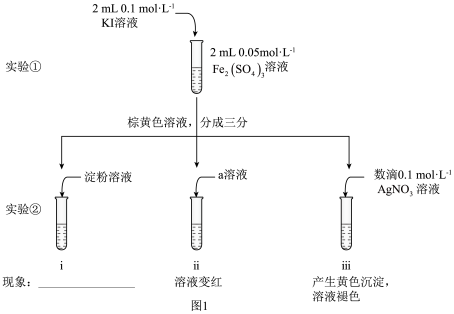
回答下列问题:
(1)甲同学利用实验②中ⅰ和ⅱ证明Fe2(SO4)3溶液与KI溶液的反应为可逆反应,实验ⅰ中的现象是_____ ,实验ⅱ中a是_____ (填化学式)溶液。
(2)用离子方程式表示实验②ⅲ中产生黄色沉淀的原因_____ 。
II.乙同学:利用色度计对Fe2(SO4)3溶液与KI溶液的反应进行再次探究。
【实验过程】
实验中溶液的透光率数据变化如图2所示。

回答下列问题:
(3)乙同学实验③的目的是_____ 。
(4)乙同学通过透光率变化推断:FeCl3溶液与KI溶液的反应为可逆反应.理由是_____ 。
(5)乙同学根据氧化还原反应的规律,用图3装置(a、b均为石墨电极),探究化学平衡移动与I-、Fe2+的浓度及还原性强弱关系,操作过程如图:
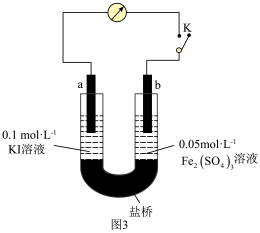
①K闭合时,电流计指针向右偏转,乙同学得出结论:2Fe3++2I- 2Fe2++I2向正反应方向进行,b作
2Fe2++I2向正反应方向进行,b作______ (填“正”或“负”)极,还原性I->Fe2+。
②当指针归零(反应达到平衡)后,向U型管右管滴加0.1mol•L-1FeSO4溶液,电流计指针向左偏转,由此得出还原性为Fe2+______ I-(填“>”或“<”)。
(6)综合甲、乙两位同学的实验探究过程,可得出结论:2Fe3++2I-=2Fe2++I2为可逆反应,改变条件可使平衡移动;Fe3+和I2的氧化性强弱受______ 影响。
已知:a.含I2的溶液呈黄色或棕黄色。
b.利用色度计可测定溶液的透光率,通常溶液颜色越深,透光率数值越小。
I.甲同学设计下列实验进行相关探究,实验如图1所示。

回答下列问题:
(1)甲同学利用实验②中ⅰ和ⅱ证明Fe2(SO4)3溶液与KI溶液的反应为可逆反应,实验ⅰ中的现象是
(2)用离子方程式表示实验②ⅲ中产生黄色沉淀的原因
II.乙同学:利用色度计对Fe2(SO4)3溶液与KI溶液的反应进行再次探究。
【实验过程】
| 序号 | 实验步骤1 | 实验步骤2 |
| 实验③ | 将盛有2mL蒸馏水的比色皿放入色度计的槽孔中 | 向比色皿中逐滴滴入5滴(每滴约0.025mL)0.05mol•L-1Fe2(SO4)3溶液,同时采集溶液的透光率数据 |
| 实验④ | 将盛有2mL0.1mol•L-1KI溶液的比色皿放入色度计的槽孔中 | 同上 |
| 实验⑤ | 将盛有2mL0.2mol•L-1KI溶液的比色皿放入色度计的槽孔中 | 同上 |

回答下列问题:
(3)乙同学实验③的目的是
(4)乙同学通过透光率变化推断:FeCl3溶液与KI溶液的反应为可逆反应.理由是
(5)乙同学根据氧化还原反应的规律,用图3装置(a、b均为石墨电极),探究化学平衡移动与I-、Fe2+的浓度及还原性强弱关系,操作过程如图:

①K闭合时,电流计指针向右偏转,乙同学得出结论:2Fe3++2I-
 2Fe2++I2向正反应方向进行,b作
2Fe2++I2向正反应方向进行,b作②当指针归零(反应达到平衡)后,向U型管右管滴加0.1mol•L-1FeSO4溶液,电流计指针向左偏转,由此得出还原性为Fe2+
(6)综合甲、乙两位同学的实验探究过程,可得出结论:2Fe3++2I-=2Fe2++I2为可逆反应,改变条件可使平衡移动;Fe3+和I2的氧化性强弱受
您最近一年使用:0次



