名校
1 . 某家用防疫品“84消毒液”的包装说明如下,回答下列问题:
(1)“84”消毒液可由 与
与 溶液反应制得,该反应的离子方程式为
溶液反应制得,该反应的离子方程式为___________ 。
(2)欲将“84消毒液”原液稀释配制成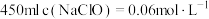 的溶液。
的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、______ 。
②配制时,需要取用______ mL“84消毒液”原液。
③下列操作会使溶液中 浓度偏高的是
浓度偏高的是______ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
E.转移时没有洗涤烧杯和玻璃棒
(3)用次氯酸钠固体配置一定物质的量浓度溶液的消毒液,下列操作正确的是______ 。
A. B.
B. C.
C.
(4)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到 试纸的现象是
试纸的现象是______ 。棉花团(蘸有溶液A)的作用是___________ 。

(5)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式___________ 。
| 【产品名称】84消毒液 【有效成分】  【规格】  【物质的量浓度】  注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用 |
(1)“84”消毒液可由
 与
与 溶液反应制得,该反应的离子方程式为
溶液反应制得,该反应的离子方程式为(2)欲将“84消毒液”原液稀释配制成
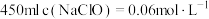 的溶液。
的溶液。①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②配制时,需要取用
③下列操作会使溶液中
 浓度偏高的是
浓度偏高的是A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
E.转移时没有洗涤烧杯和玻璃棒
(3)用次氯酸钠固体配置一定物质的量浓度溶液的消毒液,下列操作正确的是
A.
 B.
B. C.
C.
(4)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到
 试纸的现象是
试纸的现象是
(5)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
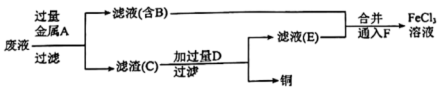
(1)滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
(2)滤渣C与试剂D反应的离子方程式为_______ ,为测定滤渣中铜的质量分数,取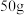 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到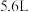 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数______ 。
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
请回答:
(3)实验I中反应的化学方程式是___________ 。
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(5)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)滤渣C中所含物质的化学式为
(2)滤渣C与试剂D反应的离子方程式为
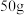 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到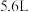 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
| 实验I | 实验Ⅱ |
 | 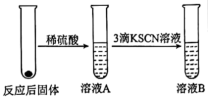 |
(3)实验I中反应的化学方程式是
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是
(5)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
名校
3 . 下列关于物质之间的转化不可以通过化合反应一步实现的是
| A.Na→Na2O2 | B.Na2O→Na2CO3 | C.Cl2→HCl | D.Cl2→HClO |
您最近一年使用:0次
2023-12-23更新
|
47次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一上学期1月月考化学试题
名校
4 . 某小组同学探究不同条件下氯气与二价锰化合物的反应,实验记录如下:
资料:水溶液中, 为棕黑色沉淀,
为棕黑色沉淀, 为白色沉淀,
为白色沉淀, 呈绿色;浓碱性条件下,
呈绿色;浓碱性条件下, 可被
可被 还原为
还原为 ;
; 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
下列说法错误的是
| 序号 | 实验方案 | 实验现象 | |
| 实验装置 | 试剂a | ||
| ① | 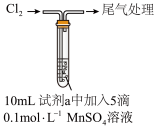 | 水 | 产生黑色沉淀,放置后不发生变化 |
| ② | 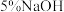 溶液 溶液 | 产生黑色沉淀,放置后溶液变为紫色,仍有沉淀 | |
| ③ | 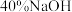 溶液 溶液 | 产生黑色沉淀,放置后溶液变为紫色,仍有沉淀 | |
| ④ | 取③中放置后的悬浊液 ,加入 ,加入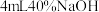 溶液 溶液 | 溶液紫色迅速变为绿色,且绿色缓慢加深 | |
| ⑤ | 取③中放置后的悬浊液 ,加入 ,加入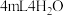 | 溶液紫色缓慢加深 | |
 为棕黑色沉淀,
为棕黑色沉淀, 为白色沉淀,
为白色沉淀, 呈绿色;浓碱性条件下,
呈绿色;浓碱性条件下, 可被
可被 还原为
还原为 ;
; 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。下列说法错误的是
| A.对比实验①和②可知,碱性环境中,二价锰化合物可被氧化到更高价态 |
B.④中溶液紫色迅速变为绿色的可能原因是: 被 被 还原生成 还原生成 |
C.⑤中紫色缓慢加深的主要原因是: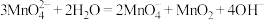 |
D.③中未得到绿色溶液,可能是因为 被氧化为 被氧化为 的反应速率快于 的反应速率快于 被还原为 被还原为 的反应速率 的反应速率 |
您最近一年使用:0次
2023-12-12更新
|
276次组卷
|
2卷引用: 湖南师范大学附属中学2023-2024学年高三下学期第六次月考化学试题
名校
解题方法
5 . 现有以下物质:① 溶液;②液态
溶液;②液态 ;③
;③ 晶体;④熔融
晶体;④熔融 ;⑤Na;⑥氯气;⑦淀粉胶体。
;⑤Na;⑥氯气;⑦淀粉胶体。
(1)以上物质中属于电解质的是________ (填序号)。
(2)将淀粉溶于水,要判定得到的分散系是胶体还是溶液。判定的方法名称是________ 。
(3)写出③ 晶体在生活中的一种应用
晶体在生活中的一种应用________________ 。
(4)写出③在水溶液中的电离方程式:________________ 。
(5)⑤Na的其中一种氧化物可用作呼吸面具和潜艇的供氧剂,写出其与水反应的化学方程式________________ 。
(6)用⑥氯气和石灰乳可以制取漂白粉,漂白粉在空气中生成 的化学方程式为
的化学方程式为________________ 。
 溶液;②液态
溶液;②液态 ;③
;③ 晶体;④熔融
晶体;④熔融 ;⑤Na;⑥氯气;⑦淀粉胶体。
;⑤Na;⑥氯气;⑦淀粉胶体。(1)以上物质中属于电解质的是
(2)将淀粉溶于水,要判定得到的分散系是胶体还是溶液。判定的方法名称是
(3)写出③
 晶体在生活中的一种应用
晶体在生活中的一种应用(4)写出③在水溶液中的电离方程式:
(5)⑤Na的其中一种氧化物可用作呼吸面具和潜艇的供氧剂,写出其与水反应的化学方程式
(6)用⑥氯气和石灰乳可以制取漂白粉,漂白粉在空气中生成
 的化学方程式为
的化学方程式为
您最近一年使用:0次
2023-12-11更新
|
48次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
名校
6 . 如图所示,在A处通入未经干燥的氯气。当关闭B处的弹簧夹时,C处的红布条看不到明显现象;当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是
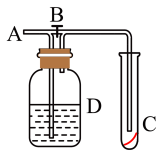
| A.③④ | B.②③ | C.①③ | D.①② |
您最近一年使用:0次
2023-12-07更新
|
105次组卷
|
3卷引用:湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷
7 . 下列关于金属钠与氯气说法不正确的是
| A.金属钠可以保存在煤油中 | B.金属钠熔点低,硬度大 |
| C.氯气、液氯是同一种物质 | D.氯气与石灰乳反应可制漂白粉 |
您最近一年使用:0次
2023-11-23更新
|
330次组卷
|
7卷引用:河南省新乡市原阳县第一高级中学2023-2024学年高一上学期1月月考化学试题
8 . 84消毒液(有效成分为 )和双氧水是常用的家用消毒剂。
)和双氧水是常用的家用消毒剂。
(1)实验室用 和
和 溶液制备84消毒液,其反应的离子方程式为
溶液制备84消毒液,其反应的离子方程式为___________ 。
(2)在研究物质性质时,研究小组向盛有 84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
[猜测1]双氧水与消毒液发生反应产生气体。
[猜测2]……
①请设计实验证明产生的气体为氧气:___________ 。
②猜测2可能为___________ 。
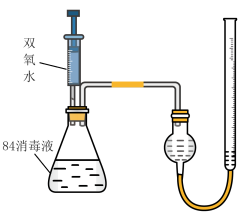
③为了验证猜想,设计用如下装置进行实验,注射器中装有 10%的双氧水,锥形瓶中装有
10%的双氧水,锥形瓶中装有 84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
④
___________ ;通过实验得出猜想1正确,其判断依据为___________ ,二者发生反应的化学方程式为___________ 。
 )和双氧水是常用的家用消毒剂。
)和双氧水是常用的家用消毒剂。(1)实验室用
 和
和 溶液制备84消毒液,其反应的离子方程式为
溶液制备84消毒液,其反应的离子方程式为(2)在研究物质性质时,研究小组向盛有
 84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
84消毒液的试管中逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。[猜测1]双氧水与消毒液发生反应产生气体。
[猜测2]……
①请设计实验证明产生的气体为氧气:
②猜测2可能为
③为了验证猜想,设计用如下装置进行实验,注射器中装有
 10%的双氧水,锥形瓶中装有
10%的双氧水,锥形瓶中装有 84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
84消毒液,分5次注入双氧水,产生气体的体积如下表所示。
| 次数 | 注入双氧水的体积/mL | 产生气体的总体积/mL |
| 第1次 | 4 | 125 |
| 第2次 | 4 | 250 |
| 第3次 | 4 | 325 |
| 第4次 | 4 | V |
| 第5次 | 4 | 333 |

您最近一年使用:0次
2023-10-30更新
|
100次组卷
|
2卷引用:江西省百师联盟2024届高三上学期9月复习联考化学试题
名校
解题方法
9 . 下列操作、现象和结论均正确且有关联性的是
| 选项 | 操作及现象 | 结论 |
| A | 向品红溶液中通入氯气,品红溶液褪色 | 氯气有漂白性 |
| B | 向酸性 溶液中滴加乙醇,溶液褪色 溶液中滴加乙醇,溶液褪色 | 乙醇表现还原性 |
| C | 在酚酞溶液中加入 粉末,溶液先变红后褪色 粉末,溶液先变红后褪色 |  表现碱性 表现碱性 |
| D | 在盛满 的集气瓶中加入烘干的活性炭,气体颜色变浅 的集气瓶中加入烘干的活性炭,气体颜色变浅 | 活性炭表现还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-27更新
|
391次组卷
|
5卷引用:黑龙江省齐齐哈尔市第八中学校2024届高三1月大联考考后强化卷化学试题
10 . 在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解。从废定影液{主要含有[Ag(S2O3)2]3-、Br-等}中回收Ag并制取催化剂PdAg@Cu2O的流程如图所示:
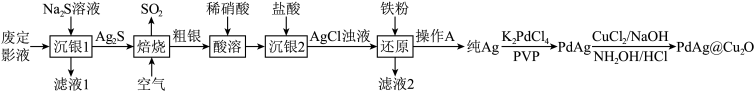
已知:① 的结构如图所示:
的结构如图所示: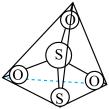 ;
;
②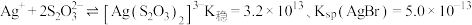 。
。
请回答下列问题:
(1)写出Na2S2O3溶液溶解AgBr生成 的离子方程式:
的离子方程式:___________ ,该反应的化学平衡常数为___________ 。
(2)在 配合反应中,作配位原子的不可能是
配合反应中,作配位原子的不可能是___________ (填字母)。
a. 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子
(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br2。通入足量氯气后,Cl2发生的氧化还原反应主要有 、
、 、
、___________ 。
(4)“酸溶”过程中产生的有害气体是___________ (填化学式),实验室消除该有害气体的方法为___________ 。
(5)操作 的目的是
的目的是___________ 。
(6)在制备PdAg@Cu2O的反应中,NH2OH被氧化成无污染物(N2),若获得0.5molPdAg@Cu2O,理论上至少需要NH2OH___________ g。

已知:①
 的结构如图所示:
的结构如图所示: ;
;②
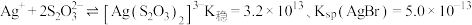 。
。请回答下列问题:
(1)写出Na2S2O3溶液溶解AgBr生成
 的离子方程式:
的离子方程式:(2)在
 配合反应中,作配位原子的不可能是
配合反应中,作配位原子的不可能是a.
 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br2。通入足量氯气后,Cl2发生的氧化还原反应主要有
 、
、 、
、(4)“酸溶”过程中产生的有害气体是
(5)操作
 的目的是
的目的是(6)在制备PdAg@Cu2O的反应中,NH2OH被氧化成无污染物(N2),若获得0.5molPdAg@Cu2O,理论上至少需要NH2OH
您最近一年使用:0次
2023-10-06更新
|
566次组卷
|
3卷引用:安徽省巢湖市第一中学2024届高三10月月考化学试题



