23-24高三上·北京东城·期中
名校
1 . 常温下,向新制氯水中滴加NaOH溶液,溶液中水电离出的 浓度与NaOH溶液体积之间的关系如图所示。下列推断
浓度与NaOH溶液体积之间的关系如图所示。下列推断不正确 的是

 浓度与NaOH溶液体积之间的关系如图所示。下列推断
浓度与NaOH溶液体积之间的关系如图所示。下列推断
| A.E、F点溶液的pH分别为3和7 |
B.F点对应的溶液中: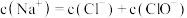 |
C.G点对应的溶液中: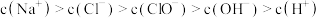 |
D.F~H点对应的溶液中, 为定值 为定值 |
您最近一年使用:0次
2023·北京顺义·二模
名校
2 . 氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。某研究性学习小组模拟热分解CuCl2•2H2O制备CuCl的过程,并进行相关物质转化的探究。
已知:酸性条件下Cu+不稳定

下列说法不正确的是
已知:酸性条件下Cu+不稳定

下列说法不正确的是
| A.X气体是HCl,可抑制CuCl2•2H2O加热时水解 |
| B.途径1中产生的Cl2可以回收利用,也可以通入饱和NaOH溶液中除去 |
C.途径2中200℃时反应的化学方程式为Cu2(OH)2Cl2 2CuO+2HCl↑ 2CuO+2HCl↑ |
D.CuCl与稀硫酸反应的离子方程式为2Cu++4H++SO =2Cu2++SO2↑+2H2O =2Cu2++SO2↑+2H2O |
您最近一年使用:0次
2023-04-12更新
|
1048次组卷
|
7卷引用:专题10 物质的反应及转化
(已下线)专题10 物质的反应及转化北京市顺义区2023届高三下学期第二次化学统练题(已下线)第07练 元素及其化合物基础知识和应用 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题江西省丰城中学2023-2024学年高三上学期开学考试化学试题河南省中原名校联盟2024届高三上学期9月调研考试化学试题陕西省西安市长安区第一中学2023-2024学年高三上学期第三次教学质量检测(期中)化学试题
22-23高三上·山东潍坊·阶段练习
解题方法
3 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
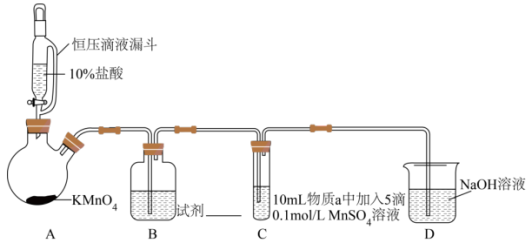
(1)通入 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为_______ 。
(2)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是 被
被_______ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量;
②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因_______ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| II | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| III | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为(2)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
 被
被②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因
您最近一年使用:0次
4 . 根据如图所示的转化关系(反应条件已略去)判断,下列说法正确的是


| A.反应①②③④⑤均属于氧化还原反应和离子反应 |
| B.反应⑤说明该条件下铝的还原性强于锰 |
| C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1 |
| D.反应①中氧化剂与还原剂的物质的量之比为1∶4 |
您最近一年使用:0次
2022-12-21更新
|
708次组卷
|
3卷引用:专题08 元素及其化合物(练)-2023年高考化学二轮复习讲练测(新高考专用)
(已下线)专题08 元素及其化合物(练)-2023年高考化学二轮复习讲练测(新高考专用)湖北省武汉海淀外国语实验学校2022-2023学年高三上学期10月月考化学试题吉林省通化市梅河口市第五中学2022-2023学年高一上学期期末考试化学试题
2022·全国·模拟预测
解题方法
5 . 84消毒液(有效成分为NaClO)和双氧水是常态抗疫常用的家用消毒剂。
(1)实验室用Cl2和NaOH溶液制备84消毒液,其反应离子方程式为____ 。
(2)某研究小组用浓盐酸与MnO2混合加热制备氯气,当发现氯气不再逸出时,固液混合物中仍有盐酸和MnO2。反应结束后仍有盐酸和MnO2的原因是____ 。若将该反应过程用电极反应表示,还原反应为____ 。
(3)在研兖物质性质时,研究小组向盛有2mL84消毒液的试管中,逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生气体。
猜测2:____。
①请设计实验证明产生的气体为氧气:____ 。
②猜测2可能为____ 。
③为了验证猜想,设计用如图装置进行实验,注射器中装有20mL10%的双氧水,锥形瓶中装有25mL84消毒液,分5次注入双氧水,产生气体的体积如表所示。
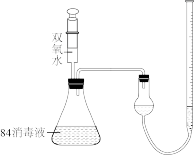
④V=____ ;通过实验得出猜想1正确,其判断依据为____ ;二者发生反应的化学方程式为____ 。
(1)实验室用Cl2和NaOH溶液制备84消毒液,其反应离子方程式为
(2)某研究小组用浓盐酸与MnO2混合加热制备氯气,当发现氯气不再逸出时,固液混合物中仍有盐酸和MnO2。反应结束后仍有盐酸和MnO2的原因是
(3)在研兖物质性质时,研究小组向盛有2mL84消毒液的试管中,逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生气体。
猜测2:____。
①请设计实验证明产生的气体为氧气:
②猜测2可能为
③为了验证猜想,设计用如图装置进行实验,注射器中装有20mL10%的双氧水,锥形瓶中装有25mL84消毒液,分5次注入双氧水,产生气体的体积如表所示。

| 次数 | 注入双氧水的体积/mL | 产生气体的总体积/mL |
| 第1次 | 4 | 125 |
| 第2次 | 4 | 250 |
| 第3次 | 4 | 325 |
| 第4次 | 4 | V |
| 第5次 | 4 | 333 |
您最近一年使用:0次
2022·湖北孝感·模拟预测
名校
解题方法
6 . 二氯异氰尿酸钠(C3N3O3Cl2Na)是一种高效、安全的消毒剂。实验室可用如图所示装置制备二氯异氰尿酸钠(加热和夹持装置均已略去),实验原理为2NaClO+C3H3N3O3 C3N3O3Cl2Na+NaOH+H2O ΔH<0。
C3N3O3Cl2Na+NaOH+H2O ΔH<0。
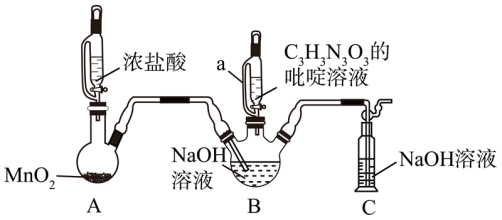
回答下列问题:
(1)装置A中发生反应的离子方程式为_______ 。
(2)当观察到B中液面上方有黄绿色气体时,打开装置a的活塞加入C3H3N3O3的吡啶溶液,此时_______ (填“继续”或“停止”)通入氯气。
(3)实验过程中B容器置于冷水浴的原因除降低其溶解度,便于分离产品外还有_______ 。
(4)装置C中发生反应的化学方程式为_______ 。
(5)上述装置存在一处缺陷,导致B中NaOH溶液的利用率较低,改进的方法是_______ 。
(6)通过下列步骤测定样品中二氯异氰尿酸钠的含量。
I.准确称取ag样品,用容量瓶配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸生成HClO ;
Ⅱ.再加入过量KI溶液,密封在暗处静置5min;
Ⅲ.用0.1000mol·L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗Na2 S2O3溶液V mL。
已知:HClO+2I—+H+=I2+Cl-+H2O; I2+2S2O =S4O
=S4O +2I—。
+2I—。
①步骤I中生成HClO的离子方程式为_______ 。
②步骤Ⅲ中所选的指示剂为_______ 。
③该样品中二氯异氰尿酸钠的质量分数为_______ %(用含a、V的代数式表示)。
 C3N3O3Cl2Na+NaOH+H2O ΔH<0。
C3N3O3Cl2Na+NaOH+H2O ΔH<0。
回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)当观察到B中液面上方有黄绿色气体时,打开装置a的活塞加入C3H3N3O3的吡啶溶液,此时
(3)实验过程中B容器置于冷水浴的原因除降低其溶解度,便于分离产品外还有
(4)装置C中发生反应的化学方程式为
(5)上述装置存在一处缺陷,导致B中NaOH溶液的利用率较低,改进的方法是
(6)通过下列步骤测定样品中二氯异氰尿酸钠的含量。
I.准确称取ag样品,用容量瓶配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸生成HClO ;
Ⅱ.再加入过量KI溶液,密封在暗处静置5min;
Ⅲ.用0.1000mol·L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入指示剂继续滴定至终点,消耗Na2 S2O3溶液V mL。
已知:HClO+2I—+H+=I2+Cl-+H2O; I2+2S2O
 =S4O
=S4O +2I—。
+2I—。①步骤I中生成HClO的离子方程式为
②步骤Ⅲ中所选的指示剂为
③该样品中二氯异氰尿酸钠的质量分数为
您最近一年使用:0次
21-22高一下·上海闵行·开学考试
名校
7 . 现有氢气与氯气的混合气体0.1mol,经充分反应后,通入60mL 2mol/L的NaOH溶液中,所得溶液中只含有2种溶质,其中NaCl为0.1mol。则原混合气体中氢气的物质的量可能是
| A.0.02mol | B.0.04mol | C.0.06mol | D.0.08mol |
您最近一年使用:0次
2022-04-25更新
|
1337次组卷
|
5卷引用:第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)上海市七宝中学2021-2022学年高一下学期开学摸底测试化学试题上海市洋泾中学2022-2023学年高一上学期期中考试化学试题四川省成都市树德中学2022-2023学年高一上学期期末复习化学试题
21-22高三上·河北邢台·阶段练习
解题方法
8 . 将 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是
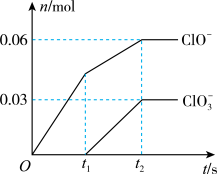
 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应放热),生成物中有三种含氯元素的离子,其中 和
和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是
A. 和苛性钾溶液在不同温度下可能发生不同反应 和苛性钾溶液在不同温度下可能发生不同反应 |
B.原苛性钾溶液中 的物质的量无法确定 的物质的量无法确定 |
C.反应中转移电子数为 |
D.生成物中 的物质的量为 的物质的量为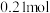 |
您最近一年使用:0次
2021-09-29更新
|
1229次组卷
|
6卷引用:专题02 卤素元素拓展之实验大题-【微专题·大素养】备战2022年高考化学核心突破(元素拓展综合题)
(已下线)专题02 卤素元素拓展之实验大题-【微专题·大素养】备战2022年高考化学核心突破(元素拓展综合题)河北省邢台市2022届高三9月第二次联合考试化学试题山东省济南市商河县第三中学2022届高三10月月考化学试题河南省南阳市2022-2023学年高一上学期1月期末考试化学试题安徽省阜阳市阜南县2022-2023学年高一上学期期末联考化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
2021·湖北·模拟预测
解题方法
9 . 无水 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水 的实验装置如图所示:
的实验装置如图所示:

E和G用来收集产物。回答下列问题:
(1)通入氯气后,A中观察到有酸雾产生,C中 的作用是
的作用是_______ 。
(2)在E、G处收集产物是利用了
_______ 的性质。
(3)实验过程中若F处出现堵塞,则在B处可观察到的现象是_______ 。可通过_______ (填简单操作),使实验能继续进行。
(4)Ⅰ中反应的离子方程式为_______ 。
(5)某同学用 干燥铁粉制得无水
干燥铁粉制得无水 样品
样品 ,该次实验的产率是
,该次实验的产率是_______ 。
(6)实验室中还常用 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为_______ .检验水合三氯化铁原料中是否存在 的试剂是
的试剂是_______ 。
 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水 的实验装置如图所示:
的实验装置如图所示:
E和G用来收集产物。回答下列问题:
(1)通入氯气后,A中观察到有酸雾产生,C中
 的作用是
的作用是(2)在E、G处收集产物是利用了

(3)实验过程中若F处出现堵塞,则在B处可观察到的现象是
(4)Ⅰ中反应的离子方程式为
(5)某同学用
 干燥铁粉制得无水
干燥铁粉制得无水 样品
样品 ,该次实验的产率是
,该次实验的产率是(6)实验室中还常用
 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为 的试剂是
的试剂是
您最近一年使用:0次
2020·河北·一模
解题方法
10 . 硫代硫酸钠晶体(Na2S2O3·5H2O)具有脱敏作用,临床上用于氰化物及腈类中毒,它又名“大苏打”、“海波”,易溶于水,难溶于乙醇,水溶液呈微弱的碱性,遇强酸发生剧烈反应。某化学兴趣小组通过查阅资料,对它的制备和性质进行了探究,研究过程如下:
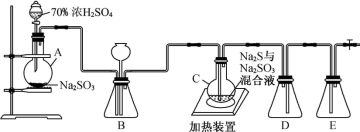
请回答下列问题:
Ⅰ.Na2S2O3的制备:已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)
S(s)+Na2SO3(aq) Na2S2O3(aq)
Na2S2O3(aq)
(1)装置A中发生的化学反应方程式为___________ 。
(2)装置B中盛放浓硫酸,除干燥气体外,还起到的作用有___________ 。
(3)C装置中放入无水乙醇的目的是___________ 。
Ⅱ.测定产品(Na2S2O3·5H2O)的纯度。该小组同学称取m g该产品,用容量瓶配成250 mL溶液。另取c mol·L-1的K2Cr2O7标准溶液V mL,用硫酸酸化后加入过量KI,再加入几滴淀粉溶液,然后用硫代硫酸钠样品溶液滴定至蓝色褪去,且30 s不恢复原色。平行滴定3次所得测定数据如下表:
(4)已知滴定过程中发生的反应: 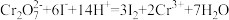 ;
; 。则样品纯度为
。则样品纯度为___________ (写出化简后表达式)。
Ⅲ.探究硫代硫酸钠(Na2S2O3)在化工上作脱氯剂的原理。下面是该兴趣小组利用制得的硫代硫酸钠样品模拟脱氯的实验装置,回答下列问题:

注:Ksp[BaS2O3]=6.96×10-11
(5)若要证明硫代硫酸钠可以作为脱氯剂,还需要补充的实验操作是___________ 。
(6)装置D作用是吸收Cl2,实验后检测到该溶液中含有ClO-、 等离子,则c(H+)-c(OH-)=
等离子,则c(H+)-c(OH-)=___________ ,若D中ClO-与 的物质的量之比为5︰1,则Cl2与NaOH的离子反应方程式为
的物质的量之比为5︰1,则Cl2与NaOH的离子反应方程式为___________ 。

请回答下列问题:
Ⅰ.Na2S2O3的制备:已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)
S(s)+Na2SO3(aq)
 Na2S2O3(aq)
Na2S2O3(aq)(1)装置A中发生的化学反应方程式为
(2)装置B中盛放浓硫酸,除干燥气体外,还起到的作用有
(3)C装置中放入无水乙醇的目的是
Ⅱ.测定产品(Na2S2O3·5H2O)的纯度。该小组同学称取m g该产品,用容量瓶配成250 mL溶液。另取c mol·L-1的K2Cr2O7标准溶液V mL,用硫酸酸化后加入过量KI,再加入几滴淀粉溶液,然后用硫代硫酸钠样品溶液滴定至蓝色褪去,且30 s不恢复原色。平行滴定3次所得测定数据如下表:
| 实验序号 | 1 | 2 | 3 |
| 消耗样品溶液体积/mL | 24.79 | 22.30 | 24.81 |
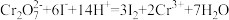 ;
; 。则样品纯度为
。则样品纯度为Ⅲ.探究硫代硫酸钠(Na2S2O3)在化工上作脱氯剂的原理。下面是该兴趣小组利用制得的硫代硫酸钠样品模拟脱氯的实验装置,回答下列问题:

注:Ksp[BaS2O3]=6.96×10-11
(5)若要证明硫代硫酸钠可以作为脱氯剂,还需要补充的实验操作是
(6)装置D作用是吸收Cl2,实验后检测到该溶液中含有ClO-、
 等离子,则c(H+)-c(OH-)=
等离子,则c(H+)-c(OH-)= 的物质的量之比为5︰1,则Cl2与NaOH的离子反应方程式为
的物质的量之比为5︰1,则Cl2与NaOH的离子反应方程式为
您最近一年使用:0次



