1 . Cl2、SO2、CO2均是中学化学常见的气体,减少Cl2、SO2的排放可以防止污染空气,减少CO2的排放,有利于保护环境,实现碳中和。回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是________ 。
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=________ 。
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为________ (填化学式)。
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用________ (填试剂名称),SO2、Cl2均有漂白性,若将两者1∶1通入品红溶液中,不能使品红褪色,理由是________ (写离子方程式),除去SO2中的HCl可采用________ (填试剂名称)。
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:________ 。
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:
您最近一年使用:0次
2 . 实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
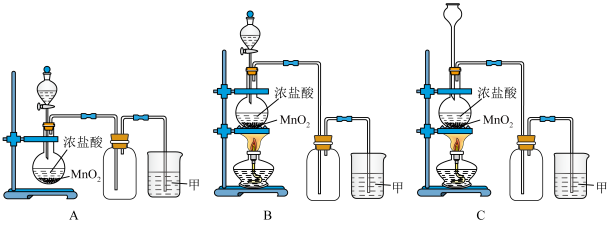
(1)A、B、C三套装置中,应选用的装置是___________ (选填“A”、“B”、“C”)。
(2)写出制取氯气的化学方程式___________ 。
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式___________ 。
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是___________ (用化学方程式说明)
(5)实验室也可用 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:___________ 。若反应中有5mol电子转移,被氧化HCl的的物质的量为___________ 。

(1)A、B、C三套装置中,应选用的装置是
(2)写出制取氯气的化学方程式
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是
(5)实验室也可用
 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:
您最近一年使用:0次
3 . 下表是生活生产中常见的物质:
(1)分别写出③、⑥的电离方程式__________ ;__________ 。
(2)③与⑥反应的离子方程式:__________ 。
(3)检验⑤的溶液中含有 的方法是:
的方法是:__________ ,有关的离子方程式为__________ 。
(4)常温下,将 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为__________ (填名称),检验中②阳离子的方法是__________ (填名称)。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
名称 | Na |
|
| 酒精 |
|
|
(2)③与⑥反应的离子方程式:
(3)检验⑤的溶液中含有
 的方法是:
的方法是:(4)常温下,将
 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为
您最近一年使用:0次
4 . 某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次
名校
5 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
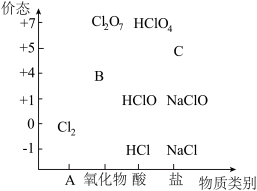
请回答下列问题:
(1)二维图中B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是___________ (填化学式,下同);C是一种钠盐,则C是___________ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与________ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_________ 性,可能与(填序号)___________ 发生反应。
(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:___________ 。
(4)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为___________ 。

请回答下列问题:
(1)二维图中B可以代替
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:(4)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
名校
6 . Ca(ClO)2、NaClO、FeCl3、Al2O3、Fe2O3、Mn2O7等都是重要的化合物。回答下列问题:
(1)属于酸性氧化物的是______ (填化学式),其相应的钾盐具有_____ (填“强氧化性”或“强还原性”),FeSO4溶液能使该钾盐的酸性溶液褪色,其原因为________ (用离子方程式解释)。
(2)属于“84"消毒液成分的是______ (填化学式),其在空气中易变质,产物之一为碳酸氢钠,写出发生该反应的离子方程式:_______ 。
(3)用覆铜板制作印刷电路板的原理是_______ (用离子方程式表示),检验“腐蚀液”中有无Fe3+的试剂为______ (填化学式)。
(4)将氯气通入冷的_____ (填物质名称)中可制得以Ca(ClO)2为有效成分的漂白粉,该过程中转移2mol电子时,消耗氧化剂与还原剂的质量之比为________ 。
(1)属于酸性氧化物的是
(2)属于“84"消毒液成分的是
(3)用覆铜板制作印刷电路板的原理是
(4)将氯气通入冷的
您最近一年使用:0次
名校
7 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)金属钠等活泼金属着火时,应该用___________ 来灭火,不能用水灭火的原因是___________ 。
(2)用下面方法可以制得白色的 沉淀。
沉淀。
用不含 的
的 溶液与用不含
溶液与用不含 的蒸馏水配制的NaOH溶液反应制备。
的蒸馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述 溶液时还需加入
溶液时还需加入___________ 。
②除去蒸馏水中溶解的 常采用
常采用___________ 的方法。
③如果没有除去氧气会看到白色沉淀变为红褐色沉淀,该反应的化学方程式为___________ 。
(3)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,发生反应的离子方程式是___________ 。为了安全,组织群众疏散的地方应是___________ (填序号)。
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(4)二氧化氯( )是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与
)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与 相比不会产生对人体有潜在危害的有机氯代物。可以由
相比不会产生对人体有潜在危害的有机氯代物。可以由 、
、 、
、 制备
制备 :
:
①配平下列方程式:___________


②上述反应中氧化剂是___________ 。
③若反应中有0.1mol电子转移,则产生的 气体在标准状况下的体积约为
气体在标准状况下的体积约为___________ L。
(1)金属钠等活泼金属着火时,应该用
(2)用下面方法可以制得白色的
 沉淀。
沉淀。用不含
 的
的 溶液与用不含
溶液与用不含 的蒸馏水配制的NaOH溶液反应制备。
的蒸馏水配制的NaOH溶液反应制备。①用硫酸亚铁晶体配制上述
 溶液时还需加入
溶液时还需加入②除去蒸馏水中溶解的
 常采用
常采用③如果没有除去氧气会看到白色沉淀变为红褐色沉淀,该反应的化学方程式为
(3)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,发生反应的离子方程式是
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(4)二氧化氯(
 )是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与
)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与 相比不会产生对人体有潜在危害的有机氯代物。可以由
相比不会产生对人体有潜在危害的有机氯代物。可以由 、
、 、
、 制备
制备 :
:①配平下列方程式:


②上述反应中氧化剂是
③若反应中有0.1mol电子转移,则产生的
 气体在标准状况下的体积约为
气体在标准状况下的体积约为
您最近一年使用:0次
8 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图中分别为钠和氯及其化合物的“价-类”二维图,请回答下列问题:

(1)填写二维图中缺失的化学式:①________ 、②________ 。
(2)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种________ 颜色气体。实验室沿用舍勒的方法制取Cl2的化学方程式为_________ 。
(3)常温下将Cl2通入NaOH溶液中,可以得到一中漂白液。上述反应的离子方程式为:________________ ,该漂白液的有效成分为________ (填名称)。
(4)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:________________ 。

(1)填写二维图中缺失的化学式:①
(2)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种
(3)常温下将Cl2通入NaOH溶液中,可以得到一中漂白液。上述反应的离子方程式为:
(4)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:
您最近一年使用:0次
名校
9 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是常见的几种消毒剂:①“84”消毒液(有效成分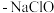 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠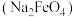 。回答下列问题:
。回答下列问题:
(1)上述杀菌消毒剂___________ (填序号)属于电解质,___________ (填序号)属于非电解质。“84”消毒液中有效成分的电离方程式为___________ 。
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”)。
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是___________ (用离子方程式表示)。
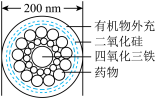
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。
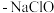 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠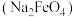 。回答下列问题:
。回答下列问题:(1)上述杀菌消毒剂
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。

| A.葡萄糖等大多数含碳化合物属于有机物 |
| B.该“纳米药物分子车"属于混合物 |
| C.该“纳米药物分子车”分散于水后能够透过半透膜 |
| D.该“纳米药物分子车”中的二氧化硅和四氧化三铁属于氧化物 |
您最近一年使用:0次
名校
解题方法
10 . 氯气可用于制取漂白剂和自来水消毒。
(1)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是_____ 。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中。反应的离子方程式为_____ 。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用H2SO4溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知,溶液中Cl2、HClO和ClO-占含氯元素微粒总数分数(α%)随溶液pH变化的关系如下图所示:
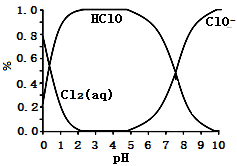

①由实验现象可获得以下结论:溶液的pH在4~10范围内,pH越大,红纸褪色_____ 。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_____ 。
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。一种制备ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为_____ 。
(1)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中。反应的离子方程式为
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用H2SO4溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色变得更浅;4h后红纸褪色 |


①由实验现象可获得以下结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。一种制备ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为
您最近一年使用:0次






