名校
解题方法
1 . 按要求回答下列问题:
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、___________ 和___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: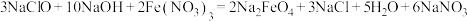 。回答下列问题:
。回答下列问题:
①用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
②制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为___________ L。
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、
(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: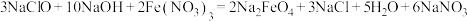 。回答下列问题:
。回答下列问题:①用氯气制备
 的反应原理为
的反应原理为②制备高铁酸钠的反应中
 体现了
体现了(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
2 . NaClO广泛用作水处理剂及漂白剂。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
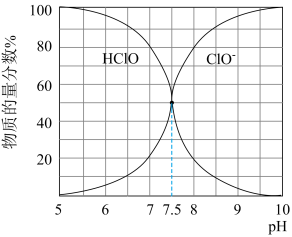
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
您最近一年使用:0次
名校
3 . 生产生活中常用84消毒液杀菌消毒。化学课外小组用Cl2和NaOH溶液制取84消毒液。请回答下列问题:
(1)制取84消毒液需要 的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为
的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为_____ ,配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、_____ ;定容时俯视刻度线将导致所配溶液浓度_____ (填“偏高”、“偏低”或“不影响”)。
(2)制取84消毒液的离子方程式为_____ 。
(3)该消毒液也用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出反应的化学方程式_____ 。
(4)已知酸性:H2CO3>HClO> ,向84消毒液中通入少量CO2的离子方程式为:
,向84消毒液中通入少量CO2的离子方程式为:_____ 。
(5)NaClO除了用于消毒外,在化工生产上常用作重要的氧化剂。比如,用NaClO和FeCl3溶液在NaOH的作用下制备一种新型水处理剂Na2FeO4,写出该反应的离子方程式:_____ 。
(1)制取84消毒液需要
 的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为
的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为(2)制取84消毒液的离子方程式为
(3)该消毒液也用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出反应的化学方程式
(4)已知酸性:H2CO3>HClO>
 ,向84消毒液中通入少量CO2的离子方程式为:
,向84消毒液中通入少量CO2的离子方程式为:(5)NaClO除了用于消毒外,在化工生产上常用作重要的氧化剂。比如,用NaClO和FeCl3溶液在NaOH的作用下制备一种新型水处理剂Na2FeO4,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 已知: 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: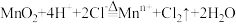 ,回答下列问题:
,回答下列问题:
(1)从方程式两边电荷守恒角度判断,方程式中
___________ 。
(2)该反应的还原剂是___________ ,实验室检验该离子的试剂是硝酸酸化的硝酸银溶液。
(3)该反应的还原产物是___________ 。
(4)若该反应消耗 ,产生标准状况下的
,产生标准状况下的
___________ L。
(5)实验室制取 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: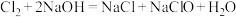 (已知:电离方程式
(已知:电离方程式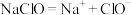 ),该反应的离子方程式为
),该反应的离子方程式为___________ 。
 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: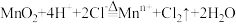 ,回答下列问题:
,回答下列问题:(1)从方程式两边电荷守恒角度判断,方程式中

(2)该反应的还原剂是
(3)该反应的还原产物是
(4)若该反应消耗
 ,产生标准状况下的
,产生标准状况下的
(5)实验室制取
 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: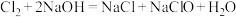 (已知:电离方程式
(已知:电离方程式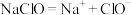 ),该反应的离子方程式为
),该反应的离子方程式为
您最近一年使用:0次
名校
5 . I.海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、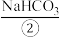 、
、 、
、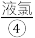 、
、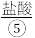 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出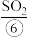 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼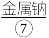 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同),既不属于电解质也不属于非电解质的是___________ 。
(2)写出③溶于水的电离方程式:___________ 。
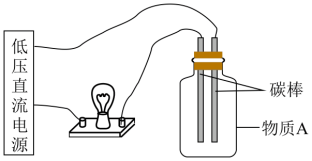
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是___________ 。(填序号)
(4) 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于___________ (填“酸性氧化物”、“碱性氧化物”或“不成盐氧化物”)
Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
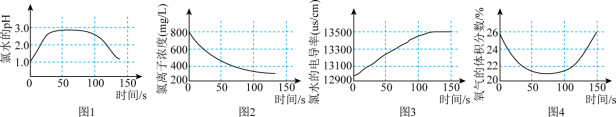
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。
(7)将氯气通入热的NaOH溶液中,反应得到NaCl, 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:___________ 。
 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、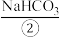 、
、 、
、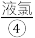 、
、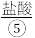 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出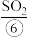 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼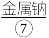 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出③溶于水的电离方程式:
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是

(4)
 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
A. | B. | C.Mg2+ | D. |
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时间的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
(7)将氯气通入热的NaOH溶液中,反应得到NaCl,
 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 根据信息和要求书写相关反应的方程式
(1)用84消毒液对新冠病毒进行消杀。将 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式___________ 。
(2) 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:_____ 。

(3)以 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:___________ 。
(1)用84消毒液对新冠病毒进行消杀。将
 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式(2)
 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
(3)以
 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . 如图为钠和氯的价类二维图,请据图完成下列问题:
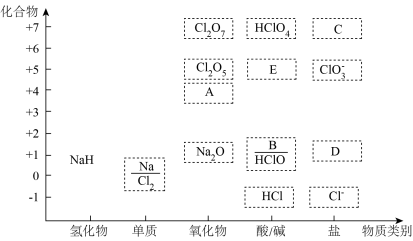
(1)NaH中的氢为___________ 价。可与水反应生成氢气,该反应中氧化产物和还原产物的质量比为___________ 。
(2)A是氯的氧化物,其化学式为___________ 。A可用于自来水消毒。其消毒效率是 的
的___________ 倍(还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。
(3)B属于碱,其水溶液与 反应生成D的离子方程式为
反应生成D的离子方程式为___________ 。
(4)C是高氯酸钠,受热分解可产生 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为___________ 。
(5) 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式___________ 。

(1)NaH中的氢为
(2)A是氯的氧化物,其化学式为
 的
的 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。(3)B属于碱,其水溶液与
 反应生成D的离子方程式为
反应生成D的离子方程式为(4)C是高氯酸钠,受热分解可产生
 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为(5)
 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
名校
8 . 按要求填空
(1)将含 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每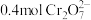 转移
转移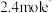 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ (用离子方程式表示)。
(3) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: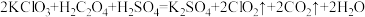 。产生
。产生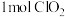 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ ;该反应中的氧化剂是___________ (填化学式)。
(1)将含
 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每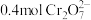 转移
转移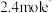 ,该反应的离子方程式为
,该反应的离子方程式为(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
(3)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: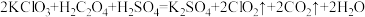 。产生
。产生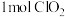 时,转移的电子的物质的量为
时,转移的电子的物质的量为
您最近一年使用:0次
名校
解题方法
9 . 写出下列反应的离子 方程式。
(1)氯气通入氢氧化钠溶液中:___________ ;
(2)冰醋酸中滴加氢氧化钾溶液:___________ ;
(3)实验室制备 :
:___________ ;
(4)氧化镁溶液中滴加氨水:___________ ;
(5)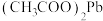 (弱电解质)溶液中滴加盐酸:
(弱电解质)溶液中滴加盐酸:___________ ;
(6)酸性高锰酸钾溶液中滴加淀粉碘化钾溶液,溶液变为蓝色:___________ 。
(1)氯气通入氢氧化钠溶液中:
(2)冰醋酸中滴加氢氧化钾溶液:
(3)实验室制备
 :
:(4)氧化镁溶液中滴加氨水:
(5)
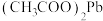 (弱电解质)溶液中滴加盐酸:
(弱电解质)溶液中滴加盐酸:(6)酸性高锰酸钾溶液中滴加淀粉碘化钾溶液,溶液变为蓝色:
您最近一年使用:0次
名校
10 . “84”消毒液是生活中常见的一种消毒剂,常用于环境的消毒,其主要成分是NaClO。
(1)“84”消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在10~20分钟左右、用化学方程式解释原因:___________ 。
(2)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式:___________ 。
 。
。
(3)“84”消毒液的制取和漂粉精的制取原理相同,请写出该反应的离子方程式:___________ 。
(4)消毒学专家指出,将“84”消毒液与洁厕灵(主要成分:浓盐酸)一起合并使用,可能会对使用者的呼吸道造成伤害。请用离子方程式分析可能的原因:___________ 。
(5)已知某市售84消毒液瓶体部分标签如图所示,该84消毒液通常稀释100倍(体积之比)后使用。请回答下列问题:
①该“84”消毒液中NaClO的物质的量浓度约为___________ mol/L。(保留1位小数)
②“84”消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用18.4mol/L的浓硫酸配制480mL2.3mol/L的稀硫酸用于增强84消毒液的消毒能力,则配置时需用浓硫酸的体积为___________ mL。
③在配制稀硫酸过程中不需要用到的仪器有___________ 。
A.玻璃棒 B.托盘天平 C.烧杯 D.量筒 E.容量瓶 F.漏斗
④配制该稀硫酸过程中,下列情况会使所配制的溶液的浓度大于2.3mol/L的有___________ 。
A.未经冷却趁热将溶液注入容量瓶中并进行定容
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视容量瓶刻度线
(1)“84”消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在10~20分钟左右、用化学方程式解释原因:
(2)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式:
 。
。(3)“84”消毒液的制取和漂粉精的制取原理相同,请写出该反应的离子方程式:
(4)消毒学专家指出,将“84”消毒液与洁厕灵(主要成分:浓盐酸)一起合并使用,可能会对使用者的呼吸道造成伤害。请用离子方程式分析可能的原因:
(5)已知某市售84消毒液瓶体部分标签如图所示,该84消毒液通常稀释100倍(体积之比)后使用。请回答下列问题:
| 84消毒液 [有效成分]NaClO [规格]1000mL [质量分数]25% [密度] 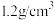 |
②“84”消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用18.4mol/L的浓硫酸配制480mL2.3mol/L的稀硫酸用于增强84消毒液的消毒能力,则配置时需用浓硫酸的体积为
③在配制稀硫酸过程中不需要用到的仪器有
A.玻璃棒 B.托盘天平 C.烧杯 D.量筒 E.容量瓶 F.漏斗
④配制该稀硫酸过程中,下列情况会使所配制的溶液的浓度大于2.3mol/L的有
A.未经冷却趁热将溶液注入容量瓶中并进行定容
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视容量瓶刻度线
您最近一年使用:0次
2023-11-29更新
|
236次组卷
|
2卷引用:辽宁省沈阳市五校协作体2023-2024学年高一上学期11月期中考试化学试题



