名校
解题方法
1 . 回答下列问题:
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)9.03×1023个CO2的物质的量是_______ ,在标准状况下的体积为_______ 。
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为_______ ,所含氧原子数之比为_______ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=_______ 。
(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为_______ 。
(6)FeCl2溶液通入氯气的反应,用离子方程式表示_______ 。
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为_______ ,该反应中被还原的物质是_______ (填化学式)。
(1)NaClO中Cl的化合价为
(2)9.03×1023个CO2的物质的量是
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
(6)FeCl2溶液通入氯气的反应,用离子方程式表示
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为
您最近一年使用:0次
2023-10-05更新
|
258次组卷
|
2卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一上学期11月期中考试化学试题
2 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式___________ 。
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式___________ 。
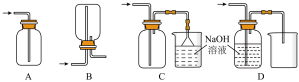
②下列收集Cl2的正确装置是___________ 。
③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为___________ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,发生反应的离子方程式为________ 、_________ 。
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
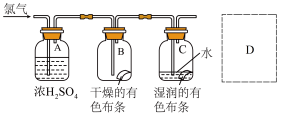
i.浓H2SO4的作用是___________ 。
ii.与研究目的直接相关的实验现象是___________ 。
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为___________ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式
②下列收集Cl2的正确装置是

③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

i.浓H2SO4的作用是
ii.与研究目的直接相关的实验现象是
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 完成下列问题。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是___________ (填化学式);用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是___________ (用化学方程式表示)。
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是___________ ;漂白粉也能用于消毒,其有效成分生效的化学方程是___________ 。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是
您最近一年使用:0次
解题方法
4 . 完成下列小题
(1)写出实验室制备氯气的化学方程式_____ 。
(2)常温下, 通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:
通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:_____ 。
(3)请用单线桥法标出此反应电子转移方向和数目:_____ 。
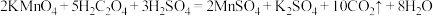
(4)现有下列七种物质:
① 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦Na
⑦Na
在上述物质中,能导电的是_____ ;属于电解质的是_____ 。
(1)写出实验室制备氯气的化学方程式
(2)常温下,
 通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:
通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:(3)请用单线桥法标出此反应电子转移方向和数目:
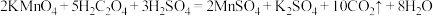
(4)现有下列七种物质:
①
 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦Na
⑦Na在上述物质中,能导电的是
您最近一年使用:0次
5 . 按要求完成下列填空
(1)写出下列物质在水溶液中的电离方程式:
①
___________
②
___________
(2)写出下列反应的化学方程式:
①除去 粉末中混有的少量
粉末中混有的少量 所涉及的反应:
所涉及的反应:___________ ;
②在消防员的呼吸面具中, 与
与 发生的反应:
发生的反应:___________ ;
③将 通入冷的石灰乳中制漂白粉:
通入冷的石灰乳中制漂白粉:___________ ;
④ 在空气中久置变成红褐色:
在空气中久置变成红褐色:___________ 。
(3)写出下列反应的离子方程式:
①钠与水的反应:___________ ;
② 与水的反应:
与水的反应:___________ ;
③除去 溶液中混有的少量
溶液中混有的少量 :
:___________ 。
(1)写出下列物质在水溶液中的电离方程式:
①

②

(2)写出下列反应的化学方程式:
①除去
 粉末中混有的少量
粉末中混有的少量 所涉及的反应:
所涉及的反应:②在消防员的呼吸面具中,
 与
与 发生的反应:
发生的反应:③将
 通入冷的石灰乳中制漂白粉:
通入冷的石灰乳中制漂白粉:④
 在空气中久置变成红褐色:
在空气中久置变成红褐色:(3)写出下列反应的离子方程式:
①钠与水的反应:
②
 与水的反应:
与水的反应:③除去
 溶液中混有的少量
溶液中混有的少量 :
:
您最近一年使用:0次
6 . 含氯消毒剂、过氧化物能有效灭活病毒,是常用消毒剂。请回答下列问题:
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为________ 。
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为________ 。
(3)兴趣小组设计如下图实验装置制取少量消毒液。
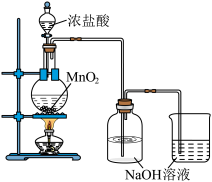
①MnO2与浓HCl反应的离子方程式为________ 。
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有________ (用文字简述)。
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为________ 。
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(3)兴趣小组设计如下图实验装置制取少量消毒液。

①MnO2与浓HCl反应的离子方程式为
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为
您最近一年使用:0次
7 . 资料:“84”消毒液中含氯微粒主要有ClO-、Cl-、HClO,相同浓度时,HClO的氧化性强于ClO-。通常情况下,应将“84”消毒液原液稀释后使用,一般不用于衣服等纺织品的洗涤消毒。
(1)常温,将氯气通入NaOH溶液中可制得“84”消毒液,该反应的化学方程式为_______ 。
(2)已知某“84”消毒液瓶体部分标签如图所示,请回答下列问题。
①该“84”消毒液的物质的量浓度为_______ mol/L。
②“84”消毒液使用时需要稀释,某小组用上述“84”消毒液配制500 mL 0.2mol/L的稀溶液,需要用量筒量取该“84”消毒液体积为_______ mL。
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是_______ 。
A.容量瓶使用时未干燥 B.没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线 D.定容后液面低于刻度线,再加蒸馏水至刻度线
(3)为研究“84”消毒液的性质与使用条件,进行下列实验:
向三支试管中分别加入2 mL“84”消毒液和5滴紫色石蕊。继续进行如下实验:
①实验1中NaClO溶液与空气中二氧化碳反应的离子方程式为_______ 。(已知酸性: )
)
②实验3中生成气体的离子方程式为_______ 。
③综合以上实验为提高单位时间内“84”消毒液的漂白效果,你的建议是_______ 。
(1)常温,将氯气通入NaOH溶液中可制得“84”消毒液,该反应的化学方程式为
(2)已知某“84”消毒液瓶体部分标签如图所示,请回答下列问题。
| “84”消毒液 有效成分:NaClO 规格:1000 mL 质量分数:25% 密度:1.192g/cm3 |
②“84”消毒液使用时需要稀释,某小组用上述“84”消毒液配制500 mL 0.2mol/L的稀溶液,需要用量筒量取该“84”消毒液体积为
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是
A.容量瓶使用时未干燥 B.没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线 D.定容后液面低于刻度线,再加蒸馏水至刻度线
(3)为研究“84”消毒液的性质与使用条件,进行下列实验:
向三支试管中分别加入2 mL“84”消毒液和5滴紫色石蕊。继续进行如下实验:
| 实验 | 操作 | 现象 |
| 实验1 | 加入2 mL蒸馏水 | 短时间内未褪色,一段时间后蓝色褪去 |
| 实验2 | 加入2 mL 0.0002 mol/L的H2SO4溶液 | 蓝色迅速褪去,无气体产生 |
| 实验3 | 加入2 mL 2 mol/L的H2SO4溶液 | 蓝色迅速褪去,并产生大量刺激性的气体 |
 )
)②实验3中生成气体的离子方程式为
③综合以上实验为提高单位时间内“84”消毒液的漂白效果,你的建议是
您最近一年使用:0次
名校
8 . 钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,常用N来杀菌消毒。请按要求填空:
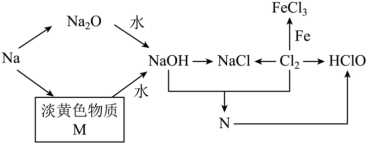
(1)淡黄色物质M是__________ ,物质N是__________ (填化学式)。
(2)写出M与水反应的化学方程式为__________ ,氧化剂为__________ ,还原剂为__________ 。
(3)请描述一小块金属钠投入 溶液中的现象:
溶液中的现象:__________ 。
(4) 与
与 反应的化学反应方程式为
反应的化学反应方程式为__________ 。
(5)除去下列括号中少量杂质,写出相关化学方程式或离子方程式:
①除去 固体混有
固体混有 的化学方程式:
的化学方程式:__________ 。
②除去 溶液中混有
溶液中混有 的离子方程式:
的离子方程式:__________ 。

(1)淡黄色物质M是
(2)写出M与水反应的化学方程式为
(3)请描述一小块金属钠投入
 溶液中的现象:
溶液中的现象:(4)
 与
与 反应的化学反应方程式为
反应的化学反应方程式为(5)除去下列括号中少量杂质,写出相关化学方程式或离子方程式:
①除去
 固体混有
固体混有 的化学方程式:
的化学方程式:②除去
 溶液中混有
溶液中混有 的离子方程式:
的离子方程式:
您最近一年使用:0次
9 . 利用图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为______ ;丁属于______ (“酸性”或“碱性”)氧化物。
(2)图中甲、乙、丁、戊中,属于电解质的是_____ (填化学式);根据氯元素的化合价判断,乙物质的性质______ (填标号)。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是_____ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_____ 。NaClO溶液中显碱性原因:______ (用离子方程式表示)。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为______ 。

(1)丙的化学式为
(2)图中甲、乙、丁、戊中,属于电解质的是
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O
 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为
您最近一年使用:0次
名校
10 . 回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
您最近一年使用:0次



