1 . 某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
解题方法
2 . 科学的分类能够反映事物的本质特征,运用分类的方法,可以发现物质及其变化的规律。基于物质类别和元素价态,可以设计物质间转化的途径。请根据下列物质回答相关问题:
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是_______ (填序号)
(2)Ⅰ.某同学用含钠元素的不同类别 物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2 2NaCl
2NaCl
b.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:_______ ;d:_______ 。
Ⅱ.另一位同学从含氯元素的不同价态 考虑,认为Cl2与NaOH溶液反应也可以生成NaCl,请写出此方法的化学反应方程式_______ 。
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为_______ ;请用单线桥法 在离子反应方程式上标出电子转移的方向和数目_______ 。
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是
(2)Ⅰ.某同学用
a.2Na+Cl2
 2NaCl
2NaClb.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:
Ⅱ.另一位同学从
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
3 . 完成下列问题
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)___________ ;
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
(3)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因:___________ 。
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
| A.O2 | B.Cl2 | C.CO2 | D.HClO |
您最近一年使用:0次
2022-04-05更新
|
46次组卷
|
2卷引用:安徽工业大学附属中学2020-2021学年高二上学期文理分科考试化学试题
名校
解题方法
4 . NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次
名校
5 . 已知钠、氯及其化合物间有如下转化关系,请按要求填空。
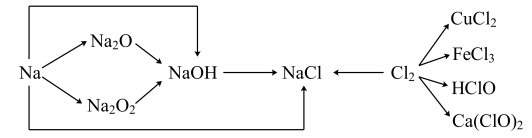
(1)一小块金属钠投入水中反应的化学方程式是___________ 。若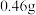 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是___________ L,若反应后所得溶液为 ,则
,则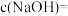
___________  。
。
(2) 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为___________ 、___________ 。
(3)新制的氯水中加入打磨过的镁条,观察到的现象是___________ ;请写出氯气与水反应的化学方程式:___________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为___________ 。

(1)一小块金属钠投入水中反应的化学方程式是
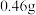 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是 ,则
,则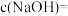
 。
。(2)
 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为(3)新制的氯水中加入打磨过的镁条,观察到的现象是
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
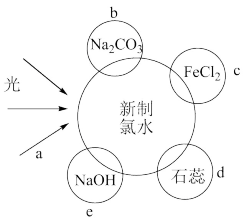
(1)氯水中含有的粒子有H2O、Cl2、___________ 、H+、Cl-、___________ 、OH-七种。
(2)久置的氯水变为___________ ,原因是___________ (用化学反应方程式表示);实验室保存饱和氯水的方法是___________ 。
(3)b过程中的离子方程式是___________ 。
(4)e过程中所发生的主要反应的化学方程式为___________ 。
(5)能证明氯水具有漂白性的是___________ (填“a”、“b”、“c”或“d”)。

(1)氯水中含有的粒子有H2O、Cl2、
(2)久置的氯水变为
(3)b过程中的离子方程式是
(4)e过程中所发生的主要反应的化学方程式为
(5)能证明氯水具有漂白性的是
您最近一年使用:0次
名校
解题方法
7 . 如图是元素周期表的一部分,主族元素A、B、C、D、E在元素周期表中的位置如图,A元素的单质在空气中含量最高(请用相应的元素符号或化学式作答)∶
(1)A简单离子结构示意图_______
(2)下列说法不正确的是_______
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为_______ ,A和D氢化物沸点的大小为_______ 。
(4)设计实验比较D与E的非金属性强(用离子方程式表示)_______ 。
(5)A2的结构式_____ ,CB4的电子式为____ ,CB4溶于NaOH溶液的化学方程式____ 。
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式_______ 。
| A | B | ||
| C | D | E |
(1)A简单离子结构示意图
(2)下列说法不正确的是
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为
(4)设计实验比较D与E的非金属性强(用离子方程式表示)
(5)A2的结构式
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式
您最近一年使用:0次
名校
8 . 按要求填空:
(1)写出钠与水反应的离子方程式:___________ 。
(2)过氧化钠的颜色为:___________ ,其阳离子和阴离子的个数比为___________ ,写出过氧化钠与水反应的化学方程式:___________ 。
(3)写出氯的原子结构示意图:___________ , 写出工业制漂白粉的化学方程式:___________ 。
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:___________ 。
(1)写出钠与水反应的离子方程式:
(2)过氧化钠的颜色为:
(3)写出氯的原子结构示意图:
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:
您最近一年使用:0次
9 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式__ 。
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式__ 。
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式__ 。
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为__ ,制备漂白粉的离子方程式为__ 。
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为__ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,反应的离子方程式为__ ,除了钠与水反应的现象其余可以观察到的现象是__ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为
您最近一年使用:0次
10 . 将 通入NaOH溶液制备84消毒液(有效成分为
通入NaOH溶液制备84消毒液(有效成分为 ),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
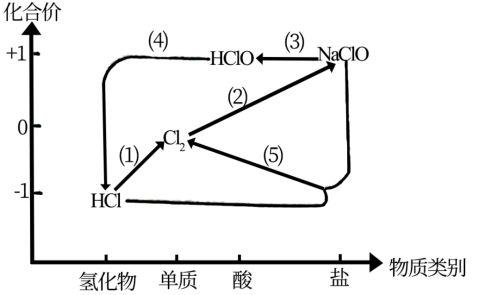
(1)实验室用二氧化锰和浓盐酸反成制备氯气的化学方程式为_______ 。
(2)制备84消毒液的离子方程式为_______ 。
(3)84消毒液中加入少量醋酸( )可增强效果,该反应的化学方程式为
)可增强效果,该反应的化学方程式为_______ 。
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为_______ 。
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为_______ (用离子反应方程式表示)。
 通入NaOH溶液制备84消毒液(有效成分为
通入NaOH溶液制备84消毒液(有效成分为 ),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
(1)实验室用二氧化锰和浓盐酸反成制备氯气的化学方程式为
(2)制备84消毒液的离子方程式为
(3)84消毒液中加入少量醋酸(
 )可增强效果,该反应的化学方程式为
)可增强效果,该反应的化学方程式为(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为
您最近一年使用:0次
2021-01-24更新
|
309次组卷
|
3卷引用:安徽省滁州市凤阳县凤阳中学2020-2021学年高一(上学期)第二次月考化学试卷



