1 . (1)意大利罗马大学的FulvioCacsce 等人获得了极具理论研究意义的N4 分子。N4与N2是氮元素的______________ ,它们的性质_____________ 。(填“相同”或“不同”)
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C= K2S+N2↑ +3CO2↑,反应中被还原的物质是______________ (填化学式)
(3)过氧化钠与CO2反应的化学方程式:_______________________________________ ;其中氧化剂是________________ ,还原剂是___________________ 。
(4)在常温下,将氯气通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式___________________________________ 。该漂白液的有效成分是___________ (填名称)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C= K2S+N2↑ +3CO2↑,反应中被还原的物质是
(3)过氧化钠与CO2反应的化学方程式:
(4)在常温下,将氯气通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式
您最近一年使用:0次
2 . 甲型H1N1流感病毒曾在全球广泛传播,给人类健康、社会经济带来了巨大的负面影响。我国采取积极应对措施,使病毒得到了有效的控制,从很大程度上减少了损失,在这里,消毒液功不可没。
(1)生产消毒液是将氯气通入NaOH溶液中,该反应的离子方程式为________ 。
(2)取少量消毒液滴加AgNO3溶液,现象是出现白色沉淀,说明消毒液中有____ 离子(写离子符号),该反应的的离子方程式为____________ 。
(3)消毒液稀释后喷洒在空气中,可以生成具有漂白性的物质,该物质为_________ ;该物质有漂白性是因为它有强的氧化性,但是它也很不稳定,写出它分解反应的化学方程式:_________ 。
(1)生产消毒液是将氯气通入NaOH溶液中,该反应的离子方程式为
(2)取少量消毒液滴加AgNO3溶液,现象是出现白色沉淀,说明消毒液中有
(3)消毒液稀释后喷洒在空气中,可以生成具有漂白性的物质,该物质为
您最近一年使用:0次
3 . 含氯的物质与人们的生活密切相关。已知氯元素常见的化合价有-1、0、+1、+3、+5、+7六种,其不同价态的物质间可相互转化。回答下列问题:
(1)氯原子的原子结构示意图___ ;氯离子的电子式___ 。
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是____ (写名称),漂粉精的主要有效成分是___ (写化学式)。
(3)实验室制取氯化氢的化学方程式____ 。
(4)工业上将含有氯气的尾气通过___ 进行处理,在处理时发生的反应中氯气作为____ 。
a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途____ 、____ 。
(1)氯原子的原子结构示意图
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是
(3)实验室制取氯化氢的化学方程式
(4)工业上将含有氯气的尾气通过
a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途
您最近一年使用:0次
4 . 元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__ ,自然界中存在的54Fe和56Fe,它们互称为___ 。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__ 。通常证明某溶液中含Fe2+的化学方法是___ 。
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__ 相同。处于同一列的N和P位于元素周期表的__ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_ ,其气态氢化物的结构式为__ 。
②与硅元素处于同一周期,两性金属元素是__ ,并写出其在元素周期表中的位置:第__ 周期,__ 族,该元素的最高价氧化物对应水化物的电离方程式为__ 。
③第三周期半径最大的金属元素__ ,该元素形成氢氧化物的电子式_ ,检验物质中是否含有该元素的方法是:__ 。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__ (写化学式)。该元素与硫元素相比,非金属性较强的元素是__ (填元素符号),请写出证明该结论的一个实验事实:__ 。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___ 。

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__ 族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__ 。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②与硅元素处于同一周期,两性金属元素是
③第三周期半径最大的金属元素
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次
5 . 将一小块钠用小刀切开,可以看到表面光亮,但很快变暗,该反应的化学方程式为__________ ,若将钠块放到石棉网上加热会生成______ 色固体,该反应的化学方程式为_______ ,该固体遇水会有无色无味的气体生成,该反应的化学方程式为___________ ,将氯气通入反应后的溶液中,发生反应的化学方程式为_________ 。
您最近一年使用:0次
名校
6 . 在高锰酸钾固体上滴加浓盐酸,马上产生黄绿色气体。反应的化学方程式为:2KMnO4 + 16HCl=2KC1 + 2MnCl2 + 5C12↑+ 8H2O
回答下列问题:
(1)此反应中的氧化剂是____ ,当在标准状况下产生0.112L氯气,转移的电子数为____ mol。
(2)氯原子的核电荷数为______ ;氧原子的原子结构示意图_______ 。
(3)在KC1固体中存在的化学键是__________ ;写出H2O电子式_________ 。
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是_________ 。
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。_________ 。
回答下列问题:
(1)此反应中的氧化剂是
(2)氯原子的核电荷数为
(3)在KC1固体中存在的化学键是
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。
您最近一年使用:0次
7 . 钠、铁、镁等元素在生产生活中有广泛的用途,完成下列填空:
Ⅰ钠的重要化合物
(1)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯气需要0.56g硫代硫酸钠,反应的离子方程式为______ 。
(2)除去Al2O3中混有的Fe2O3,可将混合物溶于过量的盐酸,再加入Na2CO3调节pH使Fe3+沉淀完全而Al3+不沉淀,用化学用语及相应的离子方程式解释加入Na2CO3的目的______ 。
Ⅱ铁的重要化合物
(3)磷酸铁(FePO4•2H2O是难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
①称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是______ 。
②向滤液中加入一定量H2O2氧化Fe2+,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、______ 和______ 。
③将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为______ 。
Ⅲ镁的重要化合物
(4)氧化镁和碳粉与氯气在一定条件下反应可制备氯化镁,若尾气可用足量的氢氧化钠溶液完全吸收,则生成的盐为______ 。
Ⅰ钠的重要化合物
(1)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯气需要0.56g硫代硫酸钠,反应的离子方程式为
(2)除去Al2O3中混有的Fe2O3,可将混合物溶于过量的盐酸,再加入Na2CO3调节pH使Fe3+沉淀完全而Al3+不沉淀,用化学用语及相应的离子方程式解释加入Na2CO3的目的
Ⅱ铁的重要化合物
(3)磷酸铁(FePO4•2H2O是难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
①称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是
②向滤液中加入一定量H2O2氧化Fe2+,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、
③将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为
Ⅲ镁的重要化合物
(4)氧化镁和碳粉与氯气在一定条件下反应可制备氯化镁,若尾气可用足量的氢氧化钠溶液完全吸收,则生成的盐为
您最近一年使用:0次
8 . 含氯消毒剂在生产生活中有着广泛的用途。完成下列填空:
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为_________ 。
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是_______________________________ ;“84消毒液”不能对钢铁制品进行消毒,原因是____________ 。
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是__________ ;处理从氯化塔中逸出气体的方法是_____ 。
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为_________ 。
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________________________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为
您最近一年使用:0次
名校
9 . 2004年4月15日,重庆某化工厂氯气泄漏并发生爆炸,爆炸现场弥漫着黄色烟雾,这起事故共造成7人丧生,并致使近15万群众紧急疏散。问题:
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为___________________________________ ;形成烟的成分包含Cl2与Fe反应的产物___________ ,Cl2是一种有毒气体,为消除毒气,消防部门用消防用水与碱液在外围50米处形成两道水幕进行稀释,写出Cl2与强碱溶液反应的离子方程式__________________________________ 。
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:________________________________ 。
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,该反应中氧化剂是_______ ,还原剂是_______ ,氧化剂与还原剂的物质的量之比为_________ ;若生成1mol ClO2则转移电子数为____________ (NA表示阿伏伽德罗常数)。
(1)爆炸现场弥漫的黄色烟雾,除氯气外,形成雾的主要原因是Cl2与水反应,反应的化学方程式为
(2)Cl2及其无机产品常用做消毒剂,如“84消毒液”(NaClO)、“漂白粉”等,它们的消毒原理都是在潮湿的空气中与CO2和水蒸气反应生成了次氯酸,请写出“84消毒液”(NaClO)在空气中发生作用的化学方程式:
(3)用氯气对饮用水消毒已经有百年的历史,这种消毒的方法中氯气会与水中的有机物发生氯代生成对人体有害的的氯代物,于是世界环保联盟建议推广广谱高效消毒剂二氧化氯(ClO2),制取二氧化氯的其中一种方法是:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O,该反应中氧化剂是
您最近一年使用:0次
10 . 以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下(氯化过程中少量Ca(ClO)2分解为CaCl2和O2):
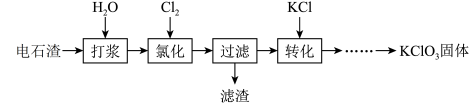
(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为__________________________________________________ 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________ (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为__________ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]________ 1∶5(填“>”、“<”或“=”)。

(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]
您最近一年使用:0次



