名校
1 . 2020年突如其来的“新冠病毒”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉、二氧化氯都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84“消毒液,可以说化学让生活更美好。
图为“84”消毒液说明书。
请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式_______ , 若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO 和NaClO3的混合液。当混合液中Cl-和 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为_______ 。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目_______ 。
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐( ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是_______ (填字母)。
a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为: +FeS2+H+
+FeS2+H+ 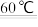 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式_______ 。
图为“84”消毒液说明书。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~ 60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1: 200水溶液餐饮具,瓜果等1: 100 水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式
 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(
 ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为:
 +FeS2+H+
+FeS2+H+ 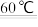 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
2 . 分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为_______ ;(CN)2称为“拟卤素”,具有类似Cl2的化学性质,则(CN)2与NaOH水溶液反应的化学方程式为_______ 。
您最近一年使用:0次
3 . 1984年我国研制出有效杀灭肝炎病毒的消毒液,命名为“84消毒液”。完成下列问题。
(1)实验室“84 消毒液”可通过将氯气通入冷而稀的氢氧化钠溶液获得,写出该反应的离子方程式_______ 。

(2)“84消毒液”与洁厕灵(主要成分为盐酸)混用,会产生黄绿色有毒气体。反应离子方程式为_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(3)将“84 消毒液”与 同时用于织物漂白,效果不佳,原因
同时用于织物漂白,效果不佳,原因 _______ (用离子方程式表示)。
(4)高铁酸钠 是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
①某兴趣小组欲用 固体配制
固体配制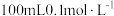 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为_______ g 。配制所用的容量瓶上标有
。配制所用的容量瓶上标有_______ 、_______ 、刻度线。
②下列操作导致浓度偏低的是_______ 。
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
(1)实验室“84 消毒液”可通过将氯气通入冷而稀的氢氧化钠溶液获得,写出该反应的离子方程式

(2)“84消毒液”与洁厕灵(主要成分为盐酸)混用,会产生黄绿色有毒气体。反应离子方程式为
(3)将“84 消毒液”与
 同时用于织物漂白,效果不佳,原因
同时用于织物漂白,效果不佳,原因 (4)高铁酸钠
 是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。①某兴趣小组欲用
 固体配制
固体配制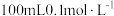 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为 。配制所用的容量瓶上标有
。配制所用的容量瓶上标有②下列操作导致浓度偏低的是
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
您最近一年使用:0次
4 . 工业上,我们用电解饱和食盐水制取氯气,请写出其中的化学方程式:_______ ,阳极产物是_______ 。实验室制备氯气时,为防止氯气污染空气,通常将氯气通入氢氧化钠溶液中,写出化学方程式:_______ ;对应的离子方程式_______ 。
您最近一年使用:0次
解题方法
5 . 工业上是将氯气通入到 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为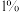 ,则生产
,则生产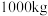 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为_______  (保留整数)。
(保留整数)。
 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为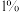 ,则生产
,则生产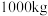 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为 (保留整数)。
(保留整数)。
您最近一年使用:0次
解题方法
6 . 现有以下物质:①Cl2②SO2③Na2O④NaHSO4⑤漂白粉⑥NaOH溶液⑦Ba(OH)2。回答下列问题:
(1)上述物质中,属于酸性氧化物的有_______ (填标号,下同),属于电解质的有_______ ,⑤的有效成分为_______ (填化学式)。
(2)将②通入足量⑥中,发生反应的离子方程式为_______ 。
(3)④在熔融状态下的电离方程式_______ 。
(4)向⑥中通入适量①可制取84消毒液,反应的化学方程式_______ 。
(1)上述物质中,属于酸性氧化物的有
(2)将②通入足量⑥中,发生反应的离子方程式为
(3)④在熔融状态下的电离方程式
(4)向⑥中通入适量①可制取84消毒液,反应的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
396次组卷
|
3卷引用:四川省泸州市泸县2022-2023学年高一下学期开学考试化学试题
8 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
9 . 某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
解题方法
10 . 氯气是一种非常重要的化工原料,可用于制造盐酸、漂白剂、农药等,但氯气有毒,使用或接触到有关物质时应注意安全。请回答下列问题:
(1)新制氯水中,含有氯元素的微粒有___________ (填微粒符号,下同,不考虑水中杂质与氯气的反应),其中使新制氯水显淡黄绿色的微粒是___________ 。
(2) 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为___________ L。
(3)标准状况下,氯气的密度为___________ 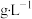 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是___________ (填序号)。
a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为___________ ;通常不用澄清石灰水吸收氯气的原因是___________ 。
(1)新制氯水中,含有氯元素的微粒有
(2)
 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为(3)标准状况下,氯气的密度为
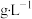 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为
您最近一年使用:0次



