1 . 汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是_______ 。
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)写出催化转化器中,一氧化碳和一氧化氮反应的化学方程式为_______ 。
(3)下列措施中有利于控制城市空气污染的是_______ 。
a.推广电动汽车 b.加快煤炭开采和使用 c.开发和使用氢能
(4)可利用 等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出
等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出 与NO反应的化学方程式
与NO反应的化学方程式_______ 。
(5)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: 。若反应时消耗了10L 0.1
。若反应时消耗了10L 0.1 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量_______ mol。
(1)汽车尾气中易造成光化学烟雾的物质是
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)写出催化转化器中,一氧化碳和一氧化氮反应的化学方程式为
(3)下列措施中有利于控制城市空气污染的是
a.推广电动汽车 b.加快煤炭开采和使用 c.开发和使用氢能
(4)可利用
 等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出
等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出 与NO反应的化学方程式
与NO反应的化学方程式(5)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 。若反应时消耗了10L 0.1
。若反应时消耗了10L 0.1 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量
您最近一年使用:0次
2022-05-28更新
|
553次组卷
|
5卷引用:江苏省徐州市沛县2021-2022学年高一下学期第二次学情调研化学试题
江苏省徐州市沛县2021-2022学年高一下学期第二次学情调研化学试题(已下线)专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)第5讲 氮及其化合物江苏省常州市联盟学校2022-2023学年高一下学期期末考试化学试题江苏省盐城市五校联考2023-2024学年高二上学期10月月考化学试题
2022高一·全国·专题练习
2 . 硝酸型酸雨及治理
(1)形成原理:_______ 。
(2)治理:工业尾气中的NOx一般用烧碱吸收,汽车尾气一般进行催化转化。
①碱液吸收:2NO2+2NaOH=NaNO3+NaNO2+H2O NO2+NO+2NaOH=2NaNO2+H2O
②催化转化:2NO2+4CO N2+4CO2
N2+4CO2
(1)形成原理:
(2)治理:工业尾气中的NOx一般用烧碱吸收,汽车尾气一般进行催化转化。
①碱液吸收:2NO2+2NaOH=NaNO3+NaNO2+H2O NO2+NO+2NaOH=2NaNO2+H2O
②催化转化:2NO2+4CO
 N2+4CO2
N2+4CO2
您最近一年使用:0次
名校
3 . 利用固体表面催化工艺进行NO分解的过程如图所示。

下列说法不正确 的是

下列说法
| A.NO是无色有毒气体 | B.催化剂能改变NO的分解速率 |
C.NO分解生成 和 和 | D.过程②释放能量,过程③吸收能量 |
您最近一年使用:0次
解题方法
4 . 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH 、NO
、NO 、NO
、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO
2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO 、NO
、NO 转化为N2。在指定条件下,下列选项所示的物质间转化
转化为N2。在指定条件下,下列选项所示的物质间转化不能 实现的是
 、NO
、NO 、NO
、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO
2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO 、NO
、NO 转化为N2。在指定条件下,下列选项所示的物质间转化
转化为N2。在指定条件下,下列选项所示的物质间转化A.N2(g)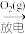 NO(g) NO(g) | B.NO(g) NaNO2(aq) NaNO2(aq) |
C.NH3(g)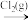 N2(g) N2(g) | D.NO2(g) HNO3(aq) HNO3(aq) |
您最近一年使用:0次
名校
解题方法
5 . 下列关于下图的叙述正确的是

①装置甲是利用外接电源的阴极保护法来防止铁钉生锈
②实验室常用装置乙来做NaCl溶液蒸发结晶的实验
③装置丙可除去乙烷中混有的乙烯
④装置丁可用于收集一氧化氮
⑤装置戊可用来验证 在水中的溶解性
在水中的溶解性

①装置甲是利用外接电源的阴极保护法来防止铁钉生锈
②实验室常用装置乙来做NaCl溶液蒸发结晶的实验
③装置丙可除去乙烷中混有的乙烯
④装置丁可用于收集一氧化氮
⑤装置戊可用来验证
 在水中的溶解性
在水中的溶解性| A.①③⑤ | B.①④⑤ | C.②③④ | D.①②④ |
您最近一年使用:0次
2022-05-26更新
|
240次组卷
|
2卷引用:重庆市巴蜀中学2022届高三适应性月考化学试题
6 . 下列说法正确的是
| A.SO2 和Cl2 均使品红溶液褪色,将同体积的SO2 和Cl2 混合通入水中,漂白能力增强 |
| B.用向上排空气法收集铜粉与稀硝酸反应产生的NO |
| C.浓硫酸与过量的铜加热反应,可以得到能使品红溶液褪色的SO2气体 |
D.检验 时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验生成的气体 时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验生成的气体 |
您最近一年使用:0次
7 . 实验室设计下列装置,不能达到目的的是
 |  |  |  |
| A.制取NH3 | B.干燥SO2 | C.Cl2“喷泉”实验 | D.收集NO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 研究硝酸工业尾气的处理对环境保护和资源的开发利用有重要意义。一种利用硝酸尾气初步处理后获得的高浓度NOx(NO、NO2)烟气制备NaNO2、NaNO3的工艺流程如下:
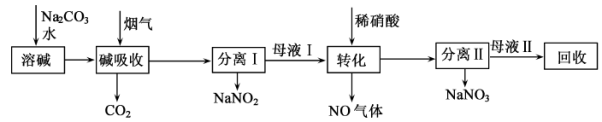
回答下列问题:
(1)NH3是工业上制备硝酸的原料,工业上NH3的催化氧化反应的化学方程式为_______ 。
(2)NaNO2中N元素的化合价为____ ,“碱吸收”过程中发生反应的离子方程式为______ 。
(3)母液I“转化”时生成NO的化学方程式为_______ ,“转化”时产生的气体应导入_______ (填操作单元的名称)循环利用。
(4)工业制硝酸尾气中的NOx(NO、NO2)常用NaOH溶液吸收,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O。硝酸尾气中的NOx,通入足量NaOH溶液中充分反应后气体没有剩余,则:
①NOx中x的取值范围为_______ ;
②反应后溶液中n( ):n(
):n( )=
)=_______ (用含x的代数式表示)。

回答下列问题:
(1)NH3是工业上制备硝酸的原料,工业上NH3的催化氧化反应的化学方程式为
(2)NaNO2中N元素的化合价为
(3)母液I“转化”时生成NO的化学方程式为
(4)工业制硝酸尾气中的NOx(NO、NO2)常用NaOH溶液吸收,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O。硝酸尾气中的NOx,通入足量NaOH溶液中充分反应后气体没有剩余,则:
①NOx中x的取值范围为
②反应后溶液中n(
 ):n(
):n( )=
)=
您最近一年使用:0次
9 . 如图所示装置,开始时夹子处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了。则液体A和气体B的组合不可能是


| A.氢氧化钠溶液、二氧化硫 | B.水、氯化氢 |
| C.氢氧化钠溶液、一氧化氮 | D.水、二氧化氮 |
您最近一年使用:0次
10 . 硝酸是一种重要的化工原料。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出开始时发生反应的离子方程式_______ ;反应停止后,仍有铜剩余,加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是_______ (填字母)。
A.还原剂 B.氧化剂 C.酸化 D.提供热能
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。

①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了NO,因为集气瓶中无色气体的来源可能是_______ 。
②乙组实验的操作步骤是:
a.关闭活塞K1,打开活塞K2,将过量稀硝酸加入石灰石中。该操作的目的是_______ 。
b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是NO,应进行的操作是_______ ,观察到的现象是_______ 。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出开始时发生反应的离子方程式
A.还原剂 B.氧化剂 C.酸化 D.提供热能
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。

①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了NO,因为集气瓶中无色气体的来源可能是
②乙组实验的操作步骤是:
a.关闭活塞K1,打开活塞K2,将过量稀硝酸加入石灰石中。该操作的目的是
b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是NO,应进行的操作是
您最近一年使用:0次



