1 . ⅰ.某学习小组在实验室中利用下图装置制备 并进行其相关性质的探究。
并进行其相关性质的探究。
(1)装置C中的现象为___________ ;装置D中的现象为___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)装置E中___________ (填现象)可说明 具有还原性。
具有还原性。
(4)装置F中过量的NaOH溶液吸收尾气,发生反应的离子方程式为___________ 。
ⅱ.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略),已知在溶液中: (棕色),该反应可用于检验NO。
(棕色),该反应可用于检验NO。 ,目的是
,目的是___________ 。
(6)写出装置E中发生反应的离子方程式:___________ 。
(7)若观察到装置H中红色粉末变黑,则NO与Cu发生反应,同时生成一种单质,写出该反应的化学方程式:___________ 。
 并进行其相关性质的探究。
并进行其相关性质的探究。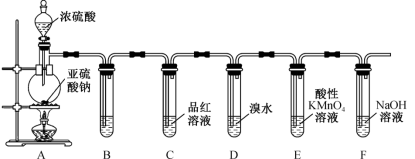
(1)装置C中的现象为
(2)装置A中发生反应的化学方程式为
(3)装置E中
 具有还原性。
具有还原性。(4)装置F中过量的NaOH溶液吸收尾气,发生反应的离子方程式为
ⅱ.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略),已知在溶液中:
 (棕色),该反应可用于检验NO。
(棕色),该反应可用于检验NO。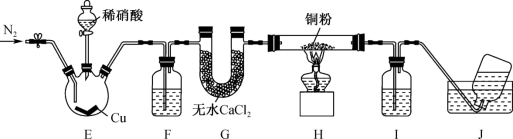
 ,目的是
,目的是(6)写出装置E中发生反应的离子方程式:
(7)若观察到装置H中红色粉末变黑,则NO与Cu发生反应,同时生成一种单质,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
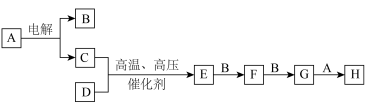
2 . 某些无机物的转化关系(部分反应物和生成物未列出)如图。已知化合物A为常见液体,气体E能使湿润的红色石蕊试纸变蓝。_____________ (填标号)。
a. b.
b.
(2)B、D在常温下难以发生反应,其主要原因为____________ 。
(3)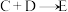 对人类的意义为
对人类的意义为_________________ (任写一点即可)。
(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:______________ ;试推测过量的E与氯气反应的现象:_____________ 。
(5)用 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:_________________ ,该反应中氧化产物与还原产物的物质的量之比为______________ 。
(6)常温常压下(气体摩尔体积为 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为______________  ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为_____________  (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
a.
 b.
b.
(2)B、D在常温下难以发生反应,其主要原因为
(3)
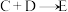 对人类的意义为
对人类的意义为(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:
(5)用
 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:(6)常温常压下(气体摩尔体积为
 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为 ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为 (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
您最近一年使用:0次
2024-05-03更新
|
70次组卷
|
3卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
3 . 到目前为止,我们学习了 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等气体。
等气体。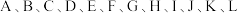 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:
①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和 ;
;
⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)写出A与B反应的化学方程式______ 。
(2)写出E和F反应的化学方程式______ 。
(3)写出G在足量F中燃烧的方程式______ 。
(4)④中发生反应的化学方程式为______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等气体。
等气体。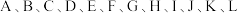 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和
 ;
;⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)写出A与B反应的化学方程式
(2)写出E和F反应的化学方程式
(3)写出G在足量F中燃烧的方程式
(4)④中发生反应的化学方程式为
您最近一年使用:0次
4 . 过多的NOx排放,往往会产生污染。某研究性小组探究 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
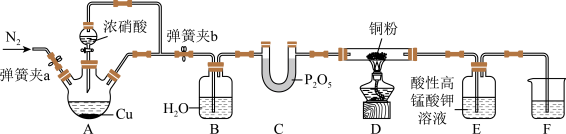
已知: 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。
(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:将F中的长导管插入液面以下→_______→_______→_______→_______→_______ (操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)装置B的作用_______ 。
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式_______ 。
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为_______ ;
(5)实验前和实验结束时,都需通一段时间的 ,目的分别是
,目的分别是_______ 、_______ 。
(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行 的是_______。
 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
已知:
 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:将F中的长导管插入液面以下→_______→_______→_______→_______→____
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)装置B的作用
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为
(5)实验前和实验结束时,都需通一段时间的
 ,目的分别是
,目的分别是(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中
| A.加热该绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
您最近一年使用:0次
名校
解题方法
5 . 某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。回答下列问题:
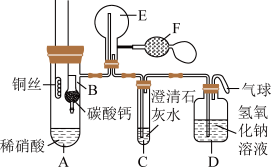
(1)实验中,先将装置B下移,使碳酸钙与稀硝酸接触,装置C中产生白色沉淀时,立刻将装置B上提。
①进行此操作的目的是_______
②装置C中产生的白色沉淀的化学式为_______
③装置D的作用是_______
④写出碳酸钙与稀硝酸反应的离子方程式:_______
(2)将装置A中铜丝放入稀硝酸中,给装置A微微加热,装置A中产生无色气体
①写出发生反应的化学方程式:_______
②用装置F向装置E中鼓入空气后出现红棕色,用化学方程式解释其原因是_______

(1)实验中,先将装置B下移,使碳酸钙与稀硝酸接触,装置C中产生白色沉淀时,立刻将装置B上提。
①进行此操作的目的是
②装置C中产生的白色沉淀的化学式为
③装置D的作用是
④写出碳酸钙与稀硝酸反应的离子方程式:
(2)将装置A中铜丝放入稀硝酸中,给装置A微微加热,装置A中产生无色气体
①写出发生反应的化学方程式:
②用装置F向装置E中鼓入空气后出现红棕色,用化学方程式解释其原因是
您最近一年使用:0次
6 . 某学习小组用氨催化氧化法(已知: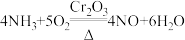 )在实验室模拟制硝酸,设计如图2所示装置。
)在实验室模拟制硝酸,设计如图2所示装置。
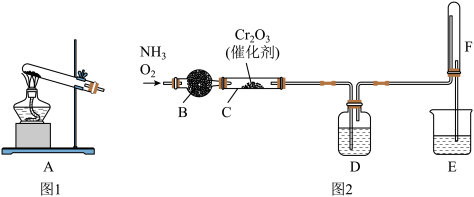
(1)写出实验室以图1装置A作发生装置制备氨气的化学方程式_______ 。
(2)仪器B的名称是_______ 。
(3)按图2所示连接好装置,首先_______ ,接着装好药品,按一定比例通入氧气、氨气,在催化剂、加热条件下反应。
(4)若没有装置D,可以观察到F中有白烟生成,则白烟成分是_______ (写化学式)。装置D盛放的试剂是_______ (写名称)。
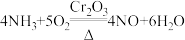 )在实验室模拟制硝酸,设计如图2所示装置。
)在实验室模拟制硝酸,设计如图2所示装置。
(1)写出实验室以图1装置A作发生装置制备氨气的化学方程式
(2)仪器B的名称是
(3)按图2所示连接好装置,首先
(4)若没有装置D,可以观察到F中有白烟生成,则白烟成分是
您最近一年使用:0次
名校
7 . 某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。已知在溶液中:FeSO4+NO⇌Fe(NO)]SO4(棕色),该反应可用于检验NO。
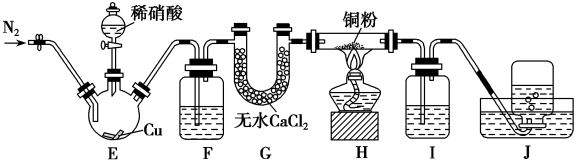
(1)实验开始前,向装置中通入一段时间的N2,目的是_______ 。
(2)盛装Cu片的仪器名称叫_______ ,请写出装置E中反应的离子方程式_______ 。
(3)装置F中盛放的是水,作用是_______ ;装置Ⅰ中盛放的试剂是_______ ,作用是_______ 。
(4)若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应,同时生成一种单质,请写出该反应的化学方程式:_______ 。

(1)实验开始前,向装置中通入一段时间的N2,目的是
(2)盛装Cu片的仪器名称叫
(3)装置F中盛放的是水,作用是
(4)若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应,同时生成一种单质,请写出该反应的化学方程式:
您最近一年使用:0次
2021-07-02更新
|
1353次组卷
|
6卷引用:吉林省长春外国语学校2020-2021学年高二下学期期末考试化学试题
8 . 为模拟二氧化氮溶于水生成硝酸,现进行如下实验:
实验I:制备并收集一试管二氧化氮
(1)某同学用图1所示装置制备并收集一试管二氧化氮,该装置的缺点是___________ 。(只填一个缺点即可)
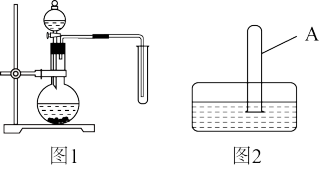
实验II:尽可能多地使试管中的二氧化氮被水吸收
(2)将充满二氧化氮的试管A倒放在盛有水的水槽中(如图2),并轻轻晃动试管,观察到的现象是___________ ,反应的化学方程式是___________ 。
(3)在该装置的基础上,请你设计实验,要求尽可能多地使试管中的二氧化氮被水吸收,实验操作是___________ 。
实验I:制备并收集一试管二氧化氮
(1)某同学用图1所示装置制备并收集一试管二氧化氮,该装置的缺点是

实验II:尽可能多地使试管中的二氧化氮被水吸收
(2)将充满二氧化氮的试管A倒放在盛有水的水槽中(如图2),并轻轻晃动试管,观察到的现象是
(3)在该装置的基础上,请你设计实验,要求尽可能多地使试管中的二氧化氮被水吸收,实验操作是
您最近一年使用:0次
9 . 如图表示A、B、C、D、E五种含氮物质相互转化的关系。其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式。
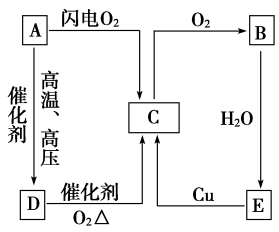
(1)写出各物质的化学式:A_______ ,B_______ ,C_______ ,D_______ ,E_______ 。
(2)写出各步反应的化学方程式。
①A→C_______ 。
②D→C_______ 。
③B→E_______ 。
④C→B_______ 。

(1)写出各物质的化学式:A
(2)写出各步反应的化学方程式。
①A→C
②D→C
③B→E
④C→B
您最近一年使用:0次
2021-03-03更新
|
519次组卷
|
3卷引用:吉林省延边朝鲜族自治州汪清县第六中学2020-2021学年高一下学期3月月考化学试题
名校
10 . 某研究小组设计如图所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
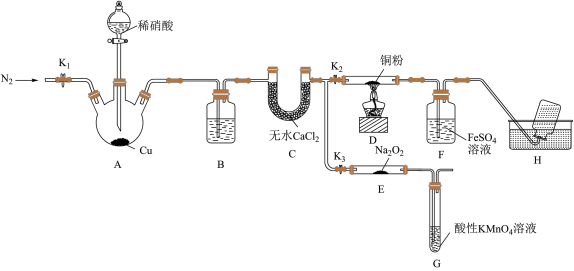
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是________ 。
(2)装置B中盛放的试剂为水,其作用是________ 。
(3)装置F中的实验现象为______ 。装置H中收集的气体为N2和_______ (填化学式)。
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是________ 。
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和_____ (填化学式)。
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①判断滴定终点的方法________ 。
②样品中NaNO2的质量分数为___________ (用含有a、b的代数式表示)。
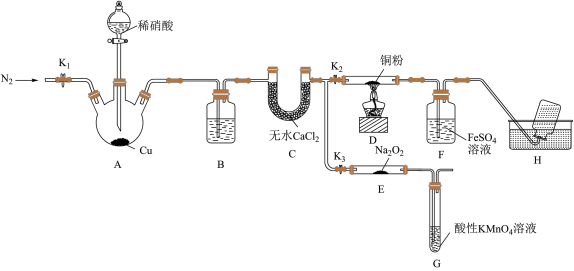
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO
 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO
 Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO
 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。①判断滴定终点的方法
②样品中NaNO2的质量分数为
您最近一年使用:0次
2020-11-04更新
|
690次组卷
|
5卷引用:吉林省白城市洮南一中2021届高三上学期第三次月考化学试题



