1 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。_______ 。
(2)写出E的一种用途是_______ ,其与氢氧化钠溶液反应的离子方程式为_______ 。
(3)反应③的化学方程式是_______ 。
(4)反应④中B物质过量的离子方程式是_______ 。

(2)写出E的一种用途是
(3)反应③的化学方程式是
(4)反应④中B物质过量的离子方程式是
您最近一年使用:0次
名校
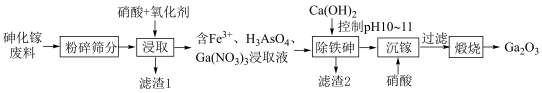
2 . 氧化镓(Ga2O3)可用作有机及无机合成的催化剂及制备高纯镓的原料。以砷化镓废料(主要成分为 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如图所示:
的工艺流程如图所示:
已知:镓(Ga)、铝(Al)是同主族相邻元素,Ga元素在溶液中存在的形式有 、
、 、
、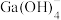 。
。
回答下列问题:
(1)滤渣1为 ,工业上以石英砂(主要成分为
,工业上以石英砂(主要成分为 )、
)、___________ (填化学式)为原料生产普通玻璃。
(2)“浸取”时,不是只用硝酸,而是还用氧化剂 或空气(提供
或空气(提供 ),其优点是不产生污染环境的
),其优点是不产生污染环境的 ,写出
,写出 、空气(O2)和稀硝酸反应的化学方程式:
、空气(O2)和稀硝酸反应的化学方程式:___________ 。
(3)硝酸用量一定时,在相同的浸取时间内,氧化剂不同时,镓浸取率随时间的变化如图所示。用空气作氧化剂的浸取率明显低于过氧化氢,其原因是___________ 。
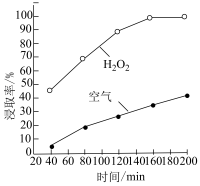
(4)“浸取”时,温度保持在60℃,其原因是___________ 。
(5)滤渣2是___________ [写化学式,不考虑 和
和 ]。
]。
(6)写出“沉镓”时反应的离子方程式:___________ 。不同 时,镓的沉淀率如下表所示。
时,镓的沉淀率如下表所示。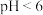 时,镓的沉淀率显著降低的原因是
时,镓的沉淀率显著降低的原因是___________ 。
 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如图所示:
的工艺流程如图所示:
已知:镓(Ga)、铝(Al)是同主族相邻元素,Ga元素在溶液中存在的形式有
 、
、 、
、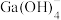 。
。回答下列问题:
(1)滤渣1为
 ,工业上以石英砂(主要成分为
,工业上以石英砂(主要成分为 )、
)、(2)“浸取”时,不是只用硝酸,而是还用氧化剂
 或空气(提供
或空气(提供 ),其优点是不产生污染环境的
),其优点是不产生污染环境的 ,写出
,写出 、空气(O2)和稀硝酸反应的化学方程式:
、空气(O2)和稀硝酸反应的化学方程式:(3)硝酸用量一定时,在相同的浸取时间内,氧化剂不同时,镓浸取率随时间的变化如图所示。用空气作氧化剂的浸取率明显低于过氧化氢,其原因是

(4)“浸取”时,温度保持在60℃,其原因是
(5)滤渣2是
 和
和 ]。
]。(6)写出“沉镓”时反应的离子方程式:
 时,镓的沉淀率如下表所示。
时,镓的沉淀率如下表所示。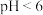 时,镓的沉淀率显著降低的原因是
时,镓的沉淀率显著降低的原因是 | 4 | 5 | 6 | 7 | 8 | 9 |
| 沉淀率% | 23.7 | 79.3 | 98.7 | 95.4 | 46.3 | 19.5 |
您最近一年使用:0次
2024-01-02更新
|
289次组卷
|
4卷引用:河南省部分名校2023-2024学年高三上学期11月期中化学试题
名校
解题方法
3 . 铜系金属元素铈可作催化剂、电弧电极、特种玻璃等。铈的合金耐高热,可以用来制造喷气推进器零件。实验室利用废旧的液晶显示器设计实验回收铈的流程如图所示(已知废旧显示器除了含有二氧化硅外,还有CeO2 、Fe2O3物质,其中铈有+3、+4两种价态,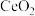 具有强氧化性,与常见的无机酸不反应):
具有强氧化性,与常见的无机酸不反应):

(1)铜在周期表的___________ 区(填s、p、d、ds、f)铜的基态原子的价电子排布式为___________ 。
(2)步骤Ⅱ的离子方程式是___________ ;为了加快步骤Ⅱ的反应速率,有人提出在较高温度下进行,你认为是否合适,___________ (填是或否)解释理由___________ 。
(3)固体B的主要成分化学式是___________ ,说出该物质两个主要用途___________ 。
(4)直接加热CeCl3溶液蒸干得不到CeCl3固体,说明理由并写出有关离子方程式________ 。
(5)步骤IV的化学方程式是___________ 。
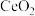 具有强氧化性,与常见的无机酸不反应):
具有强氧化性,与常见的无机酸不反应):
(1)铜在周期表的
(2)步骤Ⅱ的离子方程式是
(3)固体B的主要成分化学式是
(4)直接加热CeCl3溶液蒸干得不到CeCl3固体,说明理由并写出有关离子方程式
(5)步骤IV的化学方程式是
您最近一年使用:0次
4 . 为探究固体X(仅含两种常见短周期元素)的组成和性质,设计并完成如下实验:

已知:气体A是一种纯净物,标准状况下 的A质量为
的A质量为 ;固体B是光导纤维的主要成分。请回答:
;固体B是光导纤维的主要成分。请回答:
(1)气体A的摩尔质量为_______  ;A分子的电子式
;A分子的电子式_______ 。
(2)B的化学式_______ ;D的化学式_______ 。
(3)固体X与稀硫酸反应的离子方程式是_______ 。
(4)已知 与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为
与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为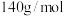 )和
)和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。

已知:气体A是一种纯净物,标准状况下
 的A质量为
的A质量为 ;固体B是光导纤维的主要成分。请回答:
;固体B是光导纤维的主要成分。请回答:(1)气体A的摩尔质量为
 ;A分子的电子式
;A分子的电子式(2)B的化学式
(3)固体X与稀硫酸反应的离子方程式是
(4)已知
 与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为
与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为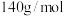 )和
)和 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
5 . LiFePO4是新一代理想型正极材料,某科研小组设计由钛磁铁矿(主要成分为FeTiO3,还含有少量MgO和SiO2等杂质)制备LiFePO4的工艺流程图如下:

已知25℃时相关金属离子[co(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
(1)列举滤渣A的一种用途_____ ,请写出滤渣A与NaOH溶液反应的离子方程式_____ 。
(2)为了加快钛磁铁矿酸浸速率,可采取的措施有_______ (任答两条即可)。
(3)写出氧化过程发生的离子方程式:_______ ,氧化需要控制在适当的温度下进行,温度不宜过高的原因是_______ 。
(4)写出“高温煅烧”制备LiFePO4的化学方程式:_______ 。
(5)新一代LiFePO4电池是一种高能量密度、电性能优良的新型电池,其工作原理如图所示,电池反应:LixC6+Li1-xFePO4 LiFePO4+6C。
LiFePO4+6C。

①放电时,正极反应式:_______ 。
②充电时,LixC6电极增重14g时,电路中转移电子数目为_______ 。

已知25℃时相关金属离子[co(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Mg2+ |
| 开始沉淀的pH | 6.3 | 1.5 | 8.9 |
| 沉淀完全的pH | 8.3 | 3.2 | 10.9 |
(1)列举滤渣A的一种用途
(2)为了加快钛磁铁矿酸浸速率,可采取的措施有
(3)写出氧化过程发生的离子方程式:
(4)写出“高温煅烧”制备LiFePO4的化学方程式:
(5)新一代LiFePO4电池是一种高能量密度、电性能优良的新型电池,其工作原理如图所示,电池反应:LixC6+Li1-xFePO4
 LiFePO4+6C。
LiFePO4+6C。
①放电时,正极反应式:
②充电时,LixC6电极增重14g时,电路中转移电子数目为
您最近一年使用:0次
6 . A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,A是单质,B是A的氧化物。它们有如图反应关系:
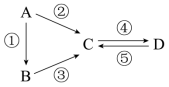
(1)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成_______ ,反应①②③④⑤中,属于氧化还原反应的有_______ (填序号),写出D转化为C的离子方程_______ 。
(2)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为_______ ;若C、D组成元素相同,则C转化为D的离子方程式为_______ ,在D中滴入氢氧化钠溶液,一段时间内观察到的现象是_______ 。

(1)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成
(2)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为
您最近一年使用:0次
7 . 某矿石可能由 、
、 、
、 中的一种或几种组成,某兴趣小组欲探究其组成,设计探究过程如图所示。
中的一种或几种组成,某兴趣小组欲探究其组成,设计探究过程如图所示。

已知:① 可以与过量的NaOH溶液反应生成
可以与过量的NaOH溶液反应生成 ,
, 可以与
可以与 反应生成
反应生成 沉淀。
沉淀。
② 是一种酸性氧化物,
是一种酸性氧化物, 难溶于水。
难溶于水。
(1)下列有关 说法正确的是
说法正确的是_______ 。
A.用石英和焦炭制取粗硅:
B.造月球探测器中的瞄准镜时使用的光导纤维,其主要成分是
C.月球探测器使用的硅太阳能电池板,其主要成分是
D. 、石灰石和纯碱是制备玻璃的原料
、石灰石和纯碱是制备玻璃的原料
E.氢氟酸雕刻玻璃发生的离子反应:
(2)写出反应④的离子方程式_______ 。
(3)反应③没有沉淀生成,说明矿石中不存在_______ (填化学式),为了达到此目的,_______ (填“能”或“否”)将反应②中NaOH溶液改用 溶液,说明理由
溶液,说明理由_______ 。
(4)该矿石和 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的 混合循环通入反应池中,目的是
混合循环通入反应池中,目的是_______ 。
 、
、 、
、 中的一种或几种组成,某兴趣小组欲探究其组成,设计探究过程如图所示。
中的一种或几种组成,某兴趣小组欲探究其组成,设计探究过程如图所示。
已知:①
 可以与过量的NaOH溶液反应生成
可以与过量的NaOH溶液反应生成 ,
, 可以与
可以与 反应生成
反应生成 沉淀。
沉淀。②
 是一种酸性氧化物,
是一种酸性氧化物, 难溶于水。
难溶于水。(1)下列有关
 说法正确的是
说法正确的是A.用石英和焦炭制取粗硅:

B.造月球探测器中的瞄准镜时使用的光导纤维,其主要成分是

C.月球探测器使用的硅太阳能电池板,其主要成分是

D.
 、石灰石和纯碱是制备玻璃的原料
、石灰石和纯碱是制备玻璃的原料E.氢氟酸雕刻玻璃发生的离子反应:

(2)写出反应④的离子方程式
(3)反应③没有沉淀生成,说明矿石中不存在
 溶液,说明理由
溶液,说明理由(4)该矿石和
 溶液反应的离子方程式为
溶液反应的离子方程式为(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的
 混合循环通入反应池中,目的是
混合循环通入反应池中,目的是
您最近一年使用:0次
2022-07-03更新
|
240次组卷
|
2卷引用:湖南省邵阳邵东市第四中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
8 . 下图是元素周期表的一部分,表中①~⑦分别代表某种元素。回答下列问题:
(1)表中有_______ 种金属元素;⑦元素在周期表中的位置是第_______ 周期第_______ 族。
(2)①的最高价氧化物的化学式为_______ ;
②与氢元素形成的最简单氢化物的电子式为_______ 。
(3)光导纤维是一种高性能的现代通讯材料,这种材料含有①~⑦元素中的_______ 元素(填元素符号)。
(4)①~⑦元素中,最高价氧化物对应的水化物是两性氢氧化物的元素是_______ (填元素符号),写出该两性氢氧化物与NaOH溶液反应的离子方程式_______ 。
| ① | ② | ||||||||||||||||
| ③ | ④ | ⑤ | |||||||||||||||
| ⑥ | ⑦ |
(2)①的最高价氧化物的化学式为
②与氢元素形成的最简单氢化物的电子式为
(3)光导纤维是一种高性能的现代通讯材料,这种材料含有①~⑦元素中的
(4)①~⑦元素中,最高价氧化物对应的水化物是两性氢氧化物的元素是
您最近一年使用:0次
名校
解题方法
9 . 氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。不溶于酸(氢氟酸除外)。高温下氧气及水蒸气能明显腐蚀氮化硅。一种用工业硅(含少量铁、铜的单质及氧化物)和 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下: 净化时,铜屑的作用是
净化时,铜屑的作用是_______ ;硅胶的作用是_______ 。
(2) 可能是
可能是_______ (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)如何说明氮化硅产品已用水洗干净?_______ 。
(4)推测氮化硅可能有哪些用途:_______ (填字母)。
a. 制作切削刀具 b. 制作坩埚 c. 制作耐高温轴承
(5)工业上还可以采用化学气相沉积法,在 的环境中,使
的环境中,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为_______ 。
 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下:
 净化时,铜屑的作用是
净化时,铜屑的作用是(2)
 可能是
可能是(3)如何说明氮化硅产品已用水洗干净?
(4)推测氮化硅可能有哪些用途:
a. 制作切削刀具 b. 制作坩埚 c. 制作耐高温轴承
(5)工业上还可以采用化学气相沉积法,在
 的环境中,使
的环境中,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为
您最近一年使用:0次
2022-03-18更新
|
296次组卷
|
3卷引用:湖南省常德市石门县第一中学2022-2023学年高一下学期期中考试化学试题
10 . 铜系金属元素铈可作催化剂、电弧电极、特种玻璃等。铈的合金耐高热,可以用来制造喷气推进器零件。实验室利用废旧的液晶显示器设计实验回收铈的流程如图所示(已知废旧显示器除了含有二氧化硅外,还有 、
、 等物质,其中铺有
等物质,其中铺有 、
、 两种价态,
两种价态, 具有强氧化性,与常见的无机酸不反应):
具有强氧化性,与常见的无机酸不反应):

(1)步骤Ⅰ和步骤Ⅱ进行的实验操作是_______ 。
(2)步骤Ⅱ的离子方程式是_______ ;为了加快步骤Ⅱ的反应速率,有人提出在较高温度下进行,你认为是否合适,解释理由_______ 。
(3)固体B的主要成分化学式是_______ ,说出该物质两个主要用途_______ 。
(4)可否省掉真空加热这一步,对 溶液直接加热蒸干而得到
溶液直接加热蒸干而得到 ,请说明理由
,请说明理由_______ 。
(5)步骤IV的化学方程式是_______ 。
 、
、 等物质,其中铺有
等物质,其中铺有 、
、 两种价态,
两种价态, 具有强氧化性,与常见的无机酸不反应):
具有强氧化性,与常见的无机酸不反应):
(1)步骤Ⅰ和步骤Ⅱ进行的实验操作是
(2)步骤Ⅱ的离子方程式是
(3)固体B的主要成分化学式是
(4)可否省掉真空加热这一步,对
 溶液直接加热蒸干而得到
溶液直接加热蒸干而得到 ,请说明理由
,请说明理由(5)步骤IV的化学方程式是
您最近一年使用:0次



