名校
解题方法
1 . 某小组同学依据性质差异,采用比较的方法设计实验鉴别 和
和 。
。
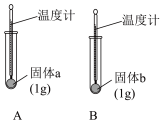
(1)实验Ⅰ中,分别向两支试管中滴加几滴水, 中温度计示数略有降低,
中温度计示数略有降低, 中温度计示数升高。说明固体
中温度计示数升高。说明固体 溶解于水的过程中
溶解于水的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为 。
。
(2)实验Ⅱ中,向试管 和
和 中分别加入
中分别加入 水,充分振荡,试管
水,充分振荡,试管 中固体有剩余,试管D中固体完全溶解。
中固体有剩余,试管D中固体完全溶解。
①判断固体 为
为_______ 。
②分别向两支试管中滴加2滴酚酞,_______ 试管中红色较深。
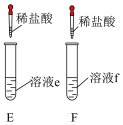
(3)实验Ⅲ中,分别向溶液 和溶液
和溶液 中逐滴加入稀盐酸,
中逐滴加入稀盐酸, 中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。用离子方程式解释E中开始无气泡产生的原因
中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。用离子方程式解释E中开始无气泡产生的原因_______ 。
(4)请你再设计一个鉴别固体 和
和 的实验方案
的实验方案_______ 。
(5)写出 在水中电离的方程式
在水中电离的方程式_______ 。
 和
和 。
。| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
 |  |  |
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,
 中温度计示数略有降低,
中温度计示数略有降低, 中温度计示数升高。说明固体
中温度计示数升高。说明固体 溶解于水的过程中
溶解于水的过程中 。
。(2)实验Ⅱ中,向试管
 和
和 中分别加入
中分别加入 水,充分振荡,试管
水,充分振荡,试管 中固体有剩余,试管D中固体完全溶解。
中固体有剩余,试管D中固体完全溶解。①判断固体
 为
为②分别向两支试管中滴加2滴酚酞,
(3)实验Ⅲ中,分别向溶液
 和溶液
和溶液 中逐滴加入稀盐酸,
中逐滴加入稀盐酸, 中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。用离子方程式解释E中开始无气泡产生的原因
中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。用离子方程式解释E中开始无气泡产生的原因(4)请你再设计一个鉴别固体
 和
和 的实验方案
的实验方案(5)写出
 在水中电离的方程式
在水中电离的方程式
您最近一年使用:0次
名校
2 . 下列实验过程不能达到实验目的的是
| 实验目的 | 实验过程 | |
| A | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| B | 配制100mL1.0mol/L CuSO4溶液 | 将25.0gCuSO4·5H2O配成100mL溶液 |
| C | 验证X溶液中是否含有Fe2+ | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,观察溶液颜色变化 |
| D | 鉴别碳酸钠和碳酸氢钠溶液 | 向溶液中分别逐滴滴加等浓度的稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . (Ⅰ)某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为Na2CO3。
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,_______ 试管中红色较浅。
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因_______ 。
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为_______ mol。
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是_______
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和_______ (写出化学式)。
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是_______ (写化学式)。
实验I | 实验Ⅱ | 实验Ⅲ |
 |  |  |
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。分别向两支试管中滴加2滴酚酞,
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因
(Ⅱ)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(4)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为
(5)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①配料中属于两性氧化物的是
②“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:2Na2SiO3+2NaAlO2+2H2O= Na2Al2Si2O8↓+4NaOH ,“赤泥”的主要成分为Na2Al2Si2O8和
③ “酸化”时,通入过量CO2与之反应,生成滤液的主要成分是
您最近一年使用:0次
名校
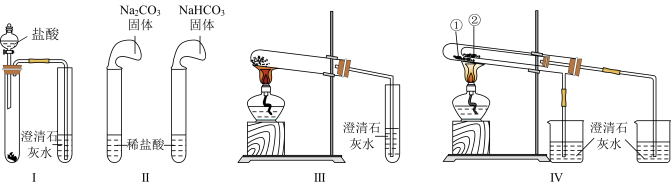
4 . 某课外小组为了鉴别 和
和 两种白色固体,用不同的方法做了以下四组实验,如图Ⅰ~Ⅳ所示。下列说法不正确的是
两种白色固体,用不同的方法做了以下四组实验,如图Ⅰ~Ⅳ所示。下列说法不正确的是
 和
和 两种白色固体,用不同的方法做了以下四组实验,如图Ⅰ~Ⅳ所示。下列说法不正确的是
两种白色固体,用不同的方法做了以下四组实验,如图Ⅰ~Ⅳ所示。下列说法不正确的是
| A.将两种固体分别放入装置Ⅰ中,均能与盐酸反应,并产生能使澄清石灰水变浑浊的气体 |
B.若装置Ⅱ中两种固体质量相等且稀盐酸足量时,气球鼓起较小的是 |
C.装置Ⅲ和Ⅳ均能鉴别 和 和 ,Ⅳ可同时进行两个对比实验 ,Ⅳ可同时进行两个对比实验 |
| D.装置Ⅳ试管①②中的药品可以互换 |
您最近一年使用:0次
名校
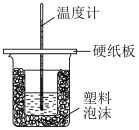
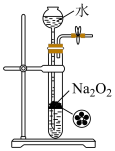
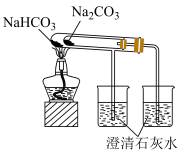
5 . 下列实验中的仪器、药品选择正确且能达到实验目的的是
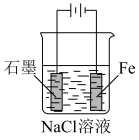 |  |  |  |
| 甲 | 乙 | 丙 | 丁 |
| A.图甲:防止铁被腐蚀 |
| B.图乙:测定中和热 |
| C.图丙:制备氧气,并能随时控制反应的发生和停止 |
D.图丁:比较 和 和 的热稳定性 的热稳定性 |
您最近一年使用:0次
名校
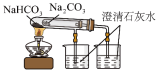
6 . 下列实验装置及实验结果合理的是
 |  |  |  |
| 图1 | 图2 | 图3 | 图 |
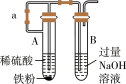
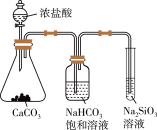
A.实验室用图1比较 与 与 的热稳定性 的热稳定性 |
| B.实验室用图2所示装置测定氯水的pH |
C.实验室用图3所示装置制备少量 ,先打开止水夹a,一段时间后再关闭a ,先打开止水夹a,一段时间后再关闭a |
| D.实验室用图4所示装置证明非金属性强弱:Cl>C>Si |
您最近一年使用:0次
名校
7 . 化学是以实验为基础的科学。下列实验操作能达到实验预期目的的是


| A.图甲制备Fe(OH)2 |
| B.图乙分离Fe(OH)3胶体和NaCl溶液 |
| C.图丙验证NaHCO3和Na2CO3的热稳定性,x中放的物质是Na2CO3 |
| D.图丁证明Na能与水反应,且Na的密度比煤油大 |
您最近一年使用:0次
名校
解题方法
8 . 某校化学课外小组为了测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数,用不同的方法开展了实验,具体情况如图所示。
测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数
方案一、用沉淀分析法,按如下图所示的实验流程进行实验:

(1)①操作Ⅰ、Ⅱ涉及的实验名称依次是_________ 、洗涤、干燥、称量。
②该方案中涉及有关反应的离子方程式为_____________ 。
③该试样中碳酸钠的质量分数的计算式为_______________ 。
方案二、按如下图所示装置及主要流程进行实验:
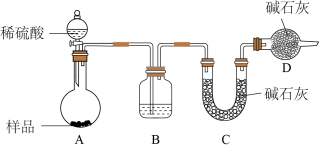

(2)装置A装稀硫酸的仪器是_______ ,装置B盛放的物质是_________ ,能否用盐酸代替稀硫酸进行实验(填”能"或“不能")。
(3)在装置C中装碱石灰来吸收净化后的气体。在滴加稀硫酸时应缓慢滴加,若快速滴加,则会导致测定结果______ (填“偏大”、 “偏小”或“不变”)。
(4)有同学认为,为了减少实验误差,在反应前和反应后都要通入N2,反应后通入N2的目的是__________ 。
测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数
方案一、用沉淀分析法,按如下图所示的实验流程进行实验:

(1)①操作Ⅰ、Ⅱ涉及的实验名称依次是
②该方案中涉及有关反应的离子方程式为
③该试样中碳酸钠的质量分数的计算式为
方案二、按如下图所示装置及主要流程进行实验:
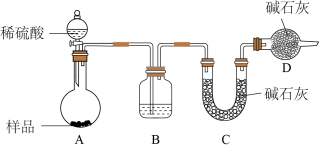

(2)装置A装稀硫酸的仪器是
(3)在装置C中装碱石灰来吸收净化后的气体。在滴加稀硫酸时应缓慢滴加,若快速滴加,则会导致测定结果
(4)有同学认为,为了减少实验误差,在反应前和反应后都要通入N2,反应后通入N2的目的是
您最近一年使用:0次
名校
9 . 下列对于某些物质的检验及结论正确的是
A.向溶液中加入稀盐酸产生气体,气体能使澄清石灰水变浑浊,原溶液中一定有 |
| B.向溶液中加入硝酸银溶液产生白色沉淀,原溶液中一定有Cl- |
| C.用洁净的铁丝蘸取某物质,在酒精灯外焰上灼烧,火焰为黄色则该物质一定是钠盐 |
| D.用CaCl2鉴别Na2CO3、NaHCO3溶液,有白色沉淀生成的是Na2CO3溶液 |
您最近一年使用:0次
名校
10 . 下列实验装置能达到实验目的的是
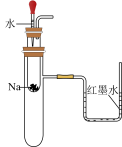
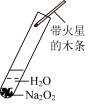
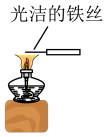
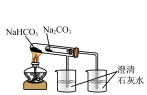
①验证 和水反应是否为放热反应 和水反应是否为放热反应 | ②检验Na2O2与 反应有 反应有 生成 生成 | ③观察 的焰色试验 的焰色试验 | ④比较 、 、 的稳定性 的稳定性 |
|
|
|
|
| A.①② | B.①③ | C.②③ | D.③④ |
您最近一年使用:0次
2024-01-20更新
|
155次组卷
|
6卷引用:江西省南昌市第二中学2023-2024学年高一上学期12月月考考试化学试题