1 . 某同学用不同长度的光亮镁条分别与4.0mL5%的稀盐酸反应,实验现象如下:
[提出问题]灰白色沉淀是什么?实验中为什么出现了灰白色沉淀?
[查阅资料]氢氧化镁难溶于水,Mg(OH)2 MgO+H2O。
MgO+H2O。
[猜想与假设]I.灰白色沉淀可能是析出的MgCl2
II.灰白色沉淀可能是生成的Mg(OH)2
[进行实验]
[解释与结论]
(1)试管A中,镁与稀盐酸反应的化学方程式为___ 。
(2)[猜想与假设]I不成立,其原因是___ 。
(3)根据上述实验能得出的结论是___ (填序号)。
A.灰白色固体不是氢氧化镁
B.镁条的用量偏多导致沉淀产生
C.灰白色固体受热产生碱性物质
(4)经过进一步实验测定,灰白色沉淀中含有镁、氯、氢、氧四种元素。实验3中产生灰白色沉淀是因为镁与反应生成的___ 。
| 试管 | A | B | C | D |
| 镁条长度 | 1cm | 2cm | 3cm | 4cm |
| 实验现象 | 产生大量气泡,镁条溶解。 | |||
| 无沉淀 | 少量灰白色沉淀 | 多量灰白色沉淀 | 大量灰白色沉淀 | |
[查阅资料]氢氧化镁难溶于水,Mg(OH)2
 MgO+H2O。
MgO+H2O。[猜想与假设]I.灰白色沉淀可能是析出的MgCl2
II.灰白色沉淀可能是生成的Mg(OH)2
[进行实验]
| 实验 | 实验操作 | 实验现象 |
| 1 | ①取一定量上述实验中灰白色沉淀放入试管中,然后加入5mL蒸馏水,振荡、静置; ②取等量氯化镁固体放入另一支试管中,加5mL蒸馏水,振荡、静置。 | ①中固体量未减少 ②中固体全部溶解得到澄清溶液 |
| 2 | 取上述实验中灰白色沉淀,用蒸馏水洗涤、室温晾干,放入试管中进行加热,试管口用浸有紫色石蕊试液的滤纸检验。 | 滤纸变红 |
| 3 | ①在1支试管中放入一小段光亮的镁条,5mL蒸馏水; ②向上述试管中加入几滴饱和的氯化镁溶液。 | ①中无明显现象。 ②中镁条表面立即产生细小气泡并不断溶解,一段时间后镁条全部溶解,试管中生成大量灰白色沉淀。 |
(1)试管A中,镁与稀盐酸反应的化学方程式为
(2)[猜想与假设]I不成立,其原因是
(3)根据上述实验能得出的结论是
A.灰白色固体不是氢氧化镁
B.镁条的用量偏多导致沉淀产生
C.灰白色固体受热产生碱性物质
(4)经过进一步实验测定,灰白色沉淀中含有镁、氯、氢、氧四种元素。实验3中产生灰白色沉淀是因为镁与反应生成的
您最近一年使用:0次
名校
2 . 下列物质的性质与应用关系的描述不正确的是
| A.氧化镁的熔点高,是优质的耐高温材料 |
| B.钠具有强还原性,可用于制取钛、锆等金属 |
| C.氯气有强氧化性,可用氯气漂白干燥有色布条 |
| D.NaHCO3可与盐酸反应,小苏打可用于治疗胃病 |
您最近一年使用:0次
名校
解题方法
3 . 氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为MgCO3,还含有少量SiO2、Al2O3等杂质)设计制备氧化镁的流程如图:
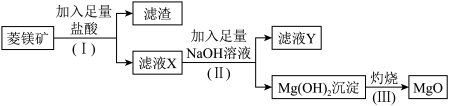
(1)步骤(Ⅰ)中分离操作的名称是___________ ;
(2)步骤(I)分离出的滤渣中主要含有_______ ,它属于______ (填“酸性”或“碱性”)氧化物;
(3)滤液Y中的阴离子除了含OH-、Cl-外还有___________ ;
(4)写出步骤(II)生成Mg(OH)2的离子方程式:_________ 。

(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(I)分离出的滤渣中主要含有
(3)滤液Y中的阴离子除了含OH-、Cl-外还有
(4)写出步骤(II)生成Mg(OH)2的离子方程式:
您最近一年使用:0次
2020-11-23更新
|
231次组卷
|
4卷引用:福建省南安市第六中学2021-2022学年高一下学期4月阶段考试化学试题
4 . 下列有关物质的性质与用途具有对应关系的是
A.浓硫酸具有脱水性,可用于干燥 |
| B.维生素C具有还原性,可用于鲜榨的果汁保鲜 |
| C.氧化镁难溶于水,可用作阻燃材料 |
| D.次氯酸钠呈碱性,可用作染料等有机色素的漂白剂 |
您最近一年使用:0次
名校
解题方法
5 . 下列物质的性质与应用关系的描述不正确的是
| A.氧化镁的熔点高,可用作耐高温材料 |
| B.金属钠具有还原性,可从CuSO4溶液中置换出铜 |
| C.过氧化钠有漂白性,可用于漂白纸浆及草帽等编织物 |
| D.碳酸钠溶液显碱性,其热溶液可除去物品表面的油污 |
您最近一年使用:0次
6 . 小强同学观看体操和举重比赛时,注意到运动员上场前都要在手上抹一些称为“镁粉”的白色粉末。小强和化学兴趣小组的同学一起探究“镁粉”的组成。
【提出猜想】①是金属镁的粉末;②是氧化镁;③是碳酸镁;④是氢氧化镁。大家一致认为猜想______ 是错误的,原因是______________________________ 。
【收集资料】氧化镁、碳酸镁和氢氧化镁都是白色粉末,三种物质几乎都不溶于水。其中,碳酸镁有很强的吸湿作用。
请你选取一种猜想,设计实验进行验证。你选的猜想是:________ ;设计实验:___________ 。
【提出猜想】①是金属镁的粉末;②是氧化镁;③是碳酸镁;④是氢氧化镁。大家一致认为猜想
【收集资料】氧化镁、碳酸镁和氢氧化镁都是白色粉末,三种物质几乎都不溶于水。其中,碳酸镁有很强的吸湿作用。
请你选取一种猜想,设计实验进行验证。你选的猜想是:
您最近一年使用:0次
名校
7 . 下列有关物质的性质与用途具有对应关系的是
| A.SO2具有氧化性,可用于漂白纸张 | B.明矾易溶于水,可用作净水剂 |
| C.金属钠具有还原性,可用于高压钠灯 | D.MgO熔点高,可用于制作耐火材料 |
您最近一年使用:0次
2021-09-24更新
|
706次组卷
|
3卷引用:江苏省昆山市周市高级中学2020-2021学年高一上学期第二次模块测试化学试题
8 . 卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
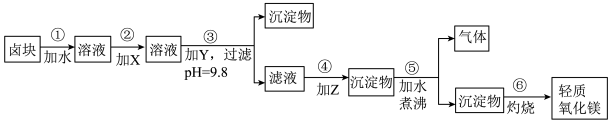
若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去
表2 原料价格表
(1)在步骤②中加入的试剂X,最佳的选择是____________ ,其作用是_________________ ;
(2)在步骤③中加入的试剂应是_______________________ ;之所以要控制pH=9.8,其目的是___________________________________________________________ 。
(3)在步骤④中加入的试剂Z应是________________ ;
(4)在步骤⑤中发生反应的化学方程式是_____________________________________________ 。

若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6﹡ |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格表
| 物质 | 价格/(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
(2)在步骤③中加入的试剂应是
(3)在步骤④中加入的试剂Z应是
(4)在步骤⑤中发生反应的化学方程式是
您最近一年使用:0次
解题方法
9 . 卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁(已知其中有一种中间产物是MgCO3)。
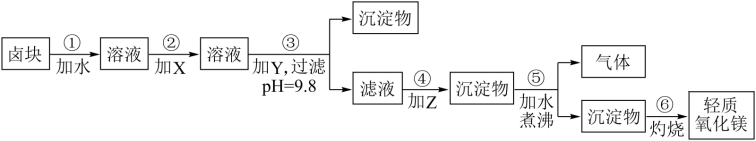
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
表2原料价格表
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)在步骤②中加入的试剂X,最佳的选择是______,其反应的离子方程式是 。
(2)在步骤③中如要控制pH=9.8,其目的是______;在步骤④中加入的试剂Z应是______;
(3)在步骤⑤中发生的化学方程式是______。

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2原料价格表
| 物质 | 价格/元・吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)在步骤②中加入的试剂X,最佳的选择是______,其反应的离子方程式是 。
(2)在步骤③中如要控制pH=9.8,其目的是______;在步骤④中加入的试剂Z应是______;
(3)在步骤⑤中发生的化学方程式是______。
您最近一年使用:0次
10 . 镁的化合物用途广泛,如 在医药上用作抗酸剂;
在医药上用作抗酸剂; 能快速吸收汗液、增加物体表面摩擦力,是体操比赛中常用的防滑剂,也可用作阻燃剂。
能快速吸收汗液、增加物体表面摩擦力,是体操比赛中常用的防滑剂,也可用作阻燃剂。
I.
(1)无机化合物根据其组成和性质可进行如下分类:
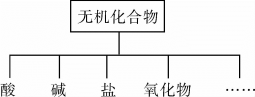
该分类方法属于___________ 分类法, 用作抗酸剂体现了它
用作抗酸剂体现了它___________ (填“酸性”、“碱性”或“两性”)氧化物的性质。
(2) 可用作阻燃剂的原因是
可用作阻燃剂的原因是___________ (用化学方程式表示)。
II.某学习小组拟用酸性 废液(主要成分是
废液(主要成分是 ,含
,含 、
、 等杂质)制取
等杂质)制取 、
、 和副产品
和副产品 ,部分流程如图所示。
,部分流程如图所示。

(3)为减少污染和防止引入其他杂质离子,氧化过程最好用___________ 代替新制氯水。
(4)滤渣的成分是___________ 。
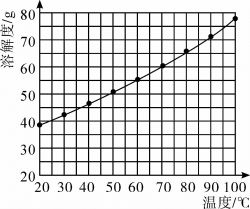
(5)已知 的溶解度如图所示,则操作3为
的溶解度如图所示,则操作3为___________ ,过滤、洗涤、干燥。
(6)所得 固体在
固体在___________ (填仪器名称)中灼烧可得 。
。
(7)该小组用上述方案制取 ,废液中
,废液中 的浓度为
的浓度为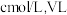 废液最终制得
废液最终制得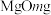 ,计算该过程的产率为
,计算该过程的产率为___________ (产率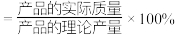 )。
)。
 在医药上用作抗酸剂;
在医药上用作抗酸剂; 能快速吸收汗液、增加物体表面摩擦力,是体操比赛中常用的防滑剂,也可用作阻燃剂。
能快速吸收汗液、增加物体表面摩擦力,是体操比赛中常用的防滑剂,也可用作阻燃剂。I.
(1)无机化合物根据其组成和性质可进行如下分类:

该分类方法属于
 用作抗酸剂体现了它
用作抗酸剂体现了它(2)
 可用作阻燃剂的原因是
可用作阻燃剂的原因是II.某学习小组拟用酸性
 废液(主要成分是
废液(主要成分是 ,含
,含 、
、 等杂质)制取
等杂质)制取 、
、 和副产品
和副产品 ,部分流程如图所示。
,部分流程如图所示。
(3)为减少污染和防止引入其他杂质离子,氧化过程最好用
(4)滤渣的成分是
(5)已知
 的溶解度如图所示,则操作3为
的溶解度如图所示,则操作3为
(6)所得
 固体在
固体在 。
。(7)该小组用上述方案制取
 ,废液中
,废液中 的浓度为
的浓度为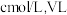 废液最终制得
废液最终制得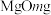 ,计算该过程的产率为
,计算该过程的产率为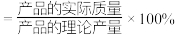 )。
)。
您最近一年使用:0次



