1 . 下列有关物质的应用与性质相对应的说法正确的有几个 ( )
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
③浓硫酸可用作干燥剂是因为其具有脱水性
④光导纤维可用作通讯材料是因为其具有导电性
⑤MgO、Al2O3的熔点很高,可制作耐高温材料
⑧NaHCO3能与碱反应,因此食品工业上用作焙制糕点的膨松剂
⑦铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
③浓硫酸可用作干燥剂是因为其具有脱水性
④光导纤维可用作通讯材料是因为其具有导电性
⑤MgO、Al2O3的熔点很高,可制作耐高温材料
⑧NaHCO3能与碱反应,因此食品工业上用作焙制糕点的膨松剂
⑦铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
2 . 下列物质性质与用途具有对应关系的是
| A.银氨溶液具有弱氧化性,可用于制银镜 |
| B.MgO在水中的溶解度小,可用作耐火材料 |
| C.NH3具有还原性,可用作制冷剂 |
| D.NH4HCO3 受热易分解,可用作氮肥 |
您最近一年使用:0次
解题方法
3 . 下列关于Na、Mg、Al、Fe、Cu的说法正确的是
| A.常温下,Al、Cu均不与氧气反应 |
| B.Al、Fe的阳离子,只有氧化性没有还原性 |
| C.Na、Mg的单质放置在空气中均只生成氧化物 |
| D.只需用水就可以鉴别MgSO4、Al2(SO4)3和NaOH |
您最近一年使用:0次
4 . 下列实验操作能达到实验目的的是
| 实验操作 | 实验结论 | |
| A | 向NaBr溶液中滴入少量氯水和 ,振荡、静置,下层溶液呈橙红色 ,振荡、静置,下层溶液呈橙红色 |  氧化性强于 氧化性强于 |
| B | 向某溶液中加入硝酸酸化的 溶液,生成白色沉淀 溶液,生成白色沉淀 | 该溶液中含 |
| C | 向1mL蛋白质溶液中逐滴加入饱和硫酸铵溶液,出现沉淀 | 蛋白质发生变性 |
| D | 常温下,测得 饱和溶液pH大于 饱和溶液pH大于 饱和溶液pH 饱和溶液pH | 碱性: 金属性:  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列有关物质性质与用途具有对应关系的是
| A.MgO熔点高,可用于电解冶炼镁 |
| B.酒精具有挥发性,可用于消毒杀菌 |
| C.Na2O2具有强氧化性,可用作供氧剂 |
| D.Fe粉具有还原性,可用作食品袋中的抗氧化剂 |
您最近一年使用:0次
6 . 根据下列实验操作和现象得出的结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向CuSO4溶液中通入适量H2S气体 | 有黑色沉淀生成 | 酸性:H2S>H2SO4 |
| B | 将MgSO4溶液与足量的NaOH溶液混合 | 有白色沉淀生成 | Mg(OH)2不溶于强碱 |
| C | 向待测液中加入适量的浓氢氧化钠溶液并加热,将湿润的红色石蕊试纸放在试管口 | 试纸变蓝色 | 待测液中含有NH |
| D | 向Fe(NO3)3溶液中加入HI溶液,再加入苯,振荡、静置 | 上层溶液呈紫红色,下层溶液呈黄色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-17更新
|
419次组卷
|
2卷引用:海南省2021-2022学年高三上学期学业水平诊断考试化学试题
2019高三·全国·专题练习
7 . 某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应。资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案验证产物并探究反应原理。
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红色变为红色。
(1)该小组对反应中产生的白色不溶物作出如下假设:
假设1:可能为_______________________________________ 。
假设2:可能为MgCO3。
假设3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证假设:
(3)设计定量实验确定实验Ⅰ的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物6.20 g,充分加热灼烧至不再产生气体为止,并使分解产生的气体全部进入装置A(盛足量浓硫酸)和B(盛足量碱石灰)中,装置A增重0.36 g,装置B增重2.64 g,则白色不溶物的化学式为________ 。
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红色变为红色。
(1)该小组对反应中产生的白色不溶物作出如下假设:
假设1:可能为
假设2:可能为MgCO3。
假设3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证假设:
| 实验序号 | 实验 | 预期现象和结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量 | 产生气泡,沉淀全部溶解;白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2溶液 | 产生白色沉淀;说明溶液中存在的离子有 |
(3)设计定量实验确定实验Ⅰ的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物6.20 g,充分加热灼烧至不再产生气体为止,并使分解产生的气体全部进入装置A(盛足量浓硫酸)和B(盛足量碱石灰)中,装置A增重0.36 g,装置B增重2.64 g,则白色不溶物的化学式为
您最近一年使用:0次
名校
8 . 纳米氧化镁是在磁性、催化方面有许多特异功能的新材料,具有重要价值。工业以菱镁矿(主要成分为MgCO3,少量FeCO3和SiO2杂质)为原料制备纳米氧化镁工艺流程如图:
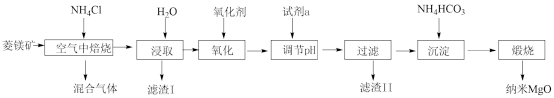
试回答下列问题:
(1)“焙烧”时生成的主要气体有___________ ;滤渣I的主要成分为___________ 。
(2)已知在该条件下金属离子开始沉淀和完全沉淀的pH如表:
上述流程中“氧化”的目的是___________ 。氧化剂常用空气或H2O2而不选用酸性KMnO4,解释其原因___________ 。
(3)试剂a可能是___________ 。
(4)资料显示煅烧MgCO3比煅烧Mg(OH)2更容易生成MgO纳米材料。“沉淀”时若将NH4HCO3更换成Na2CO3,则产生的后果是___________ 。
(5)该流程中可以循环利用的物质是___________ 。

试回答下列问题:
(1)“焙烧”时生成的主要气体有
(2)已知在该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe2+ | Fe3+ | Mg2+ |
| 开始沉淀pH | 6.3 | 1.5 | 8.9 |
| 完全沉淀pH | 8.1 | 2.8 | 10.9 |
(3)试剂a可能是
(4)资料显示煅烧MgCO3比煅烧Mg(OH)2更容易生成MgO纳米材料。“沉淀”时若将NH4HCO3更换成Na2CO3,则产生的后果是
(5)该流程中可以循环利用的物质是
您最近一年使用:0次
9 . 资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为_________ ;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示:
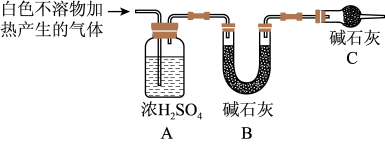
称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:_________ ;(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:_________ 。
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为 |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量 | 白色不溶物可能含有猜测2中不溶物 | |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 |

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:
您最近一年使用:0次
2016-12-09更新
|
584次组卷
|
3卷引用:2014年化学高考题型专练十八 探究型综合实验题练习卷
名校
解题方法
10 . 下列有关物质的性质与用途具有对应关系的是
| A.MgCO3分解吸热,可用于治疗胃酸过多 |
| B.浓硫酸难挥发,可用于催化酯化反应 |
| C.FeCl3具有氧化性,可用作净水剂 |
| D.碳酸钠溶液呈碱性,可用于去除油污 |
您最近一年使用:0次
2020-12-23更新
|
193次组卷
|
2卷引用:江苏省南通市如皋中学2020-2021学年高三上学期教学质量调研(二)化学试题



