1 . 某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子,并尽可能减少AlCl3的损失.请回答下列问题:
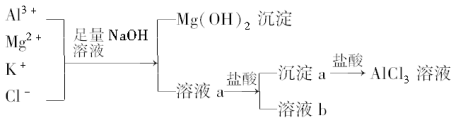
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:________ 、________ 、________ .氢氧化钠溶液能否用氨水代替,为什么?______________________ .
(2)溶液a中存在的离子有________ ;在溶液a中加入盐酸时需控制溶液的pH,为什么?________ ;为此,改进方法是____________________ .
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?____________________ .

(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
(2)溶液a中存在的离子有
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?
您最近一年使用:0次
名校
2 . 蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下图所示:

(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是__________ 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致__________ 溶解、________ 沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入__________ (填写物质的化学式),然后过滤、洗涤、灼烧。
(4)现设计一个实验,确定产品aMgCO3•bMg(OH)2•cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解
③______________________________________________________ 。
④称量碱石灰吸收CO2前后的质量 ⑤MgO称量
(5)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:a=____________ ,b=____________ ,c=____________ 。

(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入
(4)现设计一个实验,确定产品aMgCO3•bMg(OH)2•cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解
③
④称量碱石灰吸收CO2前后的质量 ⑤MgO称量
(5)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:a=
您最近一年使用:0次
3 . 只选用下列试剂中的一种就可以鉴别氯化铁、硝酸钠、氯化铝和硫酸镁四种溶液。这种试剂是
| A.BaCl2 | B.KSCN |
| C.NaOH | D.AgNO3 |
您最近一年使用:0次
2017-09-25更新
|
292次组卷
|
2卷引用:湖南省永州市祁阳县高考补习学校2018届高三上学期第二次月考化学试题
4 . 无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:


步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5 MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是____________ 。
实验中不能用干燥空气代替干燥N2,原因是___________ 。
(2)如将装置B改为装置C(图2),可能会导致的后果是___________ 。
(3)步骤3中,第一次过滤除去的物质是___________ 。
(4)有关步骤4的说法,正确的是___________ 。
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++ Y4-="===Mg" Y2-
①滴定前润洗滴定管的操作方法是__________ 。
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________________________ (以质量分数表示)。


步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5
 MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5请回答:
(1)仪器A的名称是
实验中不能用干燥空气代替干燥N2,原因是
(2)如将装置B改为装置C(图2),可能会导致的后果是
(3)步骤3中,第一次过滤除去的物质是
(4)有关步骤4的说法,正确的是
| A.可用95%的乙醇代替苯溶解粗品 | B.洗涤晶体可选用0℃的苯 |
| C.加热至160℃的主要目的是除去苯 | D.该步骤的目的是除去乙醚和可能残留的溴 |
Mg2++ Y4-="===Mg" Y2-
①滴定前润洗滴定管的操作方法是
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是
您最近一年使用:0次
2016-12-09更新
|
1509次组卷
|
6卷引用:【全国百强校】湖南省长沙市第一中学2019届高三下学期第七次月考理科综合化学试题
【全国百强校】湖南省长沙市第一中学2019届高三下学期第七次月考理科综合化学试题2017届四川省成都树德中学高三10月月考化学卷四川省雅安中学2018届高三上学期第一次月考化学试题2016年全国普通高等学校招生统一考试化学(浙江卷精编版)2016年全国普通高等学校招生统一考试化学(浙江卷参考版)(已下线)专题22.综合实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)
5 . 在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2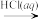 SiCl4 SiCl4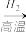 Si Si |
B.FeS2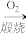 SO2 SO2 H2SO4 H2SO4 |
C.N2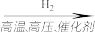 NH3 NH3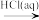 NH4Cl(aq) NH4Cl(aq) |
D.MgCO3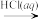 MgCl2(aq) MgCl2(aq)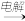 Mg Mg |
您最近一年使用:0次
2016-12-09更新
|
1482次组卷
|
32卷引用:湖南省长沙市雅礼中学2020届高三上学期第3次月考化学试题
湖南省长沙市雅礼中学2020届高三上学期第3次月考化学试题2017届广西钦州港经济开发区中学高三上9月月考化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题湖南省长沙市第一中学2018届高三上学期无机化合物综合练习(一)化学试题广东省蓝精灵中学2018-2019学年高二上学期联考化学试题【全国百强校】福建省莆田市仙游县第一中学2018-2019学年高一下学期第一次月考(3月)化学试题陕西省西安市第一中学2021届高三上学期第五次模拟考试化学试题16 2024年苏州第十中学高二3月月考2015-2016学年江苏省天一中学高二下学期期末化学试卷2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2017届安徽省师大附中高三上学期期中化学试卷2016-2017学年湖北省蕲春县高二上学期期中化学试卷2017届江西师大附中高三上学期期中化学试卷安徽省师范大学附属中学2016-2017学年高一下学期期末考试化学试题2018版化学(苏教版)高考总复习专题一对接高考精练--物质的组成、性质及分类吉林省抚松五中 、 长白县实验中学、长白山二中、长白山实验中学2018届高三四盟校期中联考化学试题福建省福建师范大学第二附属中学2018届高三上学期期中考试化学试题(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第1讲 碳、硅及其无机非金属材料【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第4讲 氮及其化合物 (教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)(已下线)考点01 传统文化化学与生活化学基本概念——《备战2020年高考精选考点专项突破题集》(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)北京市第四中学2023-22024学年高一下学期期中考试 化学试题
6 . 下列各组反应中,最终的溶液中无白色沉淀的是
| A.AlCl3溶液中加入过量氨水 |
| B.Al2(SO4)3溶液中加入过量KOH溶液 |
| C.MgCl2溶液中加入过量氨水 |
| D.MgSO4溶液中加入过量KOH溶液 |
您最近一年使用:0次
2016-12-09更新
|
105次组卷
|
5卷引用:湖南省浏阳市第一中学2016-2017学年高一下学期入学考试化学试卷
解题方法
7 . 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解。向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示。
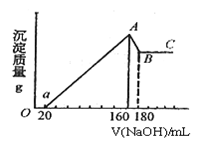
①A点时,n Mg(OH)2=_____ mol;nAl(OH)3= _______ mol。
②原HCl的物质的量浓度c=_______________ mol/L

①A点时,n Mg(OH)2=
②原HCl的物质的量浓度c=
您最近一年使用:0次
8 . 向x的溶液中,加入Y试剂,产生的沉淀示意图如图所示的是(注意线段的斜率)
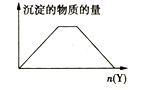

| A.向NaOH和Ca(OH)2的混合液中通入CO2 |
| B.向HCl和A1C13的混合液中滴加NaOH溶液 |
| C.向NH4A1(SO4)2溶液中滴加NaOH溶液 |
| D.向NH4C1和MgCl2的混合液中滴加NaOH溶液 |
您最近一年使用:0次
9 . AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,则消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系可用如图来表示,则下列关系图正确的是
A.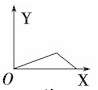 | B.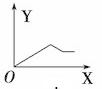 | C. | D.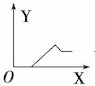 |
您最近一年使用:0次
2015-10-23更新
|
197次组卷
|
3卷引用:2016届湖南省石门县一中高三第一次月考化学试卷
10 . (1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________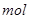 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________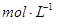 。
。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入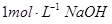 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
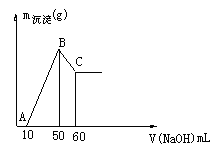
①合金中镁的质量 g。
②盐酸的物质的量浓度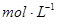 。
。
 MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________
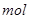 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________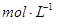 。
。(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入
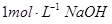 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
①合金中镁的质量 g。
②盐酸的物质的量浓度
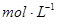 。
。
您最近一年使用:0次
2015-06-03更新
|
465次组卷
|
2卷引用:2014-2015学年湖南省益阳市箴言中学高一12月月考化学试卷



