1 . I.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
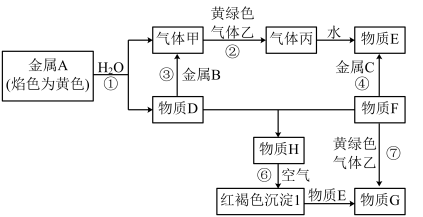
请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:_______ ;
(2)反应③的离子方程式:_______ ;
(3)反应⑦的离子方程式:_______ ;
(4)反应⑥的化学方程式:_______ 。
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
(5)铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是_______ 的质量分数;当合金熔点最低时,合金中铅与锡的质量比为_______ 。

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
(7)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿[主要成分Cu2(OH)2CO3],从其化学式可知铜绿是铜与_______ (填物质的化学式)长期作用的结果。

请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:
(2)反应③的离子方程式:
(3)反应⑦的离子方程式:
(4)反应⑥的化学方程式:
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
| A.20~40℃ | B.60~80℃ | C.230~250℃ | D.300~320℃ |
您最近一年使用:0次
2022-12-07更新
|
116次组卷
|
2卷引用:山西省怀仁市第一中学校云东校区2021-2022学年高一上学期第三次月考理综化学试题
名校
解题方法
2 . 下列各组离子在指定溶液中可能大量共存的是
A.滴加石蕊显红色的溶液:K+、Cl-、Na+、MnO 、SO 、SO |
| B.某透明溶液:Na+、Fe3+、SCN-、Cl- |
C.滴加酚酞显红色的溶液:Na+、HCO 、SO 、SO 、Cl- 、Cl- |
D.加入铝片可以产生H2的溶液:K+、Mg2+、Cl-、SO |
您最近一年使用:0次
2022-12-07更新
|
63次组卷
|
2卷引用:山西省怀仁市第一中学校云东校区2021-2022学年高一上学期第三次月考理综化学试题
解题方法
3 . 阅读材料,回答下列问题。
近年来,科研人员研究得到一种新型材料-泡沫铝。它是把发泡剂加到熔融铝合金中制成的,其优点是硬度大,密度小(为0.16~0.5 g/cm3),比木材还轻,可浮于水面,又有很大刚性,且隔音、保温,是一种良好的建筑材料和轻质材料。
(1)中国人民最早使用的合金是_______(填字母序号,下同)。
(2)下列关于泡沫铝的说法中错误的是_______ 。
(3)铝制成铝箔用于食品包装,是利用它的_______。
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为甲∶乙=1∶2,则加入铝粉质量为
(5)铝在空气中会被氧化生成一层致密的氧化膜而对内部铝起保护作用,但这层氧化膜遇到强酸或强碱溶液都会溶解,请写出:
①氧化膜与盐酸反应的离子方程式:_______ 。
②氧化膜与氢氧化钠溶液反应的离子方程式:_______ 。
近年来,科研人员研究得到一种新型材料-泡沫铝。它是把发泡剂加到熔融铝合金中制成的,其优点是硬度大,密度小(为0.16~0.5 g/cm3),比木材还轻,可浮于水面,又有很大刚性,且隔音、保温,是一种良好的建筑材料和轻质材料。
(1)中国人民最早使用的合金是_______(填字母序号,下同)。
| A.黄铜 | B.生铁 | C.青铜 | D.陨铁 |
| A.泡沫铝是铝单质泡沫 | B.泡沫铝是一种合金 |
| C.泡沫铝是一种优质的建筑材料和轻质材料 | D.泡沫铝可用于飞机制造 |
| A.金属光泽 | B.延展性 | C.导电性 | D.导热性 |
| A.5.4 g | B.3.6 g | C.2.7 g | D.1.8 g |
①氧化膜与盐酸反应的离子方程式:
②氧化膜与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
4 . 下列实验现象描述错误的是
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的钠 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落,好像有一层膜兜着 |
| C | 在Cl2中点燃铁丝 | 铁丝剧烈燃烧,并伴有棕黄色的烟 |
| D | 在空气中久置的铝条放入NaOH溶液中 | 立刻产生大量无色气体,铝条逐渐变细 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
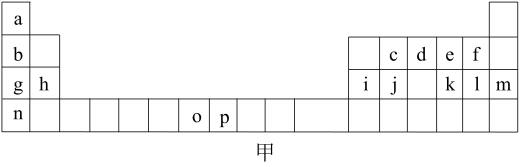
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:_______ 。
(2)c、d、e、f四种元素的第一电高能由大到小的顺序为_______ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_______ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的 、
、 可知,气态基态
可知,气态基态 再失去一个电子比基态气态
再失去一个电子比基态气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_______ 。
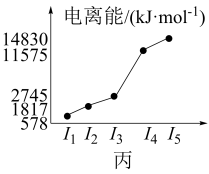
(5)图甲中的某主族元素的电离能情况如图丙所示,则该元素的单质与氢氧化钠溶液反应的化学方程式为_______ 。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电高能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
电高能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 |
 、
、 可知,气态基态
可知,气态基态 再失去一个电子比基态气态
再失去一个电子比基态气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(5)图甲中的某主族元素的电离能情况如图丙所示,则该元素的单质与氢氧化钠溶液反应的化学方程式为

您最近一年使用:0次
名校
6 . 下列除杂方法正确且除杂过程中不涉及氧化还原反应的是
| 选项 | 物质 | 杂志 | 除杂方法 |
| A | Na2CO3 | NaHCO3 | 置于硬质玻璃管中充分加热 |
| B | Cl2 | HCl | 通入饱和Na2CO3溶液中 |
| C | Fe | Al | 加入NaOH溶液,过滤 |
| D | NaOH | Ca(OH)2 | 加入足量K2CO3溶液,充分反应后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 设阿伏加德罗常数的数值为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.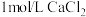 溶液中含氯离子数为 溶液中含氯离子数为 |
B.常温常压下,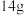 氮气所含的分子数为 氮气所含的分子数为 |
C.常温下,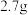 铝与足量的盐酸反应,失去的电子数为 铝与足量的盐酸反应,失去的电子数为 |
D.标准状况下, 水中含有的原子数为 水中含有的原子数为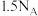 |
您最近一年使用:0次
2022-01-23更新
|
209次组卷
|
4卷引用:山西省临汾新华中学2021-2022学年高一上学期第四次月考化学试题
名校
解题方法
8 . 下列离子方程式书写正确的是
| A.铁和盐酸溶液反应:2Fe+ 6H+=2Fe3++3H2↑ |
| B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe2+ |
C.铝片溶于氢氧化钠溶液:Al+2OH-+H2O=AlO +2H2↑ +2H2↑ |
| D.氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH)3↓ |
您最近一年使用:0次
2022-01-10更新
|
230次组卷
|
2卷引用:山西省临县第一中学2021-2022学年高一上学期12月月考化学试题
9 . 把13.4g镁铝铜合金的粉末加入过量的盐酸中,在标准状况下放出氢气11.2L,反应后过滤得沉淀3.2g。试计算:
(1)该合金中镁的质量分数(保留小数点后一位数);___________
(2)该合金中镁、铝、铜的物质的量之比。___________
(1)该合金中镁的质量分数(保留小数点后一位数);
(2)该合金中镁、铝、铜的物质的量之比。
您最近一年使用:0次
名校
10 . 在给定条件下,下列选项所示的物质间转化均能实现的是
A.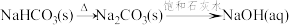 |
B. |
C. |
D.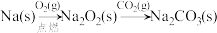 |
您最近一年使用:0次
2022-01-01更新
|
305次组卷
|
2卷引用:山西省运城市教育发展联盟2021-2022学年高一上学期12月月考化学试题



