2012·湖北·一模
名校
1 . 已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
| A.NO | B.NO2 | C.N2O | D.NH4NO3 |
您最近一年使用:0次
2017-11-09更新
|
568次组卷
|
6卷引用:2013届山西省平遥中学高三上学期12月质检考试化学试卷
(已下线)2013届山西省平遥中学高三上学期12月质检考试化学试卷(已下线)2012届湖北省普通高等学校招生5月适应性考试化学试卷(已下线)2012届北京市清华附中高三考前适应性训练理综化学试卷黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题广东省清远市第一中学实验学校2020届高三第四次月考理综化学试题(已下线)上海市虹口区2014届高三三模化学试题
名校
解题方法
2 . 某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:

(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________________ 。
(2)白色物质是__________ ,用化学方程式解释其变为红褐色的原因:____________________ 。
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
(i)根据以上实验现象,可以判断滤液中存在____________________ 离子。
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因____________________ 。

| 实验步骤 | 实验现象 |
| 1、打开弹簧夹,缓慢通入N2 | |
| 2、加入pH为2.5的0.01mol/L酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色; 铁粉不再溶解后,剩余铁粉表面出现少量白色物质附着。 |
| 3、反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化。 |
| 4、将剩余固体过滤 | 表面的白色物质变为红褐色。 |
(2)白色物质是
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
| 实验步骤 | 实验现象 |
| 1、取部分滤液于试管中,向其中加入KSCN溶液 | 溶液液无变化 |
| 2、将上述溶液分为两份,一份中滴入氯气;另一份中滴加稀硫酸 | 两份溶液均变为红色 |
| 3、另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸。 | 有气体生成,该气体使红色石蕊试纸变蓝。 |
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因
您最近一年使用:0次
2017-08-31更新
|
512次组卷
|
5卷引用:山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题
山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题北京市师范大学附属实验中学2015-2016学年高一下学期期末考试化学试题(已下线)3.3.3 硝酸的性质 人类活动对氮循环和环境的影响练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)河北省三河市第一中学2020-2021学年高一下学期第一次阶段考化学试题广东省佛山市顺德区容山中学2022-2023学年高一下学期3月月考化学试题
3 . 已知100mL某硫酸亚铁、硫酸、硫酸铁混合溶液中阳离子浓度相等,硫酸根离子总浓度为6mol/L,此溶液中还可溶解铁粉的质量为
| A.11.2g | B.16.8g | C.33.5g | D.5.6g |
您最近一年使用:0次
名校
4 . 某不纯铁片可能含有Mg、Al、Cu等金属杂质,取这种铁片5.6 g与足量的稀盐酸反应,得到0.2 g氢气,则该铁片中
| A.一定含金属镁 | B.一定含金属铝 |
| C.一定含金属铜 | D.一定同时含有四种金属 |
您最近一年使用:0次
2017-08-24更新
|
966次组卷
|
5卷引用:山西省忻州市第一中学2016-2017学年高一必修一:3.1.2金属的化学性质同步练习化学试题
名校
5 . 下列说法正确的是
| A.钠、铁均是银白色金属,熔点高,硬度大 |
| B.实验室中,通常将钠保存在四氯化碳中 |
| C.钠在空气中燃烧产生黄色火焰 |
| D.高温时,铁与水蒸气反应生成氧化铁与氢气 |
您最近一年使用:0次
2017-08-24更新
|
524次组卷
|
4卷引用:山西省忻州市第一中学2016-2017学年高一必修一:3.1.1金属的化学性质同步练习化学试题
名校
6 . 将5g含镁、锌和铁的三种金属的混和物投入到40mL稀硫酸中,恰好完全反应,产生的氢气在标况下是2.8L,则三种金属的物质的量之和为
| A.0.25mol | B.0.125mol |
| C.0.1mol | D.0.5mol |
您最近一年使用:0次
2017-08-24更新
|
1708次组卷
|
7卷引用:山西省忻州市第一中学2016-2017学年高一必修一:3 金属及其化合物 单元复习同步练习化学试题
7 . 铁、铜混合粉末20.0g加入到100mL 5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2g(忽略反应前后溶液体积变化)。求:
(1)反应后溶液中FeCl2的物质的量浓度_____________ mol·L-1
(2)原固体混合物中铜的质量分数是_____________
(1)反应后溶液中FeCl2的物质的量浓度
(2)原固体混合物中铜的质量分数是
您最近一年使用:0次
2017-02-23更新
|
338次组卷
|
3卷引用:山西省晋中市祁县中学校2020届高三上学期10月月考化学试题
8 . 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
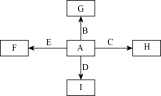
(1)① 中反应的化学方程式为________________________ ;
(2)化合物Ⅰ的电子式为____________ ,它的空间构型是______________ ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量_____________ (写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________ ,反应后溶液与过量化合物Ⅰ反应的离子方程式为__________________ ;
(5)E在I中燃烧观察到的现象是_____________________ 。
 B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)① 中反应的化学方程式为
(2)化合物Ⅰ的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
(4)C与过量NaOH溶液反应的离子方程式为
(5)E在I中燃烧观察到的现象是
您最近一年使用:0次
2016-12-09更新
|
271次组卷
|
2卷引用:山西省阳高县第一中学2018届高三上学期第二次月考化学试题
9 . 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)
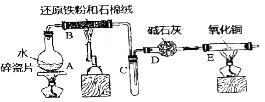
(1)装置B中发生反应的化学方程式是________ ;
(2)装置E中的现象是________ ;
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为________ ,现象是________ ;
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因________ ;
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的________
④在③所得溶液浓缩结晶前需要用实验证明FeCl2已完全氧化,实验方法是________ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的
| A.酸性KMnO4溶液 | B.Cl2 | C.Na2O2 | D.FeCl3 |
您最近一年使用:0次
2016-12-09更新
|
426次组卷
|
3卷引用:2015-2016学年山西省怀仁一中高一下第一次月考化学试卷
2015-2016学年山西省怀仁一中高一下第一次月考化学试卷(已下线)第三章 章末检测(1)——《高中新教材同步备课》(人教版 必修第一册)安徽省池州市第一中学2020-2021学年高一12月月考化学试题
12-13高一上·陕西·期末
名校
解题方法
10 . 将6 g的铁粉加入200 mLFe2(SO4)3和CuSO4的混合溶液,充分反应得到200 mL0.5mol /LFeSO4溶液和5.2 g固体沉淀物。试计算
(1)反应后生成铜的质量;
(2)原Fe2(SO4)3溶液的物质的量浓度。
(1)反应后生成铜的质量;
(2)原Fe2(SO4)3溶液的物质的量浓度。
您最近一年使用:0次
2016-12-09更新
|
880次组卷
|
9卷引用:2014-2015山西省山大附中高一12月月考化学试卷
2014-2015山西省山大附中高一12月月考化学试卷【全国百强校】山西省山西大学附属中学2018-2019学年高一上学期12月月考化学试题(已下线)2011-2012学年陕西省陕师大附中高一上学期期末试题化学(理)试卷2015-2016学年河南省周口市高一上学期期末考试化学试卷江西省抚州市南城县第二中学2019-2020学年高一上学期第二次月考化学试题(已下线)【南昌新东方】师大附中2019-2020 高一(上) 期末(已下线)第03章 铁 金属材料(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)黑龙江嫩江市高级中学2020-2021学年高一上学期第一次月考化学试题甘肃省武威市凉州区2021-2022学年高一上学期期末考试化学试题



