名校
1 .  (三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。
(三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。
回答下列问题:
I.利用如图所示装置检验三草酸合铁酸钾受热分解所得产物中是否含有 ,
, (下列仪器可重复使用)。
(下列仪器可重复使用)。
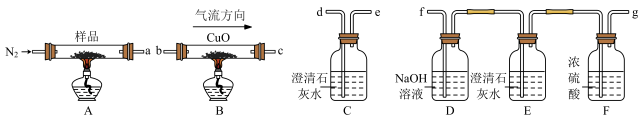
(1)为达到实验目的,连接以上装置,c接___________ (填小写标号),D装置的作用是___________ 。
(2)样品完全分解后,装置A中残留物含有FeO和Fe2O3,为证明残留物中存在FeO,选择的试剂包含___________ (填写试剂的编号)。
提供试剂:①稀盐酸 ②稀硫酸 ③KSCN溶液 ④氯水 ⑤NaOH溶液 ⑥KMnO4溶液。
Ⅱ.测定三草酸合铁酸钾样品(含杂质)中铁元素的含量。
(3)称取mg三草酸合铁酸钾样品,溶于水配成250mL溶液,所需玻璃仪器除烧杯、玻璃棒、量筒外还有___________ (填仪器名称)。
(4)取25mL上述溶液于锥形瓶中,加入稀硫酸酸化,再滴加KMnO4溶液至恰好与 反应,反应的离子方程式为
反应,反应的离子方程式为___________ 。
(5)向(4)反应后溶液中加入足量Zn固体,将Fe3+还原成Fe2+,过滤,用cmol/L酸性KMnO4溶液滴定。测得实验数据如下表:
酸性高锰酸钾溶液应该装在如图___________ (填“A”或“B”)滴定管中,晶体中铁元素的质量分数为___________ ,若配制样品溶液定容时俯视读数会导致测定结果___________ (填“偏高”“偏低”或“无影响”)。

 (三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。
(三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。回答下列问题:
I.利用如图所示装置检验三草酸合铁酸钾受热分解所得产物中是否含有
 ,
, (下列仪器可重复使用)。
(下列仪器可重复使用)。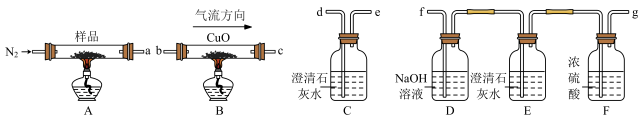
(1)为达到实验目的,连接以上装置,c接
(2)样品完全分解后,装置A中残留物含有FeO和Fe2O3,为证明残留物中存在FeO,选择的试剂包含
提供试剂:①稀盐酸 ②稀硫酸 ③KSCN溶液 ④氯水 ⑤NaOH溶液 ⑥KMnO4溶液。
Ⅱ.测定三草酸合铁酸钾样品(含杂质)中铁元素的含量。
(3)称取mg三草酸合铁酸钾样品,溶于水配成250mL溶液,所需玻璃仪器除烧杯、玻璃棒、量筒外还有
(4)取25mL上述溶液于锥形瓶中,加入稀硫酸酸化,再滴加KMnO4溶液至恰好与
 反应,反应的离子方程式为
反应,反应的离子方程式为(5)向(4)反应后溶液中加入足量Zn固体,将Fe3+还原成Fe2+,过滤,用cmol/L酸性KMnO4溶液滴定。测得实验数据如下表:
| 实验次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 0.10 | 20.20 |
| 2 | 0.52 | 20.52 |
| 3 | 1.85 | 21.75 |
| 4 | 0.00 | 24.06 |

您最近一年使用:0次
解题方法
2 . 氢溴酸常用于合成镇静剂和麻醉剂等医药用品。已知: 液溴是易挥发的深红棕色液体,沸点为58.78℃。质量分数为47%的氢溴酸是易挥发的无色液体,沸点 为 126℃. 实验室制备质量分数为47%的氢溴酸的一种方法如下。回答下列问题:
(2)操作 II的蒸馏装置如图所示(部分夹持装置省略),仪器a的名称是_________ ,装置中除缺石棉网外还有两处明显错误,分别是_________ 、 _______________ 。
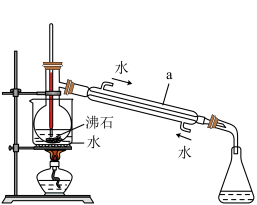
(3)操作III加入适量Na2SO3发生反应的离子方程式为__________ 。
(4)工业生产制得的氢溴酸常常有淡淡的黄色, 有同学推测是因为含Fe3+,可用试剂__________ 检验。若观察到的现象为________ ,则推测正确。
(5)质量分数为 47%的氢溴酸的产率为__________ 。
实验橾作 | 现象 |
| I .向锥形瓶中依次加入适量冰水、m1g 液溴,再通入SO2充分反应 | 得到淡黄色溶液 |
| II. 将操作 I 所得溶液转移至蒸馏烧瓶,蒸馏 | 锥形瓶中得橙黄色粗产品 |
| III.在不断搅拌下,向锥形瓶中加入适量Na2SO3溶液 | (1)① |
| IV.继续加入适量 Ba(OH)2溶液 | ② |
| V.过滤,滤液经蒸馏后得质量分数为47%的氢溴酸m2g |

(3)操作III加入适量Na2SO3发生反应的离子方程式为
(4)工业生产制得的氢溴酸常常有淡淡的黄色, 有同学推测是因为含Fe3+,可用试剂
(5)质量分数为 47%的氢溴酸的产率为
您最近一年使用:0次
3 . 下列实验操作能达到相应目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 证明加碘食盐中存在 | 向食盐水中加入 溶液,取该溶液滴在碘化钾淀粉试纸上 溶液,取该溶液滴在碘化钾淀粉试纸上 |
| B | 证明 溶液部分被氧化 溶液部分被氧化 | 向 溶液中滴加 溶液中滴加 溶液 溶液 |
| C | 证明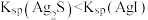 | 向 溶液中滴加 1 mL 溶液中滴加 1 mL  KI再滴加 1 mL KI再滴加 1 mL 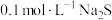 溶液 溶液 |
| D | 制备 胶体 胶体 | 将饱和 溶液滴入NaOH溶液 溶液滴入NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列实验能达到实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将CuCl2·H2O晶体置于坩埚中加入 | 制备CuCl2固体 |
| B | 加热氯化铵和氢氧化钙的混合物,并将产生的气体通过装有无水氯化钙的干燥管 | 制取氨气并干燥 |
| C | 向FeCl2溶液中滴加酸性高锰酸钾溶液 | 证明Fe2+具有还原性 |
| D | 向装有亚硫酸钠白色固体粉末的圆底烧瓶中加入浓硫酸,用排饱和亚硫酸氢钠的方法收集气体 | 制取并收集二氧化碳 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 按表中如图所示装置完成下列实验,预测的现象不合理的是
| 选项 | 滴管 | 试管 | 预测的现象 |  |
| A | 浓硫酸 | 铝片 | 持续产生使品红溶液褪色的气体 | |
| B | 浓氨水 | CaO固体 | 产生使湿润的红色石蕊试纸变蓝的气体 | |
| C | KSCN溶液 | FeCl3溶液 | 溶液变为红色 | |
| D | KI溶液 | AgCl悬浊液 | 白色沉淀变黄 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 工业上由黄铜矿(主要成分为CuFeS2)冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的____ 吸收。
a.浓硫酸 b.稀硝酸 c.NaOH溶液 d.氨水
(2)用稀硫酸浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_____ (填离子符号),检验溶液中还存在Fe2+的方法是_______ (注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为______________ 。
(4)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_____ 。随着放电的进行电解质溶液pH变____ 。(填大、小、或不变)

(1)气体A中的大气污染物可选用下列试剂中的
a.浓硫酸 b.稀硝酸 c.NaOH溶液 d.氨水
(2)用稀硫酸浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)由泡铜冶炼粗铜的化学反应方程式为
(4)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
您最近一年使用:0次



