名校
解题方法
1 . 由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4•7H2O),然后制取透明氧化铁颜料的流程如图:
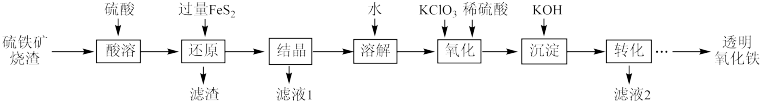
已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是_____ 。
(2)“滤渣”中的主要成分是_____ (填名称)。
(3)流程中“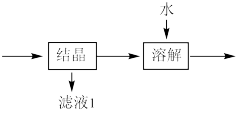 ”环节的目的是
”环节的目的是_____ 。
(4)“还原”过程中涉及的离子方程式为_____ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以_____ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。
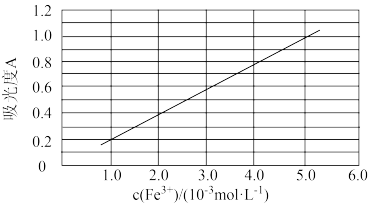
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为_____ 。

已知:
I.透明氧化铁又称纳米氧化铁,粒子直径很微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
II.Fe3+能将FeS2中的硫元素氧化为+6价。
(1)FeS2的电子式是
(2)“滤渣”中的主要成分是
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“还原”过程中涉及的离子方程式为
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示。

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL,测得溶液吸光度A=0.8,则透明氧化铁中氧化铁黄的质量分数为
您最近一年使用:0次
2 . K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。请回答下列问题:
某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

(1)通入氮气的目的是_____ 。
(2)实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有____ 和____ 。
(3)为防止倒吸,停止实验时应进行的操作是___ 。
(4)样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:____ 。
(5)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用cmol•L-1KMnO4,溶液滴定至终点。在滴定管中装入KMnO4溶液(装液)的前一步,应进行的操作为____ 。滴定终点的现象是____ 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为_____ 。若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,则测定结果____ (填“偏高”或“偏低”)。
某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

(1)通入氮气的目的是
(2)实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
(3)为防止倒吸,停止实验时应进行的操作是
(4)样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
(5)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用cmol•L-1KMnO4,溶液滴定至终点。在滴定管中装入KMnO4溶液(装液)的前一步,应进行的操作为
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
名校
解题方法
3 . 计算(要有计算过程)
(1)常温常压下,用等质量的 、
、 、
、 三种气体分别吹出三个气球,求三个气球的体积之比为
三种气体分别吹出三个气球,求三个气球的体积之比为______ 。
(2)把 溶液和
溶液和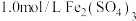 溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中
溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中 的物质的量浓度
的物质的量浓度___________ 。
(3)某种胃药的有效成分为碳酸钠,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药片(0.10g)中加入20.00ml蒸馏水;
②配置 稀盐酸和
稀盐酸和 溶液;
溶液;
③加入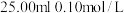 稀盐酸;
稀盐酸;
④用 溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
某同学4次测定所消耗的NaOH溶液的体积如下:
根据这个同学的实验数据,计算这种药片中碳酸钙的质量分数_________ 。
(1)常温常压下,用等质量的
 、
、 、
、 三种气体分别吹出三个气球,求三个气球的体积之比为
三种气体分别吹出三个气球,求三个气球的体积之比为(2)把
 溶液和
溶液和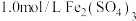 溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中
溶液各0.5L混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。求此时溶液中 的物质的量浓度
的物质的量浓度(3)某种胃药的有效成分为碳酸钠,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药片(0.10g)中加入20.00ml蒸馏水;
②配置
 稀盐酸和
稀盐酸和 溶液;
溶液;③加入
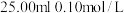 稀盐酸;
稀盐酸;④用
 溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;
溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积;某同学4次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
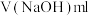 | 13.00 | 12.90 | 13.10 | 13.50 |
您最近一年使用:0次
解题方法
4 . 硼镁泥是一种工业废料,主要成分是MgO(占40%,质量分数),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4∙7H2O的工艺流程如图:
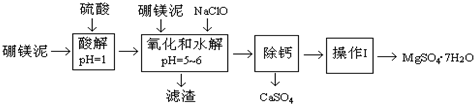
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,浓硫酸的浓度为_______ mol·L-1 ,量取浓硫酸需要使用量筒的规格为_______ (填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO‾ + H2O = MnO2↓+ 2H+ + Cl‾,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为_______ 。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有_______ 。
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法_______ 。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤_______ 、_______ 。

(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,浓硫酸的浓度为
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO‾ + H2O = MnO2↓+ 2H+ + Cl‾,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤
您最近一年使用:0次
名校
解题方法
5 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。
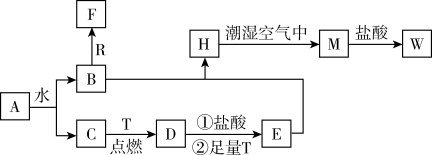
请回答下列问题:
(1)A的电子式是_____ ,R元素在元素周期表中位置为______ ,D的俗称是_____ 。
(2)A与水反应的离子方程式为______ 。
(3)检验W溶液中金属阳离子的操作方法是_______ 。
(4)H转化为M的化学方程式为_______ 。
(5)B生成F的反应中氧化剂是_____ ,反应的离子方程式为______ 。

请回答下列问题:
(1)A的电子式是
(2)A与水反应的离子方程式为
(3)检验W溶液中金属阳离子的操作方法是
(4)H转化为M的化学方程式为
(5)B生成F的反应中氧化剂是
您最近一年使用:0次
2022-01-05更新
|
582次组卷
|
2卷引用:新疆疏勒县第一中学等3校2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
6 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。

(1)检验W溶液中金属阳离子所用试剂为_______ (填化学式);
(2)H在潮湿空气中变成M的现象是_______ ,发生反应的化学方程式为_______ ;
(3)A和水反应生成B和C的离子方程式为_______ ;在标准状况下生成11.2 LC气体时,转移电子的个数为_______ NA(用阿伏加德罗常数NA表示);
(4)D中加入盐酸发生反应的离子方程式为_______ 。

(1)检验W溶液中金属阳离子所用试剂为
(2)H在潮湿空气中变成M的现象是
(3)A和水反应生成B和C的离子方程式为
(4)D中加入盐酸发生反应的离子方程式为
您最近一年使用:0次
2022-07-07更新
|
194次组卷
|
2卷引用:新疆第二师八一中学2022-2023学年高三上学期第一次月考化学试题
7 . W为某短周期元素X的固态单质,E气体在标准状况下的密度为1.52g/L,A、B、C均为含X元素的酸式钠盐,它们在一定条件下有如图所示的转化关系,其中某些反应产物中的H2O已略去。
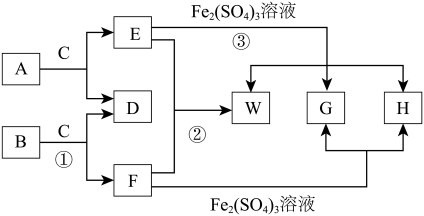
(1)画出X原子的原子结构示意图________ A的电子式可表示为___________ ;
(2)写出反应①的离子反应方程式___________ ;
(3)写出反应②的化学反应方程式_______________________________________ ;
(4)写出反应③的化学反应方程式_______________________________________ ;
(5)医学上常用含有H的糖衣片给患贫血的病人补铁,可检验该药片是否变质的化学试剂为_________ ,对于H来说,药片上糖衣可以起到________ 作用;
(6)有A、B与MgXO4组成的固体混合物中,测得X元素的质量分数为a,则O元素的质量分数为________ 。

(1)画出X原子的原子结构示意图
(2)写出反应①的离子反应方程式
(3)写出反应②的化学反应方程式
(4)写出反应③的化学反应方程式
(5)医学上常用含有H的糖衣片给患贫血的病人补铁,可检验该药片是否变质的化学试剂为
(6)有A、B与MgXO4组成的固体混合物中,测得X元素的质量分数为a,则O元素的质量分数为
您最近一年使用:0次
2020-03-18更新
|
89次组卷
|
2卷引用:新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题
名校
解题方法
8 . 现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。
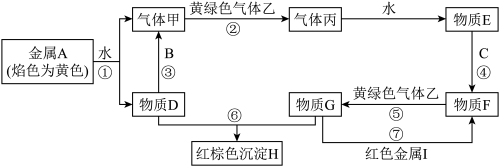
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C__ 、H__ ;
(2)写出反应⑦的离子方程式:__ ;
(3)实验室检验物质G中阳离子的常用试剂是:__ ;实验室检验物质D中阳离子的方法是__ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C
(2)写出反应⑦的离子方程式:
(3)实验室检验物质G中阳离子的常用试剂是:
您最近一年使用:0次
名校
9 . 往 100 g FeCl3 和 CuCl2 的混合溶液中加入铁粉。已知 FeCl3会先与铁粉发生反应:2FeCl3 + Fe =3FeCl2。下图为加入铁粉的质量与反应后剩余固体质量关系。下列说法不正确的是


| A.D 点对应纵坐标为 6.4 |
| B.B 点后溶液的颜色为蓝色 |
| C.该 100 g 溶液中的 CuCl2质量分数为 13.5% |
| D.取 DE 两点间(不含 D)的剩余固体加入盐酸,均有气泡产生 |
您最近一年使用:0次
2017-08-25更新
|
554次组卷
|
8卷引用:新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题
新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题四川省成都市第七中学2017-2018学年高一上学期入学考试化学试题江西省南昌市第十中学2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】南昌十中2019-2020 高一(上)期末河南省许昌市长葛市第一高级中学2019-2020学年高一下学期期末考试化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)第三章 金属及其化合物(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)3.2.3 铁的重要化合物(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)
10 . 实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
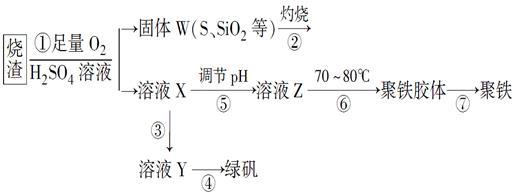
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是________ 。
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为:________ 。
(3)过程③中,需加入的物质是________ 。
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有___________ 。
(5)过程⑤调节pH可选用下列试剂中的________ (填选项序号)。
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70~80℃,目的是___________ 。
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.800 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495 g。若该聚铁主要成分为[Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为________ 。(假设杂质中不含铁元素和硫元素)。

(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为:
(3)过程③中,需加入的物质是
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有
(5)过程⑤调节pH可选用下列试剂中的
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70~80℃,目的是
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.800 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495 g。若该聚铁主要成分为[Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为
您最近一年使用:0次
2016-01-05更新
|
272次组卷
|
2卷引用:新疆乌鲁木齐县柴窝堡林场中学2019届高三第三次模拟考试理科综合化学试题



