名校
1 . 某化学兴趣小组向盛有铜粉的烧杯中加入一定量 溶液,待铜粉完全溶解后,再加入一定量铁粉,充分反应后有固体残余,则下列判断正确的是
溶液,待铜粉完全溶解后,再加入一定量铁粉,充分反应后有固体残余,则下列判断正确的是
 溶液,待铜粉完全溶解后,再加入一定量铁粉,充分反应后有固体残余,则下列判断正确的是
溶液,待铜粉完全溶解后,再加入一定量铁粉,充分反应后有固体残余,则下列判断正确的是| A.残余固体中一定含铜粉,可能含铁粉 |
B.最后所得溶液中一定含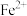 ,可能含 ,可能含 和 和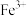 |
C.加入铁粉后可能发生反应的先后顺序依次为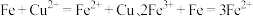 |
D.可向最后所得溶液中滴加酸性 溶液检验是否含有 溶液检验是否含有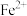 |
您最近一年使用:0次
2024-02-03更新
|
55次组卷
|
2卷引用:山东省名校考试联盟2023-2024学年高一上学期12月阶段测试化学试题
名校
2 . 取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为 ),反应现象有较明显差别的是
),反应现象有较明显差别的是
 ),反应现象有较明显差别的是
),反应现象有较明显差别的是| 选项 | 试剂① | 试剂② |
| Ⅰ |  溶液 溶液 |  的稀溶液 的稀溶液 |
| Ⅱ | 澄清石灰水 |  溶液 溶液 |
| Ⅲ |  的水溶液 的水溶液 | 酸性 溶液 溶液 |
| Ⅳ | KSCN溶液 |  溶液 溶液 |
| A.Ⅰ | B.Ⅱ | C.Ⅲ | D.Ⅳ |
您最近一年使用:0次
名校
3 . 工业上用赤铁矿(主要成分为 ,含
,含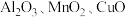 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。
回答下列问题:
(1)试剂a为___________ 。
(2)试剂b需过量,其目的是___________ ;“滤渣”的成分是___________ 。
(3)“结晶”需隔绝空气,原因是___________ 。
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取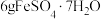 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。 主要成分的化学式为
主要成分的化学式为___________ 。
②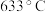 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为___________ ;该样品中 的质量分数为
的质量分数为___________  (保留一位小数)。
(保留一位小数)。
 ,含
,含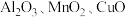 等杂质)制备绿矾
等杂质)制备绿矾 的流程如下:
的流程如下: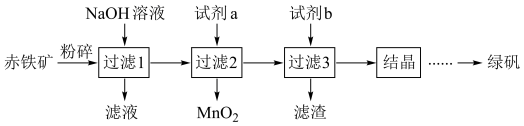
 能与
能与 溶液反应生成可溶性盐
溶液反应生成可溶性盐 。
。回答下列问题:
(1)试剂a为
(2)试剂b需过量,其目的是
(3)“结晶”需隔绝空气,原因是
(4)绿矾隔绝空气加强热可用于制备红色颜料铁红。取
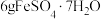 样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体
样品隔绝空气加热(杂质不反应),受热过程中样品质量随温度变化的曲线如图所示(已知固体 不含结晶水)。
不含结晶水)。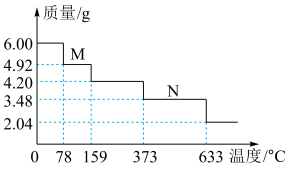
 主要成分的化学式为
主要成分的化学式为②
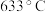 时,除生成铁红外,同时生成能使
时,除生成铁红外,同时生成能使 溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为
溶液变浑浊的气体和使品红溶液裉色的气体。该温度下反应的化学方程式为 的质量分数为
的质量分数为 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
2024-02-02更新
|
258次组卷
|
3卷引用:山东省潍坊市2023-2024学年高一上学期期末考试化学试题
解题方法
4 . 某化学兴趣小组为探究菠菜中铁元素的价态及含量,进行如下实验。回答下列问题:
I.定性检测菠菜中的铁元素

(1)研磨需要的仪器名称为___________ ,操作I的名称为___________ 。
(2)甲同学根据实验现象推测菠菜中不含铁元素。乙同学认为菠菜中铁元素可能以Fe2+形式存在,并对实验进行如下改进:

“溶液褪色”不能证明菠菜中含有Fe2+的原因是___________ ,若“现象I”为___________ ,则可证明菠菜中铁元素以Fe2+存在。
Ⅱ.定量测定菠菜中铁元素含量

(3)沉淀法:取 滤液Ⅱ,加入足量
滤液Ⅱ,加入足量 溶液,生成沉淀,静置一段时间,沉淀颜色逐渐加深,过滤、洗涤、灼烧、冷却、称量、计算。用化学方程式说明沉淀颜色加深的原因是
溶液,生成沉淀,静置一段时间,沉淀颜色逐渐加深,过滤、洗涤、灼烧、冷却、称量、计算。用化学方程式说明沉淀颜色加深的原因是___________ 。
(4)比色法:另取 滤液Ⅱ,加入足量稀硝酸,配制成
滤液Ⅱ,加入足量稀硝酸,配制成 溶液,使用分光光度计测得待测液中
溶液,使用分光光度计测得待测液中 吸光度位于图中
吸光度位于图中 点。
点。

稀 与
与 反应的离子方程式为
反应的离子方程式为_______ ;菠菜中铁元素的含量为________  。
。
I.定性检测菠菜中的铁元素

(1)研磨需要的仪器名称为
(2)甲同学根据实验现象推测菠菜中不含铁元素。乙同学认为菠菜中铁元素可能以Fe2+形式存在,并对实验进行如下改进:

“溶液褪色”不能证明菠菜中含有Fe2+的原因是
Ⅱ.定量测定菠菜中铁元素含量

(3)沉淀法:取
 滤液Ⅱ,加入足量
滤液Ⅱ,加入足量 溶液,生成沉淀,静置一段时间,沉淀颜色逐渐加深,过滤、洗涤、灼烧、冷却、称量、计算。用化学方程式说明沉淀颜色加深的原因是
溶液,生成沉淀,静置一段时间,沉淀颜色逐渐加深,过滤、洗涤、灼烧、冷却、称量、计算。用化学方程式说明沉淀颜色加深的原因是(4)比色法:另取
 滤液Ⅱ,加入足量稀硝酸,配制成
滤液Ⅱ,加入足量稀硝酸,配制成 溶液,使用分光光度计测得待测液中
溶液,使用分光光度计测得待测液中 吸光度位于图中
吸光度位于图中 点。
点。
稀
 与
与 反应的离子方程式为
反应的离子方程式为 。
。
您最近一年使用:0次
5 . 下列由实验现象所得结论正确的是
A.将铁锈溶于浓盐酸,滴入酸性 溶液,紫色褪去,说明铁锈中含二价铁 溶液,紫色褪去,说明铁锈中含二价铁 |
B.向 溶液中加 溶液中加 溶液和稀硝酸,振荡有白色沉淀,说明 溶液和稀硝酸,振荡有白色沉淀,说明 溶液已变质 溶液已变质 |
C.向含 和 和 溶液中加酸化的 溶液中加酸化的 溶液,溶液变红,说明氧化性: 溶液,溶液变红,说明氧化性: |
D.向品红溶液中通入适量 ,品红褪色,说明 ,品红褪色,说明 具有漂白性 具有漂白性 |
您最近一年使用:0次
名校
6 . 氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产CuCl的工艺如图:
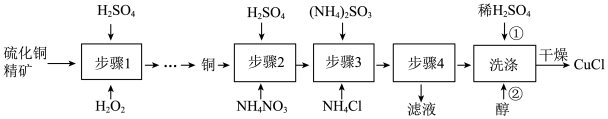
已知:CuCl难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是___________ 。
(2)步骤4进行的实验操作是___________ 。
(3)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是___________ 。用乙醇洗涤的目的是___________ 。
(4)产品纯度测定:称取CuCl产品ag于锥形瓶中,加入足量的酸性Fe2(SO4)3溶液使其充分溶解,然后用0.1000mol/LKMnO4标准溶液滴定Fe2+,消耗KMnO4溶液bmL(本实验中 的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
①CuCl溶于Fe2(SO4)3溶液的离子方程式是___________ 。
②产品中CuCl的质量分数为___________ (列计算式即可)。

已知:CuCl难溶于醇和水,溶于
 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是
(2)步骤4进行的实验操作是
(3)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是
(4)产品纯度测定:称取CuCl产品ag于锥形瓶中,加入足量的酸性Fe2(SO4)3溶液使其充分溶解,然后用0.1000mol/LKMnO4标准溶液滴定Fe2+,消耗KMnO4溶液bmL(本实验中
 的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。①CuCl溶于Fe2(SO4)3溶液的离子方程式是
②产品中CuCl的质量分数为
您最近一年使用:0次
名校
解题方法
7 . 某同学对下列相应反应的离子方程式所作的评价,其中合理的是
| 选项 | 化学反应 | 离子方程式 | 评价 |
| A | 用 溶液检验 溶液检验 的存在 的存在 |  | 正确 |
| B | 向 溶液中加入铜粉 溶液中加入铜粉 |  | 错误,电荷不守恒 |
| C | “84消毒液”(有效成分为 溶液)和“洁厕灵”(有成分为浓盐酸)混合放出氯气 溶液)和“洁厕灵”(有成分为浓盐酸)混合放出氯气 | 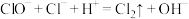 | 正确 |
| D | 等物质的量的 和 和 反应 反应 |  | 错误, 与 与 的物质的量之比与化学式不符 的物质的量之比与化学式不符 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下列反应对应的离子方程式正确的是
| A.Fe2(SO4)3的酸性溶液中通入足量硫化氢:Fe3++H2S=Fe2++S↓+2H+ |
B.碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++2 +2OH-=CaCO3↓+2H2O+ +2OH-=CaCO3↓+2H2O+ |
| C.氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
D.用Na2SO3溶液吸收少量Cl2:3 +Cl2+H2O=2 +Cl2+H2O=2 +2Cl-+ +2Cl-+ |
您最近一年使用:0次
名校
解题方法
9 . 某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取 晶体。(图中夹持及尾气处理装置均已略去)请回答下列问题:
晶体。(图中夹持及尾气处理装置均已略去)请回答下列问题:
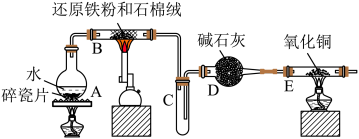
(1)装置 中发生反应的化学方程式是
中发生反应的化学方程式是___________ 。
(2) 中出现的现象是
中出现的现象是___________ 。
(3)该小组把 中反应后的产物加入足量的盐酸,用该溶液制取
中反应后的产物加入足量的盐酸,用该溶液制取 晶体。
晶体。
①欲检验溶液中含有 ,选用的试剂为
,选用的试剂为___________ ,现象是___________ 。
②该实验小组同学用上述试剂没有检测到 ,用离子方程式解释滤液中不存在
,用离子方程式解释滤液中不存在 可能的原因:
可能的原因:___________ 。
③将此滤液中 完全氧化为
完全氧化为 最好选择下列物质中的
最好选择下列物质中的___________ 。
A.酸性 溶液 B.
溶液 B. C.
C. D.
D.
④在③所得溶液浓缩结晶前需要用实验证明 已完全氧化,实验方法是
已完全氧化,实验方法是___________ 。
(4)取少量 于试管中,滴加
于试管中,滴加 溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:___________
______ ______
______ ______
______ ______
______ ,该反应中
,该反应中 表现了
表现了___________ 性(填“氧化”或“还原”)。
 晶体。(图中夹持及尾气处理装置均已略去)请回答下列问题:
晶体。(图中夹持及尾气处理装置均已略去)请回答下列问题:
(1)装置
 中发生反应的化学方程式是
中发生反应的化学方程式是(2)
 中出现的现象是
中出现的现象是(3)该小组把
 中反应后的产物加入足量的盐酸,用该溶液制取
中反应后的产物加入足量的盐酸,用该溶液制取 晶体。
晶体。①欲检验溶液中含有
 ,选用的试剂为
,选用的试剂为②该实验小组同学用上述试剂没有检测到
 ,用离子方程式解释滤液中不存在
,用离子方程式解释滤液中不存在 可能的原因:
可能的原因:③将此滤液中
 完全氧化为
完全氧化为 最好选择下列物质中的
最好选择下列物质中的A.酸性
 溶液 B.
溶液 B. C.
C. D.
D.
④在③所得溶液浓缩结晶前需要用实验证明
 已完全氧化,实验方法是
已完全氧化,实验方法是(4)取少量
 于试管中,滴加
于试管中,滴加 溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:______
 ______
______ ______
______ ______
______ ,该反应中
,该反应中 表现了
表现了
您最近一年使用:0次
名校
解题方法
10 . 硫酸亚铁是一种重要的工业原料,同时也可以用于制造补血药物,但其具有毒性,故严禁在食品中滥用硫酸亚铁,请回答下列问题:
I.
(1)下列说法中正确的是___________(填字母)。
Ⅱ.某同学为探究富含硫酸亚铁且保存时间较长的糕点情况,设计了如下实验方案:

(2)试剂1的名称是___________ 。
(3)加入新制氯水后,溶液红色加深的原因是___________ (用离子方程式表示)。
(4)该同学实验中加入过量新制氯水,放置一段时间后,深红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
①【提出假设】
假设1:溶液中的+3价铁被氧化为更高的价态。
假设2:___________ 。
②【设计方案】
为了对假设2进行验证,简述你的设计方案:___________ 。
(5)将铜片放入0.1mol/LFeCl3溶液中浸泡,一段时间,溶液中c(Fe3+):c(Fe2+)=2:3,则此时Cu2+与Fe3+的物质的量之比为___________ 。
I.
(1)下列说法中正确的是___________(填字母)。
| A.向FeSO4溶液中加入铜粉可以析出铁单质 |
| B.大量服用FeSO4导致人体中毒可能与其氧化性有关 |
| C.FeSO4可以使酸性KMnO4溶液褪色 |
| D.FeSO4需密封保存主要原因是硫酸亚铁有毒 |
Ⅱ.某同学为探究富含硫酸亚铁且保存时间较长的糕点情况,设计了如下实验方案:

(2)试剂1的名称是
(3)加入新制氯水后,溶液红色加深的原因是
(4)该同学实验中加入过量新制氯水,放置一段时间后,深红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
①【提出假设】
假设1:溶液中的+3价铁被氧化为更高的价态。
假设2:
②【设计方案】
为了对假设2进行验证,简述你的设计方案:
(5)将铜片放入0.1mol/LFeCl3溶液中浸泡,一段时间,溶液中c(Fe3+):c(Fe2+)=2:3,则此时Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次



