名校
解题方法
1 . 下列离子组在指定条件下能大量共存的是
A.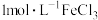 溶液中: 溶液中: 、 、 、 、 、 、 |
B.使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.久置氯水中: 、 、 、 、 、 、 |
D.加入铝粉有气体生成的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
2 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
504次组卷
|
5卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
3 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-04-19更新
|
290次组卷
|
2卷引用:吉林省长春市第五中学2023-2024学年高一下学期第一学程考试化学试题
4 . 为完成相应实验目的,下列方案设计、现象和结论均正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究铁粉在 中燃烧所得固体粉末的成分 中燃烧所得固体粉末的成分 | 取少量固体粉末,加入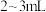 蒸馏水,振荡,迅速滴入几滴 蒸馏水,振荡,迅速滴入几滴 溶液 溶液 | 溶液不显红色,说明该固体粉末中不存在 |
| B | 探究 和 和 的酸性强弱 的酸性强弱 | 将 气体通入 气体通入 溶液中 溶液中 | 产生白色沉淀,说明酸性: |
| C | 探究温度对化学平衡的影响 | 加热盛有 溶液的试管 溶液的试管 | 加热,溶液变为黄色,冷却后变为蓝色,说明 转化为 转化为 的反应为吸热反应 的反应为吸热反应 |
| D | 检验溴乙烷中含溴元素 | 加热溴乙烷与 的混合液,然后滴加 的混合液,然后滴加 溶液 溶液 | 有沉淀生成,说明溴乙烷中含溴元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 无水三氯化铁是有机合成的催化剂,为棕黄色固体,易潮解产生白雾,300℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,下图是甲组学生设计的制备装置。
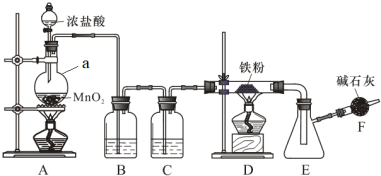
回答下列问题:
(1)仪器a的名称是___________ ;a中反应的离子方程式为___________ 。
(2)装置B的作用是___________ ,C中盛装试剂是___________ 。
(3)当出现什么现象时点燃装置D处酒精灯___________ 。装置D与E之间用粗导管连接,原因是___________ ;
(4)装置F的作用是___________ 。
(5)称取2.8 g该铁屑,最终制得无水三氯化铁6.5 g,则该反应的产率为___________ 。
(6)与甲组设计对比,乙组同学去掉了装置C.实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是___________ 。
(7)已知氧化性: ,请设计简单实验证明该结论
,请设计简单实验证明该结论___________ 。

回答下列问题:
(1)仪器a的名称是
(2)装置B的作用是
(3)当出现什么现象时点燃装置D处酒精灯
(4)装置F的作用是
(5)称取2.8 g该铁屑,最终制得无水三氯化铁6.5 g,则该反应的产率为
(6)与甲组设计对比,乙组同学去掉了装置C.实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是
(7)已知氧化性:
 ,请设计简单实验证明该结论
,请设计简单实验证明该结论
您最近一年使用:0次
2024-03-02更新
|
123次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题
名校
6 . 下列反应的离子方程式正确的是
A.向 溶液中通入 溶液中通入 气体: 气体: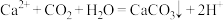 |
B.向氯化铁溶液中滴入过量的 溶液: 溶液: |
C. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: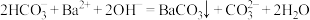 |
D.向大理石中滴加稀醋酸: |
您最近一年使用:0次
名校
解题方法
7 . 实验室用 还原
还原 (沸点:31.85℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是
(沸点:31.85℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是

 还原
还原 (沸点:31.85℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是
(沸点:31.85℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是
| A.装置Ⅱ、Ⅲ中依次盛装的是浓硫酸、冰水 |
| B.实验时,应先加热管式炉,再打开活塞K |
| C.为鉴定制得硅中是否含有微量铁单质,需要用到的试剂为盐酸、双氧水、KSCN溶液 |
D.该实验中制备氢气的装置也可用于硫酸与 反应制备 反应制备 |
您最近一年使用:0次
2024-02-10更新
|
404次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期4月月考化学试题
名校
8 . 某溶液X中仅可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
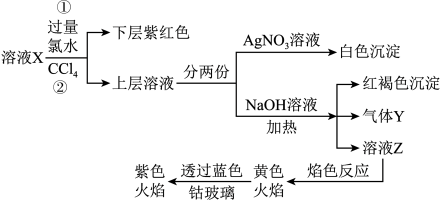
、 中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是(已知:
中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是(已知: 不能与
不能与 、
、 共存)
共存)
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是(已知:
中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是(已知: 不能与
不能与 、
、 共存)
共存)
A.该溶液X中可能有 、 、 |
B.为了确认溶液X中是否含有 ,还需要取溶液滴加 ,还需要取溶液滴加 观察现象 观察现象 |
| C.该溶液可能由是硫酸亚铁、碘化钾和氯化铵溶于水后得到的 |
D.如果气体Y能使石蕊试液变红,说明溶液中一定含有 |
您最近一年使用:0次
2024-02-08更新
|
367次组卷
|
4卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题吉林省长春市东北师范大学附属中学2023-2024学年高一上学期期末化学试题山东省济宁市育才中学2023-2024学年高一下学期开学化学试题(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
9 . 高铁酸钠( )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
①湿法制备:___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)
②干法制备: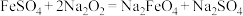
(1) 中Fe元素的化合价为
中Fe元素的化合价为___________ ,其在水溶液中的电离方程式为___________ 。
(2) 的电子式为
的电子式为___________ ,其与 反应的化学方程式为
反应的化学方程式为___________ 。
(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目___________ 。该反应每生成1 mol  ,转移的电子数为
,转移的电子数为___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:
___________  (选填“<”或“>”)。
(选填“<”或“>”)。
(5) 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂___________ 检验。 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是___________ 。
 )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:①湿法制备:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)②干法制备:
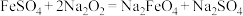
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)
 的电子式为
的电子式为 反应的化学方程式为
反应的化学方程式为(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目
 ,转移的电子数为
,转移的电子数为___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:

 (选填“<”或“>”)。
(选填“<”或“>”)。(5)
 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是
您最近一年使用:0次
2024-02-07更新
|
122次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题
10 . 硒是人体微量元素中的“胰岛素”。含硒废料(主要含Se、S、Fe2O3、ZnO、CuO、SiO2等)制取硒的流程如图,下列有关说法正确的是


| A.“分离”时得到含硫煤油的操作方法是分液 |
| B.“酸溶”后,滤渣是Se |
| C.“酸化”时,生成1mol Se,反应转移2mol电子 |
| D.若向“酸溶”所得的滤液中滴加硫氰化钾溶液,溶液不变红 |
您最近一年使用:0次
2024-01-17更新
|
340次组卷
|
3卷引用:吉林省吉林市2023-2024学年高三上学期第二次模拟考试 化学试题



