名校
解题方法
1 . 铁元素在地壳中含量居于第四位。铁是目前产量最大,使用最广泛的金属。铁及其化合物在日常生产生活中有着广泛应用。
Ⅰ.铁是人体必需的微量元素之一,当人体贫血时,可以服用含 的补血剂,补铁剂中的
的补血剂,补铁剂中的 在空气中很容易被氧化为
在空气中很容易被氧化为 ,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂搭配维C一起服用效果更好。
,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂搭配维C一起服用效果更好。
[实验操作]第一步:在A、B两支试管中加入对比试剂;
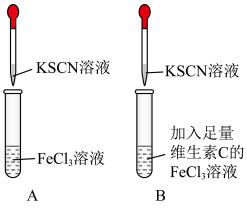
第二步:振荡;
第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变___________ 色,B试管中无明显现象。
[实验结论]
(2)维生素C具有___________ (填“氧化性”或“还原性”),能防止 被氧化为
被氧化为 ,所以补铁剂和维生素C一起服用具有科学依据。
,所以补铁剂和维生素C一起服用具有科学依据。
[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和 ,放入水中立即产生大量气泡(
,放入水中立即产生大量气泡( )使口感更好,说明维生素C具有
)使口感更好,说明维生素C具有___________ (填“酸性”或“碱性”)。
(4)由以上信息可知,为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意___________ (写一条即可)。
Ⅱ.在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,原因是:在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知: 中Fe的化合价为
中Fe的化合价为 价、
价、 价)。
价)。
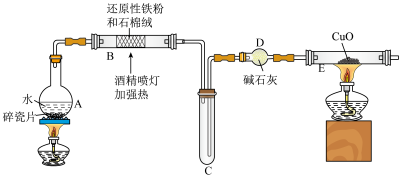
(5)装置B中发生反应的化学方程式为___________ 。
(6)装置C中导管“短进长出”的原因___________ 。
(7)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液若没有出现红色,原因是___________ (用离子方程式表示)。
Ⅰ.铁是人体必需的微量元素之一,当人体贫血时,可以服用含
 的补血剂,补铁剂中的
的补血剂,补铁剂中的 在空气中很容易被氧化为
在空气中很容易被氧化为 ,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂搭配维C一起服用效果更好。
,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂搭配维C一起服用效果更好。[实验操作]第一步:在A、B两支试管中加入对比试剂;

第二步:振荡;
第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变
[实验结论]
(2)维生素C具有
 被氧化为
被氧化为 ,所以补铁剂和维生素C一起服用具有科学依据。
,所以补铁剂和维生素C一起服用具有科学依据。[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和
 ,放入水中立即产生大量气泡(
,放入水中立即产生大量气泡( )使口感更好,说明维生素C具有
)使口感更好,说明维生素C具有(4)由以上信息可知,为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意
Ⅱ.在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,原因是:在高温下,Fe与水蒸气可发生反应。现设计如下装置完成高温下“Fe与水蒸气反应”的实验,并检验其产物(已知:
 中Fe的化合价为
中Fe的化合价为 价、
价、 价)。
价)。
(5)装置B中发生反应的化学方程式为
(6)装置C中导管“短进长出”的原因
(7)取反应后得到的黑色粉末放入一试管中,加入稀硫酸将固体溶解,再滴加几滴KSCN溶液,振荡,溶液若没有出现红色,原因是
您最近一年使用:0次
名校
2 . 下列各组实验所得结论不正确的是
| 实验现象 | 结论 | |
| A | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加 溶液,溶液未出现红色 溶液,溶液未出现红色 | 样品中没有+3价铁 |
| B | 加热 溶液,溶液变黄绿色 溶液,溶液变黄绿色 | 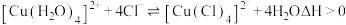 |
| C | 将 溶液和稀 溶液和稀 混合,出现淡黄色沉淀和可使品红溶液褪色的气体 混合,出现淡黄色沉淀和可使品红溶液褪色的气体 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向苯酚浊液中加入 溶液变澄清 溶液变澄清 | 酸性:苯酚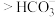 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 化学与生产、生活密切相关。下列有关物质的性质与用途对应关系错误的是
| A.FeCl3溶液具有酸性,可用于蚀刻铜制品 |
| B.过氧乙酸具有强氧化性,可用于杀菌消毒 |
| C.甘油具有吸水性,可用作化妆品的保湿剂 |
| D.Na具有还原性,可用于高温下与TiCl4反应制备Ti |
您最近一年使用:0次
2021-03-03更新
|
452次组卷
|
5卷引用:吉林省松原市实验高级中学2020-2021学年高三下学期第三次摸底测试化学试题
吉林省松原市实验高级中学2020-2021学年高三下学期第三次摸底测试化学试题江苏省常州市2021届高三下学期期初调研考试化学试题河北省张家口市宣化第一中学2021届高三下学期阶段模拟(五)化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题1-5)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(选择题1-5)
14-15高一上·吉林长春·期末
名校
解题方法
4 . 为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符合实验要求且完全正确的是( )
| 实验操作 | 实验现象 | 离子反应 | 实验结论 | |
| A | 在氯化亚铁溶液中通入氯气 | 浅绿色溶液变成棕黄色溶液 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| B | 在氯化亚铁溶液中加入锌片 | 浅绿色溶液变成无色溶液 | Fe2++Zn=Fe+Zn2+ | Zn具有还原性 |
| C | 在氯化铁溶液中加入铁粉 | 棕黄色溶液变成浅绿色溶液 | Fe3++Fe=2Fe2+ | 铁单质具有还原性 |
| D | 在氯化铁溶液中加入铜粉 | 蓝色溶液变成棕黄色溶液 | 2Fe3++Cu=2Fe2++Cu2+ | Fe3+具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2014-01-14更新
|
879次组卷
|
7卷引用:2013-2014学年吉林省长春外国语学校高一上学期期末理科化学试卷
(已下线)2013-2014学年吉林省长春外国语学校高一上学期期末理科化学试卷(已下线)2014吉林省长春外国语学校高一上学期期末化学(理)试卷 吉林省白城市洮南市第一中学2020-2021学年高一上学期第三次月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【押题专练】黑龙江省牡丹江市2020-2021学年高一上学期期末考试化学试题黑龙江省哈尔滨市第六中学校2022—2023学年高一上学期期中考试化学试题青海省西宁市海湖中学2021-2022学年高三上学期期中考试化学试题
名校
5 . 某同学为了检验一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在一支试管中滴入酸性高锰酸钾溶液,在另一支试管中滴入KSCN溶液.据此回答下列相关问题:
(1)将药品研细的目的是______________________
(2)过滤所用到的玻璃仪器除烧杯外还有________________________
(3)若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液变红,结论是________ .
(4)已知高锰酸钾在酸性溶液中的还原产物为Mn2+,写出酸性高锰酸钾溶液褪色的离子方程式____
(1)将药品研细的目的是
(2)过滤所用到的玻璃仪器除烧杯外还有
(3)若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液变红,结论是
(4)已知高锰酸钾在酸性溶液中的还原产物为Mn2+,写出酸性高锰酸钾溶液褪色的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 无水三氯化铁是有机合成的催化剂,为棕黄色固体,易潮解产生白雾,300℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,下图是甲组学生设计的制备装置。
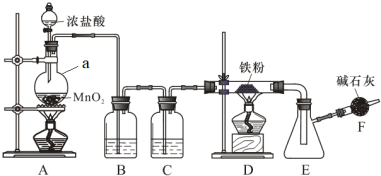
回答下列问题:
(1)仪器a的名称是___________ ;a中反应的离子方程式为___________ 。
(2)装置B的作用是___________ ,C中盛装试剂是___________ 。
(3)当出现什么现象时点燃装置D处酒精灯___________ 。装置D与E之间用粗导管连接,原因是___________ ;
(4)装置F的作用是___________ 。
(5)称取2.8 g该铁屑,最终制得无水三氯化铁6.5 g,则该反应的产率为___________ 。
(6)与甲组设计对比,乙组同学去掉了装置C.实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是___________ 。
(7)已知氧化性: ,请设计简单实验证明该结论
,请设计简单实验证明该结论___________ 。

回答下列问题:
(1)仪器a的名称是
(2)装置B的作用是
(3)当出现什么现象时点燃装置D处酒精灯
(4)装置F的作用是
(5)称取2.8 g该铁屑,最终制得无水三氯化铁6.5 g,则该反应的产率为
(6)与甲组设计对比,乙组同学去掉了装置C.实验时无论怎样改变铁粉的用量,装置D中都有少量的黑色固体残留。乙组同学猜测该黑色固体可能是
(7)已知氧化性:
 ,请设计简单实验证明该结论
,请设计简单实验证明该结论
您最近一年使用:0次
2024-03-02更新
|
138次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题
名校
7 . 已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法错误 的是
 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法| A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器 |
B.乙组实验中 将 将 氧化为 氧化为 |
C.丙组实验发生反应的离子方程式: |
D.丁组实验说明还原性: |
您最近一年使用:0次
7日内更新
|
170次组卷
|
4卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
名校
解题方法
8 . 正三价铁元素有一定的氧化性,FeCl3溶液吸收 一定量SO2后溶液颜色发生变化。
(1)反应的离子方程式为_______ 。
(2)除H+、OH-、H2O外,上述反应后的溶液中一定含有的粒子有_______(填编号)。
(3)对还不能确定的粒子存在情况提出合理的假设:
假设1:只存在Fe3+;
假设2:只存在_______ ;
假设3:_______ 。
(4)设计实验方案进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂: 3mol·L-1 H2SO4、l mol·L-1 NaOH、0.01 mol·L-1 KMnO4、20%KSCN、3%H2O2、淀粉- KI溶液、紫色石蕊试液、品红溶液。
(1)反应的离子方程式为
(2)除H+、OH-、H2O外,上述反应后的溶液中一定含有的粒子有_______(填编号)。
| A.Fe2+ | B.Fe3+ | C.Cl- | D.SO | E.H2SO3 |
假设1:只存在Fe3+;
假设2:只存在
假设3:
(4)设计实验方案进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂: 3mol·L-1 H2SO4、l mol·L-1 NaOH、0.01 mol·L-1 KMnO4、20%KSCN、3%H2O2、淀粉- KI溶液、紫色石蕊试液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
您最近一年使用:0次
2021-08-03更新
|
184次组卷
|
2卷引用:吉林省长春市第二实验中学2022-2023学年高一下学期4月月考化学试题
9 . FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。
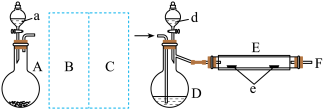
请回答:
(1)若在A中盛固体CaCO3,a中盛6mol/L盐酸,B处是装有饱和NaHCO3溶液的洗气瓶为使导入D中的CO2为干燥纯净的气体,则图中C处的装置和其中的试剂应是:________ ,为防止污染空气,实验时应在F处连接盛________ 的尾气吸收装置。
(2)反应过程中要不断通入CO2,其主要作用有两个:①是利用CO2把反应器中空气赶尽;②是________ .
Ⅱ.探究FeBr2的还原性
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是________ 。
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
设计实验证明假设2是正确的_______________________________
(3)实验证明:还原性Fe2+ > Br-请用一个离子方程式来证明:_____________ ;
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:____________ 。
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。

请回答:
(1)若在A中盛固体CaCO3,a中盛6mol/L盐酸,B处是装有饱和NaHCO3溶液的洗气瓶为使导入D中的CO2为干燥纯净的气体,则图中C处的装置和其中的试剂应是:
(2)反应过程中要不断通入CO2,其主要作用有两个:①是利用CO2把反应器中空气赶尽;②是
Ⅱ.探究FeBr2的还原性
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
设计实验证明假设2是正确的
(3)实验证明:还原性Fe2+ > Br-请用一个离子方程式来证明:
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:
您最近一年使用:0次
2019-10-08更新
|
147次组卷
|
3卷引用:吉林省公主岭市范家屯镇第一中学2020届高三上学期第二次月考化学试题
名校
10 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 比较S与C的非金属性强弱 | 用pH试纸分别测定1 mol/LNa2CO3溶液和1 mol/LNa2SO3溶液的pH | 前者的试纸颜色比后者深,说明非金属性:S>C |
| B | 探究Ag+与Fe3+氧化性的强弱 | 向Fe(NO3)2和KSCN的混合溶液中滴入酸化的AgNO3溶液 | 溶液变红,说明氧化性Ag+>Fe3+ |
| C | 证明溴乙烷与NaOH的乙醇溶液发生消去反应 | 将溴乙烷与NaOH的乙醇溶液共热产生的气体通入酸性KMnO4溶液中 | 溶液褪色,说明发生了消去反应 |
| D | 探究KI与FeCl3 反应的限度 | 取5 mL0.1 mol/LKI溶液于试管中,加入1 mL0.1 mol/LFeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 溶液变红,则KI与FeCl3的反应 有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



