解题方法
1 . 下列“推理或结论”与“实验操作及现象”相符的一组是
| 选项 | 实验操作及现象 | 推理或结论 |
| A | 向某固体中加入稀盐酸,产生气泡 | 该固体一定是碳酸盐 |
| B | 向 溶液中加入淀粉碘化钾溶液,溶液变蓝 溶液中加入淀粉碘化钾溶液,溶液变蓝 | 氧化性 |
| C | 用铂丝蘸取某溶液在火焰上灼烧,火焰的颜色为黄色 | 该溶液是 溶液 溶液 |
| D | 向某溶液中通入 ,再加入 ,再加入 溶液,溶液变红 溶液,溶液变红 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
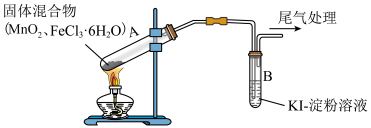
2 . 氯气是一种常用的氧化剂,其制取方法是重要的科研项目。通过下列装置探究 与
与 能否反应产生
能否反应产生 。
。 会产生氯化氢,
会产生氯化氢, 会升华为气体。实验记录:
会升华为气体。实验记录:
(1)实验室常用 和浓盐酸制备
和浓盐酸制备 ,反应的化学方程式为
,反应的化学方程式为___________ 。
(2)上述实验中可用___________ (填化学式)溶液进行尾气吸收。
(3)“黄色气体”中可能含有氧化性物质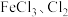 ,均能氧化
,均能氧化 。确认“黄色气体”中含有
。确认“黄色气体”中含有 的实验操作及现象是
的实验操作及现象是___________ 。
(4)为验证“黄色气体”中有 的存在,进行以下两种改进实验。
的存在,进行以下两种改进实验。
①方案1中添加“饱和 溶液”的目的是
溶液”的目的是___________ 。
②方案2中将 -淀粉溶液用
-淀粉溶液用 代替,是因为
代替,是因为 的氧化性强弱顺序为
的氧化性强弱顺序为___________ ,写出方案2试管B中发生反应的离子方程式___________ 。
 与
与 能否反应产生
能否反应产生 。
。
 会产生氯化氢,
会产生氯化氢, 会升华为气体。实验记录:
会升华为气体。实验记录:| 实验操作 | 实验现象 |
| 点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
(1)实验室常用
 和浓盐酸制备
和浓盐酸制备 ,反应的化学方程式为
,反应的化学方程式为(2)上述实验中可用
(3)“黄色气体”中可能含有氧化性物质
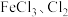 ,均能氧化
,均能氧化 。确认“黄色气体”中含有
。确认“黄色气体”中含有 的实验操作及现象是
的实验操作及现象是(4)为验证“黄色气体”中有
 的存在,进行以下两种改进实验。
的存在,进行以下两种改进实验。| 实验改进操作 | 实验现象 | |
| 方案1 | 在A、B间增加盛有饱和 溶液的洗气瓶C 溶液的洗气瓶C | B中溶液变为蓝色 |
| 方案2 | 将B中 -淀粉溶液替换为 -淀粉溶液替换为 溶液 溶液 | B中溶液呈浅橙红色 |
 溶液”的目的是
溶液”的目的是②方案2中将
 -淀粉溶液用
-淀粉溶液用 代替,是因为
代替,是因为 的氧化性强弱顺序为
的氧化性强弱顺序为
您最近一年使用:0次
3 . 金属A与其它物质之间的转化关系如下图所示。_______ 、_______ 。
(2)要检验G中的金属阳离子的实验操作、现象及结论是_______ 。
(3)流程中白色沉淀变成红褐色沉淀的化学方程式为_______ 。
(4)G溶液与金属A反应的离子方程式为_______ 。
(5)实验室配制500mL 的ASO4溶液。
的ASO4溶液。
①需要用到的主要玻璃仪器有烧杯、量筒、胶头滴管和_______ 、_______ 。
②需要称取_______ g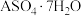 晶体。
晶体。
③实验小组的同学发现所配制的溶液放置一天后产生了黄色固体,于是他们分离出黄色固体,配制成溶液,经多次实验证明黄色固体中含有Fe3+和 ,检验溶液中
,检验溶液中 所用的试剂为
所用的试剂为_______ 。
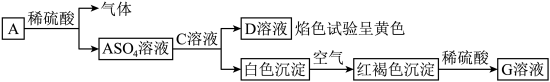
(2)要检验G中的金属阳离子的实验操作、现象及结论是
(3)流程中白色沉淀变成红褐色沉淀的化学方程式为
(4)G溶液与金属A反应的离子方程式为
(5)实验室配制500mL
 的ASO4溶液。
的ASO4溶液。①需要用到的主要玻璃仪器有烧杯、量筒、胶头滴管和
②需要称取
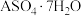 晶体。
晶体。③实验小组的同学发现所配制的溶液放置一天后产生了黄色固体,于是他们分离出黄色固体,配制成溶液,经多次实验证明黄色固体中含有Fe3+和
 ,检验溶液中
,检验溶液中 所用的试剂为
所用的试剂为
您最近一年使用:0次
4 . 工厂以镍废渣(主要成分为Ni含少量Fe、Pb、Fe3O4、Al2O3和不溶性杂质等)为原料制备翠矾(NiSO4•7H2O),其生产工艺如图:
(1)“碱浸”时Al2O3发生反应的化学方程式为_______ 。
(2)“转化”过程中加入H2O2的目的是_______ ,该过程用离子方程式表示为 _______ 。
(3)设计实验方案确认“滤液B”中的杂质离子已经被完全除去:_______ 。
(4)“操作1”的具体操作是控制pH、蒸发浓缩、冷却结晶、_______ 、_______ 、干燥。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出NiOOH。写出该反应的离子方程式_______ 。
(6)Pb3O4在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为_______ 。
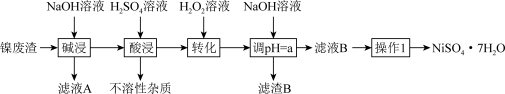
(1)“碱浸”时Al2O3发生反应的化学方程式为
(2)“转化”过程中加入H2O2的目的是
(3)设计实验方案确认“滤液B”中的杂质离子已经被完全除去:
(4)“操作1”的具体操作是控制pH、蒸发浓缩、冷却结晶、
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出NiOOH。写出该反应的离子方程式
(6)Pb3O4在涂料工业中用作防锈颜料,Pb3O4中+2价铅和+4价铅的原子个数之比为
您最近一年使用:0次
解题方法
5 . 部分含铁物质的分类与相应化合价的关系如图所示。下列说法错误的是
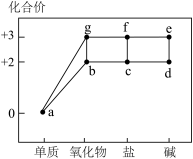
| A.b、g均是碱性氧化物化合价 | B.d→e→f→c可以实现一步转化 |
| C.纯净的d为白色固体 | D.c溶液常用于刻蚀印刷电路板的铜箔 |
您最近一年使用:0次
解题方法
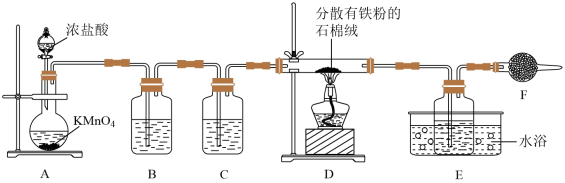
6 . FeCl3是重要的化工产品,主要用作水处理剂,还用作媒染剂、催化剂等,某小组设计如图实验装置制备氯化铁并探究其性质。
①A中发生反应的生成物有KCl、MnCl2、Cl2和H2O。
②FeCl3易升华,遇水蒸气易潮解。
③石棉绒是一种耐火材料,不参与反应。
(1)A中反应的离子方程式为______ ,D中石棉绒的作用是______ 。
(2)E采用的是______ (填“热”或“冷”)水浴,目的是______ 。
(3)F的作用为______ 。
(4)取适量FeCl3溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈______ 色;往FeCl3溶液中加入适量铜粉,发生反应的化学方程式为______ 。
①A中发生反应的生成物有KCl、MnCl2、Cl2和H2O。
②FeCl3易升华,遇水蒸气易潮解。
③石棉绒是一种耐火材料,不参与反应。
(1)A中反应的离子方程式为
(2)E采用的是
(3)F的作用为
(4)取适量FeCl3溶液于试管中,加入几滴硫氰化钾溶液,试管内溶液呈
您最近一年使用:0次
名校
解题方法
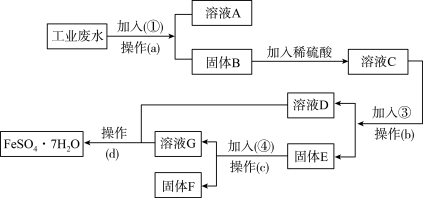
7 . 某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。_______ 。
(2)加入的试剂④为_______ 。
(3)鉴别溶液D中的金属阳离子时,应加入的试剂依次是_______ ,现象依次是_______ ;请写出鉴别过程中属于氧化还原反应的离子方程式:_______ 。
(4)若取2ml溶液D加入试管中,然后滴加氢氧化钠溶液,产生的现象是_______ ;此现象涉及氧化还原反应的化学方程式是_______ 。
(2)加入的试剂④为
(3)鉴别溶液D中的金属阳离子时,应加入的试剂依次是
(4)若取2ml溶液D加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
8 . 下列有关金属及其化合物的说法正确的是
| A.FeSO4溶液若变质,可加入Cu复原 |
| B.FeO不稳定,在空气中受热迅速转化为Fe2O3 |
| C.金属元素在自然界中都以化合态形式存在 |
| D.将mg组成不同的铝钠合金分别投入足量盐酸中,铝的质量分数越大,放出H2越多 |
您最近一年使用:0次
解题方法
9 . 铁是人体必需的微量元素,可通过化学实验的方法检验食品中的铁元素。通过挤压成熟南果梨获得液体并将其过滤,得到无色透明果汁,甲、乙、丙三名同学利用南果梨汁做了检验南果梨中铁元素的探究实验,已知南果梨中维生素 (具有还原性)、可溶性糖等含量均高于其他普通水果。下列说法正确的是
(具有还原性)、可溶性糖等含量均高于其他普通水果。下列说法正确的是
 (具有还原性)、可溶性糖等含量均高于其他普通水果。下列说法正确的是
(具有还原性)、可溶性糖等含量均高于其他普通水果。下列说法正确的是A.甲同学向南果梨汁中加入适量 溶液,无明显现象,可以证明南果梨不含铁元素 溶液,无明显现象,可以证明南果梨不含铁元素 |
| B.乙同学向高锰酸钾溶液中滴加少量南果梨汁,高锰酸钾溶液褪色,可以证明南果梨汁中含有二价铁 |
C.丙同学向南果梨汁中滴加几滴稀硝酸(具有氧化性),再滴加几滴 溶液,梨汁变红,可以证明在该过程中实现了二价铁到三价铁的转化。 溶液,梨汁变红,可以证明在该过程中实现了二价铁到三价铁的转化。 |
| D.若南果梨中存在铁元素,其可能以二价铁的形式存在 |
您最近一年使用:0次
10 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
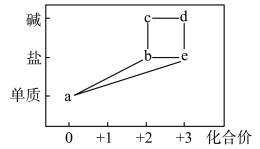
| A.b既可被氧化,也可被还原 |
| B.可将e加入浓碱液中制得d的胶体 |
| C.d受热失水后的产物可用作橡胶的颜料 |
| D.可存在b→c→d→e→b的循环转化关系 |
您最近一年使用:0次



