名校
解题方法
1 . 茶是中国人喜爱的一种饮品,茶叶中含有铁元素,可以用以下实验操作检验茶叶中的铁元素:A.取少量茶叶;B.检验滤液中的 Fe3+;C.过滤得到滤液;D.将茶叶灼烧为茶叶灰;E.用足量稀盐酸溶解茶叶灰,并加蒸馏水稀释;请回答下列问题。
(1)上述实验操作的正确顺序是___________ (填字母)。
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、___________ 。
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式___________ 。
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式___________ 。
(1)上述实验操作的正确顺序是
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式
您最近一年使用:0次
2 . 检验下列物质所选用的试剂正确的是
| 选项 | 待检验物质 | 所用试剂 |
| A | 溶液中的 |  溶液 溶液 |
| B |  气体 气体 | 澄清石灰水 |
| C | 溶液中的 |  溶液 溶液 |
| D | 溶液中的 |  溶液,湿润的蓝色石蕊试纸 溶液,湿润的蓝色石蕊试纸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 在无色透明的溶液中,可以大量共存的离子组是
A.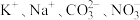 | B. |
C. | D. |
您最近一年使用:0次
名校
4 . 软锰矿浆(主要成分 )可吸收烟气中的
)可吸收烟气中的 ,同时可制备
,同时可制备 ,工艺流程如下:
,工艺流程如下: 后的软锰矿浆中含有
后的软锰矿浆中含有 等阳离子:
等阳离子:
②金属离子沉淀的 如下表
如下表
(1)脱硫的产物是 ,软锰矿中
,软锰矿中 所起的作用是
所起的作用是___________ 。
(2)过程1向浆液中通入 的目的是
的目的是___________ 。
(3)滤渣1的成分是___________ ,过程2中发生反应的离子方程式为___________ 。
(4)写出制备 时发生反应的离子方程式
时发生反应的离子方程式___________ 。
(5)取 碳酸锰样品,加适量硫酸加热溶解后,用
碳酸锰样品,加适量硫酸加热溶解后,用 的
的 溶液测定,至反应完全时,消耗
溶液测定,至反应完全时,消耗 溶液的体积为
溶液的体积为 。 (已知:反应产物为
。 (已知:反应产物为 ,杂质不参与反应)
,杂质不参与反应)
样品中 质量分数的计算式为
质量分数的计算式为___________  。
。
 )可吸收烟气中的
)可吸收烟气中的 ,同时可制备
,同时可制备 ,工艺流程如下:
,工艺流程如下:
 后的软锰矿浆中含有
后的软锰矿浆中含有 等阳离子:
等阳离子:②金属离子沉淀的
 如下表
如下表| 金属离子 |  |  |  |  |  |
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 6.2 |
沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 8.2 |
(1)脱硫的产物是
 ,软锰矿中
,软锰矿中 所起的作用是
所起的作用是(2)过程1向浆液中通入
 的目的是
的目的是(3)滤渣1的成分是
(4)写出制备
 时发生反应的离子方程式
时发生反应的离子方程式(5)取
 碳酸锰样品,加适量硫酸加热溶解后,用
碳酸锰样品,加适量硫酸加热溶解后,用 的
的 溶液测定,至反应完全时,消耗
溶液测定,至反应完全时,消耗 溶液的体积为
溶液的体积为 。 (已知:反应产物为
。 (已知:反应产物为 ,杂质不参与反应)
,杂质不参与反应)样品中
 质量分数的计算式为
质量分数的计算式为 。
。
您最近一年使用:0次
名校
5 . 为了检验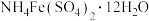 晶体中的离子,下列实验操作及结论正确的是
晶体中的离子,下列实验操作及结论正确的是
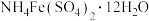 晶体中的离子,下列实验操作及结论正确的是
晶体中的离子,下列实验操作及结论正确的是A.取少量样品放入试管中,加入 溶液,将湿润的红色石蕊试纸粘在试管口,试纸变蓝,证明晶体中含有 溶液,将湿润的红色石蕊试纸粘在试管口,试纸变蓝,证明晶体中含有 |
B.取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴 溶液,溶液变为红色,证明晶体中含有 溶液,溶液变为红色,证明晶体中含有 |
C.取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴 溶液,有白色沉淀生成,证明晶体中含有 溶液,有白色沉淀生成,证明晶体中含有 |
D.取少量样品溶于水,滴加 溶液,溶液变红,证明晶体中含有 溶液,溶液变红,证明晶体中含有 |
您最近一年使用:0次
名校
6 . “水写红字”魔术原理如图所示,其中的纸张需经某溶液浸泡、干燥后使用,该溶液是
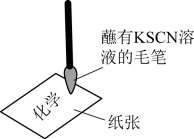
| A.NaCl溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
7日内更新
|
110次组卷
|
2卷引用:湖南省岳阳市平江县第三中学等多校联考2023年高一普通高中学业水平合格性考试仿真模拟(专家卷一)化学试题
解题方法
7 . 一种以黄铁矿烧渣(主要成分为 等)为原料制取硫酸铁晶体的工艺流程如下:(已知:
等)为原料制取硫酸铁晶体的工艺流程如下:(已知: 不溶于水,不和硫酸反应。)
不溶于水,不和硫酸反应。)_____ 。
(2)已知:25.0%硫酸的密度 ,则25.0%硫酸的物质的量浓度为
,则25.0%硫酸的物质的量浓度为______ ;若实验室用 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为_____  。
。
(3)写出“酸浸”中氧化铁与酸反应的离子方程式______ ,“酸浸”后过滤所得滤液中所含的阳离子有_______ (填离子符号)。
(4)“氧化”过程发生反应的离子方程式为_______ ;“氧化”时可用硝酸代替 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是_______ 。
(5)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为______ 、过滤洗涤、烘干。
 等)为原料制取硫酸铁晶体的工艺流程如下:(已知:
等)为原料制取硫酸铁晶体的工艺流程如下:(已知: 不溶于水,不和硫酸反应。)
不溶于水,不和硫酸反应。)
(2)已知:25.0%硫酸的密度
 ,则25.0%硫酸的物质的量浓度为
,则25.0%硫酸的物质的量浓度为 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为 。
。(3)写出“酸浸”中氧化铁与酸反应的离子方程式
(4)“氧化”过程发生反应的离子方程式为
 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是(5)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为
您最近一年使用:0次
名校
8 . 柠檬酸亚铁(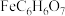 ,摩尔质量:246
,摩尔质量:246 )在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%
)在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%  、
、 、
、 及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
①“焙烧”生成了铁红;
②常温下,柠檬酸(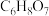 )是一种三元弱酸;
)是一种三元弱酸;
③“还原”时 发生的反应为
发生的反应为 。
。
请回答下列问题:
(1)焙烧时气体与矿料逆流而行,目的是________________ ,请写出焙烧过程中硫铁矿发生反应的化学方程式:_________________ 。
(2)滤渣1的主要成分是___________ (写化学式)。
(3)柠檬酸亚铁(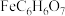 )是一种
)是一种___________ (填“正”“酸式”或“碱式”)盐。
(4)“沉铁”时需控制温度在32℃左右,温度不能过高的原因是________________ 。
(5)在制备过程中,若条件控制不当,容易生成 ,请写出检验
,请写出检验 所用试剂及现象:
所用试剂及现象:______________ 。
(6)某工厂用1kg硫铁矿经上述流程制得1.6kg柠檬酸亚铁,则柠檬酸亚铁的产率为________ (保留两位有效数字)。
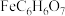 ,摩尔质量:246
,摩尔质量:246 )在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%
)在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%  、
、 、
、 及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
①“焙烧”生成了铁红;
②常温下,柠檬酸(
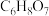 )是一种三元弱酸;
)是一种三元弱酸;③“还原”时
 发生的反应为
发生的反应为 。
。请回答下列问题:
(1)焙烧时气体与矿料逆流而行,目的是
(2)滤渣1的主要成分是
(3)柠檬酸亚铁(
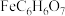 )是一种
)是一种(4)“沉铁”时需控制温度在32℃左右,温度不能过高的原因是
(5)在制备过程中,若条件控制不当,容易生成
 ,请写出检验
,请写出检验 所用试剂及现象:
所用试剂及现象:(6)某工厂用1kg硫铁矿经上述流程制得1.6kg柠檬酸亚铁,则柠檬酸亚铁的产率为
您最近一年使用:0次
9 . 高效净水剂聚合氯化铝铁(PAFC)的组成可表示为 ,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。 中的A是
中的A是___________ 。
②步骤 中发生反应生成
中发生反应生成 中溶液离子方程式为
中溶液离子方程式为___________ 。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:___________ , 的电子式为
的电子式为___________ 。
②所得酸性溶液中,一定大量存在的离子有___________ ;可能存在的离子有___________ ,证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的观象)是___________ 。
③步骤 中发生反应的离子方程式为
中发生反应的离子方程式为___________ 。
 ,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:
,该物质广泛应用于日常生活用水和工业废水的处理。回答下列问题:(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。
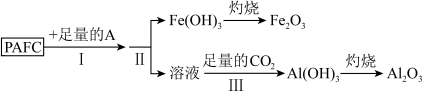
 中的A是
中的A是②步骤
 中发生反应生成
中发生反应生成 中溶液离子方程式为
中溶液离子方程式为(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:

 的电子式为
的电子式为②所得酸性溶液中,一定大量存在的离子有
③步骤
 中发生反应的离子方程式为
中发生反应的离子方程式为
您最近一年使用:0次
解题方法
10 . 工业上以铝土矿(主要成分为 ,含少量
,含少量 、FeO、
、FeO、 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。 溶液浸取铝土矿中的铝元素和铁元素,
溶液浸取铝土矿中的铝元素和铁元素, 溶液的用量不宜过量太多,其原因是
溶液的用量不宜过量太多,其原因是___________ 。
(2)氧化:用 溶液将
溶液将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)沉淀:用1mol/L 溶液调节pH,将
溶液调节pH,将 、
、 转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。___________ 。
②实验室需要1mol/L 溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和___________ 。
③检验 沉淀完全的操作为:静置,
沉淀完全的操作为:静置,___________ 。
(4)碱溶:用NaOH溶液溶解沉淀,分离出 。
。
①该反应的离子方程式为:___________ 。
②下列措施中能提高单位时间内铝元素浸出率的有___________ (填序号)。
A.适当增大NaOH溶液浓度 B.适当加快搅拌速率 C.适当降低温度
(5)碳分:向“碱溶”后的溶液中通入足量 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
 ,含少量
,含少量 、FeO、
、FeO、 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。
 溶液浸取铝土矿中的铝元素和铁元素,
溶液浸取铝土矿中的铝元素和铁元素, 溶液的用量不宜过量太多,其原因是
溶液的用量不宜过量太多,其原因是(2)氧化:用
 溶液将
溶液将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为(3)沉淀:用1mol/L
 溶液调节pH,将
溶液调节pH,将 、
、 转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。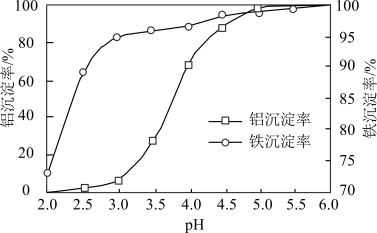
②实验室需要1mol/L
 溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和③检验
 沉淀完全的操作为:静置,
沉淀完全的操作为:静置,(4)碱溶:用NaOH溶液溶解沉淀,分离出
 。
。①该反应的离子方程式为:
②下列措施中能提高单位时间内铝元素浸出率的有
A.适当增大NaOH溶液浓度 B.适当加快搅拌速率 C.适当降低温度
(5)碳分:向“碱溶”后的溶液中通入足量
 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次



