1 . 化学反应常伴有颜色变化。下列实验中观察不到颜色变化 的是
| A.NO暴露在空气中 | B.往Na2CO3溶液中滴加稀盐酸 |
| C.往NaOH溶液中滴加酚酞试液 | D.往FeCl3溶液中滴加KSCN溶液 |
您最近一年使用:0次
解题方法
2 . 铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有_____ 元素。
(2)铁元素有三种常见的氧化物,分别是FeO、 、
、 。其中具有磁性的是
。其中具有磁性的是_____ ,可作红色颜料的是_____ 。
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,此过程中利用了维生素C的_____ 性。
(4) 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。向反应后的溶液中加入_____ ,可回收Cu,并得到 溶液。
溶液。
Ⅱ.高铁酸钾( )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
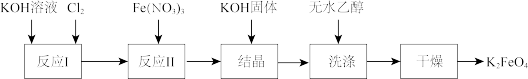
(5)下列说法错误的是_____。
(6)用电解饱和食盐水获得原料氯气的过程中有2mol电子发生转移,试计算理论上最多可制得氯气的体积(标准状况)是_____ L。
Ⅰ.
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有
(2)铁元素有三种常见的氧化物,分别是FeO、
 、
、 。其中具有磁性的是
。其中具有磁性的是(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为(4)
 可作为铜电路板的腐蚀液,其反应原理为Cu与
可作为铜电路板的腐蚀液,其反应原理为Cu与 溶液反应生成
溶液反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 溶液。
溶液。Ⅱ.高铁酸钾(
 )是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
)是一种新型、高效、多功能水处理剂。工业上制备高铁酸钾的流程如下图所示:
(5)下列说法错误的是_____。
A. 中铁元素的化合价为+6价 中铁元素的化合价为+6价 |
| B.用无水乙醇洗涤可以减少产品的损耗 |
C.反应Ⅱ中的氧化剂是 |
| D.高铁酸根离子具有强氧化性,能杀菌消毒 |
您最近一年使用:0次
名校
解题方法
3 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。日常生活中可通过食物摄入铁元素,例如黑木耳中就含有比较丰富的铁元素。某研究性学习小组为测定某地黑木耳中铁的含量,开展了如下研究与实践活动。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取a g黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取a g黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质___________ 溶于水(选填“能”或“不能”)。
(2)取少量滤液于试管中,滴入KSCN溶液,溶液变红。则滤液中铁元素的存在形式有 、
、___________ (填离子符号)。
(3)滤液与Fe生成A的离子方程式是___________ 。
(4)由A转化为B可加入的试剂X可以是___________ (填字母)
a. (
( ) b.
) b. c.
c.
(5)由C转化成D的现象是:白色沉淀迅速变为灰绿色,最终变为___________ 。
(6)将a g黑木耳中的铁元素经流程A→C-D进行完全转化,将D经过一系列处理,得到b g红棕色固体。若流程中加入的铁反应掉c g,则该黑木耳中铁元素的质量分数为___________ (用含a、b、c的代数式表示)。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取a g黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取a g黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。

(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质
(2)取少量滤液于试管中,滴入KSCN溶液,溶液变红。则滤液中铁元素的存在形式有
 、
、(3)滤液与Fe生成A的离子方程式是
(4)由A转化为B可加入的试剂X可以是
a.
 (
( ) b.
) b. c.
c.
(5)由C转化成D的现象是:白色沉淀迅速变为灰绿色,最终变为
(6)将a g黑木耳中的铁元素经流程A→C-D进行完全转化,将D经过一系列处理,得到b g红棕色固体。若流程中加入的铁反应掉c g,则该黑木耳中铁元素的质量分数为
您最近一年使用:0次
2023-09-20更新
|
236次组卷
|
2卷引用:云南省2023年春季学期期末普通高中学业水平考试化学试题
解题方法
4 . 铁是人体必需的微量元素之一,补铁剂中的Fe2+在空气中很容易被氧化为Fe3+,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂和维生素C一起服用的科学性。
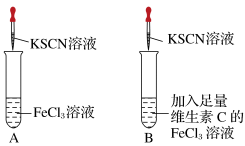
[实验操作]第一步:在A、B两支试管中加入对比试剂;第二步:振荡;第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变___________ 色,B试管中无明显现象。
[实验结论]
(2)维生素C具有___________ (填“氧化性”或“还原性”),能防止Fe2+被氧化为Fe3+,所以补铁剂和维生素C一起服用具有科学依据。
[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和NaHCO3,放入水中立即产生大量气泡(CO2)使口感更好,说明维生素C具有___________ (填“酸性”或“碱性”)。
(4)为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意___________ (写一条即可)。

[实验操作]第一步:在A、B两支试管中加入对比试剂;第二步:振荡;第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变
[实验结论]
(2)维生素C具有
[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和NaHCO3,放入水中立即产生大量气泡(CO2)使口感更好,说明维生素C具有
(4)为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意
您最近一年使用:0次
名校
解题方法
5 . 下列实验现象描述错误的是
| 编号 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先熔化成闪亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热用砂纸打磨过的铝箔 | 铝箔变软,失去光泽,熔化的铝并不滴落 |
| C | 在AlCl3溶液中滴入NaOH溶液 | 生成白色沉淀,后来白色沉淀慢慢溶解 |
| D | 向氧化铁中先加入足量稀盐酸,再滴加KSCN溶液 | 产生血红色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-17更新
|
132次组卷
|
2卷引用:黑龙江省勃利县高级中学2022-2023学年高一下学期开学考试化学试题
6 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次
名校
解题方法
7 . 某工厂以镍废渣(主要成分为 Ni,含少量 Fe、Fe3O4 、Al2O3 和不溶性杂质等)为原料制备翠矾 ( NiSO4 7H2O ),其生产工艺如下:
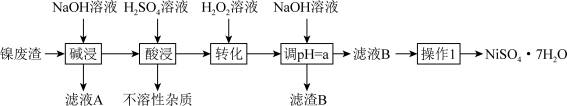
该流程中几种金属离子生成对应氢氧化物沉淀的 pH 如下表。回答下列问题:
(1)“滤液 A”中主要溶质的化学式为___________ 。
(2)“转化”过程中加入H2O2 的目的是将“酸浸”后溶液中的Fe2 氧化为Fe3 ,该过程用离子方程式表示为___________ ;“转化”过程中温度不宜过高,原因是__________ 。
(3)调节pH a ,是为了将溶液中的___________ 元素完全沉淀,则 a 的取值范围是___________ 。证明杂质离子已经被完全除去的实验操作及现象是:取少量滤液 B 于试管中,___________ 。
(4)“操作 1”的目的是将硫酸镍溶液变成NiSO4 7H2O ,具体操作是将溶液进行蒸发浓缩、___________ 、___________ 、洗涤、干燥。

该流程中几种金属离子生成对应氢氧化物沉淀的 pH 如下表。回答下列问题:
| 金属离子 | 开始沉淀的 pH | 完全沉淀的 pH |
| Fe3 | 2.7 | 3.7 |
| Fe2 | 7.6 | 9.7 |
| Ni2 | 7.1 | 9.2 |
(1)“滤液 A”中主要溶质的化学式为
(2)“转化”过程中加入H2O2 的目的是将“酸浸”后溶液中的Fe2 氧化为Fe3 ,该过程用离子方程式表示为
(3)调节pH a ,是为了将溶液中的
(4)“操作 1”的目的是将硫酸镍溶液变成NiSO4 7H2O ,具体操作是将溶液进行蒸发浓缩、
您最近一年使用:0次
8 . 舍勒制备氯气的方法至今还在实验室使用。某个合作学习小组用下图所示实验装置制取 Cl2并验证其性质。(已知:FeCl3的熔点 306℃、沸点 316℃)
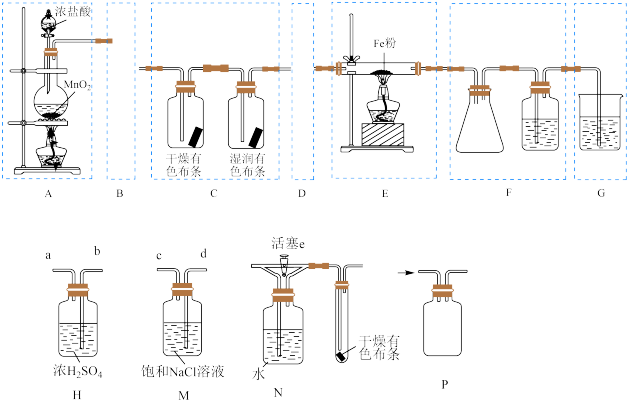
请回答下列问题。
(1)写出装置 A 的反应化学方程式___________ 。
(2)框 B 内装置的作用是净化氯气,把装置 H、M 连接后放入框 B 内,则其连接顺序是___________ (请填写小写字母)。
(3)框 D 装置的作用是收集氯气,请在答卷中按所示气流方向,将集气瓶 P 内的两个玻璃导管补充画完整___________ 。
(4)实验结束后,取锥形瓶中的少量固体于试管中,加足量蒸馏水,充分振荡使固体完全溶解,加入几滴KSCN 溶液后,再加入足量锌粉,充分振荡后静置。请描述上述实验过程中,试管中溶液的颜色变化___________ 。
(5)装置 G 可选用试剂___________ (填标号),并写出相应的离子方程式___________ 。
①KI ②NaCl ③NaOH ④H2SO4
(6)该合作学习小组完成上述实验验后,另一学习小组保留装置 A 和 B,且用装置 N 来替代装置 C,欲达到相同实验目的,请简述使用装置 N 进行实验的操作和现象___________ 。

请回答下列问题。
(1)写出装置 A 的反应化学方程式
(2)框 B 内装置的作用是净化氯气,把装置 H、M 连接后放入框 B 内,则其连接顺序是
(3)框 D 装置的作用是收集氯气,请在答卷中按所示气流方向,将集气瓶 P 内的两个玻璃导管补充画完整
(4)实验结束后,取锥形瓶中的少量固体于试管中,加足量蒸馏水,充分振荡使固体完全溶解,加入几滴KSCN 溶液后,再加入足量锌粉,充分振荡后静置。请描述上述实验过程中,试管中溶液的颜色变化
(5)装置 G 可选用试剂
①KI ②NaCl ③NaOH ④H2SO4
(6)该合作学习小组完成上述实验验后,另一学习小组保留装置 A 和 B,且用装置 N 来替代装置 C,欲达到相同实验目的,请简述使用装置 N 进行实验的操作和现象
您最近一年使用:0次
名校
解题方法
9 . 下列实验中,对应的操作、现象以及结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向KI-淀粉溶液中滴加氯水 | 溶液变成蓝色 | 还原性:Cl->I- |
| B | 浓硫酸滴入蔗糖中,产生的气体导入澄清石灰水 | 蔗糖变黑、体积膨胀,澄清石灰水变浑浊 | 浓硫酸具有脱水性和强氧化性 |
| C | 过量铁粉加入稀硝酸中,充分反应后,滴加KSCN溶液 | 有无色气泡产生,溶液呈血红色 | 稀硝酸能将Fe氧化成Fe3+ |
| D | 向CuSO4溶液中加入一小块钠 | 产生无色气泡,溶液底部有蓝色沉淀生成 | Na任何时候都不能置换铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下表中的各组物质之间通过一步反应就能实现如图所示转化的是
| 编号 | a | b | c | d | 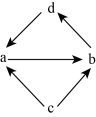 |
| ① |  |  | Na | NaOH | |
| ② |  |  | S |  | |
| ③ |  |  | Fe |  | |
| ④ | MgO |  | Mg |  |
| A.②④ | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
2023-09-14更新
|
294次组卷
|
2卷引用:河南省郑州市第四十七高级中学2022-2023学年高一上学期1月期末考试化学试题



