1 . 下列离子检验说法正确的是
A.某溶液中滴加Ba(NO3)2溶液产生白色沉淀,该溶液中有SO |
B.某溶液中滴加HNO3溶液产生气体,该溶液中一定有CO |
| C.某溶液中滴加酸性KMnO4溶液,酸性KMnO4溶液褪色,该溶液一定有Fe2+ |
| D.某溶液中滴加KSCN溶液,溶液变为红色,该溶液中一定有Fe3+ |
您最近一年使用:0次
名校
解题方法
2 . 实验室制溴苯的原理为 +Br2
+Br2
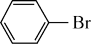 +HBr,某实验小组按如图所示流程模拟提纯粗溴苯。
+HBr,某实验小组按如图所示流程模拟提纯粗溴苯。
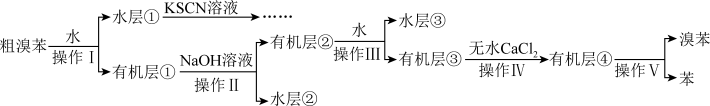
已知:①溴苯与苯互溶;
②各物质的沸点如下:
下列说法正确的是
 +Br2
+Br2
 +HBr,某实验小组按如图所示流程模拟提纯粗溴苯。
+HBr,某实验小组按如图所示流程模拟提纯粗溴苯。
已知:①溴苯与苯互溶;
②各物质的沸点如下:
| 苯 | 液溴 | 溴苯 | |
| 沸点 | 80℃ | 59℃ | 156℃ |
| A.水层①中加入KSCN溶液变红,说明溴化铁已完全被除尽 |
| B.水层②中含有两种盐 |
| C.操作II是分液,操作V是重结晶 |
| D.操作I、IV用到的玻璃仪器不重复 |
您最近一年使用:0次
名校
解题方法
3 . 由下列实验内容能得到相应结论的是
| 选项 | 实验内容 | 实验结论 |
| A | 测定同温度下同浓度的碳酸钠和硫酸钠溶液的pH,比较大小 | 碳元素和硫元素的非金属性强弱 |
| B | 向新制氢氧化铜悬浊液中滴加蔗糖溶液,加热,观察现象 | 蔗糖中含有醛基 |
| C | 向某黄色溶液中加入淀粉KI溶液,溶液变蓝 | 溶液中含有Fe3+ |
| D | 电流通过AlCl3溶液时,可以导电 | AlCl3是离子化合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 某废催化剂含58.2% SiO2、21.0% ZnO、4.50% ZnS和12.8% CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。设计实验流程如图:
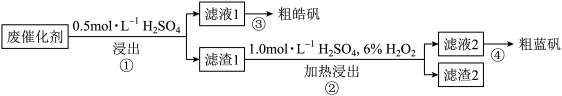
下列说法正确的是

下列说法正确的是
| A.某同学在实验完成之后,得到1.50 g CuSO4∙5H2O,则铜的回收率为30% |
| B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水 |
| C.步骤②操作中,应先加6% H2O2,再在加热搅拌下缓慢加入1.0 mol∙L−1 H2SO4 |
| D.步骤①④都需要用到蒸发皿、酒精灯、漏斗、烧杯等玻璃仪器 |
您最近一年使用:0次
5 . 下列实验现象与实验操作不匹配的是
| 选项 | 实验操作 | 实验现象 |
| A | 向蔗糖中加入浓硫酸,并将产生的气体通过足量溴水 | 蔗糖变黑、膨胀,溴水褪色,有气泡冒出 |
| B | 将足量硼酸滴入 溶液中 溶液中 | 有气泡产生 |
| C | 向盛有 溶液的试管中滴加浓的维生素C溶液 溶液的试管中滴加浓的维生素C溶液 | 溶液由黄色变为浅绿色 |
| D | Mg和盐酸反应,将温度计水银球插入反应液中 | 镁条逐渐溶解,产生气泡,温度计水银柱上升 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-20更新
|
269次组卷
|
4卷引用:重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题
重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题重庆市北碚区2022-2023学年高三上学期10月月考化学试题湖南省株洲市第八中学021-2022学年高三下学期5月月考化学试题(已下线)第9周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
6 . 为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 | 离子方程式 |
| A | 向 溶液中加入 溶液中加入 片 片 | 浅绿色溶液变为无色,溶液中有黑色固体生成 |  具有还原性 具有还原性 |  |
| B | 向 溶液中滴加新制氯水 溶液中滴加新制氯水 | 浅绿色溶液变为棕黄色 |  具有还原性 具有还原性 | 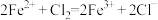 |
| C | 向 溶液中加入铁粉 溶液中加入铁粉 | 棕黄色溶液变为浅绿色 |  具有还原性 具有还原性 | 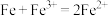 |
| D | 向 溶液中加入铜粉 溶液中加入铜粉 | 蓝色溶液变为棕黄色 |  具有氧化性 具有氧化性 | 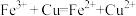 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-05更新
|
1081次组卷
|
8卷引用:重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题
重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)内蒙古巴彦淖尔市第一中学2022-2023学年高一上学期1月期末考试化学试题云南省保山市腾冲市第八中学2023--2024学年高一上学期期末化学强化训练
21-22高一上·浙江宁波·阶段练习
7 . 化学与生活密切相关,下列说法不正确的是
| A.用铁锅炒菜比用铝锅好 |
| B.FeCl3浓溶液与沸水反应生成Fe(OH)3胶体,可作净水剂 |
| C.“84消毒液”可用来杀菌消毒的原因是里面含有氯水 |
| D.食品包装袋内常用铁粉作为脱氧剂以延长食品保存时间 |
您最近一年使用:0次
21-22高三上·山东·阶段练习
8 . 某学习小组拟设计实验探究“铁与硝酸酸化的AgNO3溶液的反应”。
【提出问题】
向纯净铁粉中加入2 mL 0.1 mol·L1硝酸酸化的AgNO3溶液(pH≈2),振荡,静置,观察到溶液呈浅绿色,逐渐变成棕黄色,并伴有黑色沉淀生成。由此说明反应过程中先生成Fe2+,后Fe2+被氧化成Fe3+。氧化Fe、Fe2+的氧化剂是什么?
【设计实验】
实验一 探究Fe2+的来源
提出假设
假设1:Fe被酸性条件下的 氧化;
氧化;
假设2:_______;
假设3:铁被AgNO3和“H+ ”共同作用氧化。
”共同作用氧化。
对照实验:取两支试管,标记甲、乙,分别加入等量纯铁粉,甲中加入2 mL 0.1 mol·L1AgNO3溶液;乙中加入2 mL 硝酸酸化的NaNO3溶液(pH≈2)。一段时间后,向试剂中滴加K3[Fe(CN)6]溶液,实验现象如下表所示。
(1)假设2:_______ (补充完整)。
(2)甲中产生的“橙红色沉淀”是一种银盐,它的化学式可能是_______ 。
(3)根据上述实验可得出结论:常温下Fe和AgNO3溶液反应极慢,Fe2+来自_______ (用离子方程式表示)。已知乙中蓝色沉淀含有钾离子,写出产生蓝色沉淀的离子方程式为_______ 。
实验二 探究Fe3+的来源
对照实验:取两支试管标记丙、丁,分别加入2 mL 0.1 mol·L1新制的FeSO4溶液,再在丙试管滴加10滴0.1 mol·L1 AgNO3溶液;在丁试管中滴加10滴硝酸酸化的0.1 mol·L1 NaNO3溶液(pH≈2)。充分反应后,向上层清液中滴加KSCN溶液,实验现象如下表所示。
(4)丙中产生的黑色颗粒是_______ 。
(5)如果在AgNO3溶液中滴加KSCN溶液会产生丙中部分现象,由此推知丙中白色沉淀是_______ (填化学式)。
(6)实验结论:铁粉和0.1 mol·L1硝酸酸化的AgNO3溶液(pH≈2)反应的实质是_______ 。
【提出问题】
向纯净铁粉中加入2 mL 0.1 mol·L1硝酸酸化的AgNO3溶液(pH≈2),振荡,静置,观察到溶液呈浅绿色,逐渐变成棕黄色,并伴有黑色沉淀生成。由此说明反应过程中先生成Fe2+,后Fe2+被氧化成Fe3+。氧化Fe、Fe2+的氧化剂是什么?
【设计实验】
实验一 探究Fe2+的来源
提出假设
假设1:Fe被酸性条件下的
 氧化;
氧化;假设2:_______;
假设3:铁被AgNO3和“H+
 ”共同作用氧化。
”共同作用氧化。对照实验:取两支试管,标记甲、乙,分别加入等量纯铁粉,甲中加入2 mL 0.1 mol·L1AgNO3溶液;乙中加入2 mL 硝酸酸化的NaNO3溶液(pH≈2)。一段时间后,向试剂中滴加K3[Fe(CN)6]溶液,实验现象如下表所示。
| 试剂 | 溶液颜色 | 加入铁氰化钾溶液 |
| (甲)0.1 mol·L1 AgNO3溶液和铁粉 | 无色溶液 | 橙红色沉淀,未观察到蓝色沉淀 |
| (乙)0.1 mol·L1硝酸酸化的NaNO3溶液(pH≈2)和铁粉 | 绿色 | 蓝色沉淀 |
(2)甲中产生的“橙红色沉淀”是一种银盐,它的化学式可能是
(3)根据上述实验可得出结论:常温下Fe和AgNO3溶液反应极慢,Fe2+来自
实验二 探究Fe3+的来源
对照实验:取两支试管标记丙、丁,分别加入2 mL 0.1 mol·L1新制的FeSO4溶液,再在丙试管滴加10滴0.1 mol·L1 AgNO3溶液;在丁试管中滴加10滴硝酸酸化的0.1 mol·L1 NaNO3溶液(pH≈2)。充分反应后,向上层清液中滴加KSCN溶液,实验现象如下表所示。
| 试剂 | 溶液颜色 | 加入硫氰化钾溶液 |
| (丙)0.1 mol·L1 AgNO3溶液和新制FeSO4溶液 | 黄色,伴有少量黑色颗粒 | 深红色溶液,伴有白色沉淀 |
| (丁)0.1 mol·L1硝酸酸化的NaNO3溶液(pH≈2)和新制FeSO4溶液 | 浅绿色 | 极浅红色 |
(5)如果在AgNO3溶液中滴加KSCN溶液会产生丙中部分现象,由此推知丙中白色沉淀是
(6)实验结论:铁粉和0.1 mol·L1硝酸酸化的AgNO3溶液(pH≈2)反应的实质是
您最近一年使用:0次
9 . 钠、铝、铁是三种非常重要的常见金属。根据所学知识完成下列填空。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为_______ 。
(2)足量的Fe在Cl2中点燃,所得产物的化学式是_______ 。将该产物溶于水配成溶液,分装在两支试管中。
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ 。
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为_______ 。若2.7g纯铝片投入足量盐酸中产生氢气的物质的量为_______ mol。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为
(2)足量的Fe在Cl2中点燃,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为
您最近一年使用:0次
2021-04-02更新
|
122次组卷
|
2卷引用:重庆市巫山县官渡中学2020-2021学年高一下学期第一次月考化学试题
名校
解题方法
10 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.FeCl2溶液:K+、H+、MnO 、SO 、SO | B.NaOH溶液:Na+、K+、CO 、AlO 、AlO |
| C.NaClO溶液:K+、Na+、Fe2+、Cl- | D.FeCl3溶液:Na+、SO 、SCN-、NO 、SCN-、NO |
您最近一年使用:0次



