解题方法
1 . 下列表示对应化学反应的离子方程式正确的是
A.将少量 通入 通入 溶液: 溶液: |
B.室温下用稀 溶解铜: 溶解铜: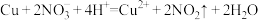 |
C.氯化铁溶液作“腐蚀液”,制作印刷电路板: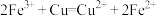 |
D.向 溶液中加入过量 溶液中加入过量 |
您最近一年使用:0次
2 . 为了除去FeCl3中的FeCl2,可向溶液中加入
| A.KMnO4 | B.Cl2 | C.浓硫酸 | D.浓硝酸 |
您最近一年使用:0次
解题方法
3 . 下列关于实验的说法不正确的是
| A.可以选择菠菜、芹菜、黑木耳、蛋黄或动物内脏来检验食品中的铁元素 |
| B.用玻璃棒蘸取某溶液于酒精灯火焰上灼烧,火焰呈黄色说明溶液含钠元素 |
| C.实验室中制取气体装置的连接顺序一般为:发生装置→除杂装置→收集装置→尾气处理装置 |
D.向沸水中逐滴加入5-6滴 饱和溶液,继续煮沸至液体呈红褐色,停止加热可制得 饱和溶液,继续煮沸至液体呈红褐色,停止加热可制得 胶体 胶体 |
您最近一年使用:0次
名校
解题方法
4 . 某无色透明的溶液中,下列离子能大量共存的一组是
A.H+、HCO 、K+、SO 、K+、SO | B.Fe3+、SO 、NH 、NH 、Cl— 、Cl— |
C.Cl—、Ca2+、CO 、K+ 、K+ | D.Na+、Cl—、Ba2+、OH— |
您最近一年使用:0次
解题方法
5 . 下列实验事实与对应的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 蓝色石蕊试纸上滴加新制氯水先变红后褪色 | 新制氯水无酸性,只有漂白性 |
| B | 一定量Fe粉与水蒸气反应后的混合物溶于稀硫酸,在此溶液中滴加KSCN后无明显变化 | 生成的 可能与多余的Fe粉反应,全部变成了 可能与多余的Fe粉反应,全部变成了 |
| C | 金属钠在空气中燃烧后生成淡黄色固体 | 钠在空气中长久放置生成 |
| D | 配制一定物质的量浓度的溶液时,定容时液面超过刻度线 | 需趁下层溶质尚未扩散之际,快速用胶头滴管吸出上层溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-27更新
|
62次组卷
|
2卷引用:浙江省“七彩阳光”新高考研究联盟2023-2024学年高一上学期期中检测化学试卷
名校
6 . 氯化铁在金属蚀刻、污水处理等方面有广泛应用。某兴趣小组以废铁屑为原料,用如图所示装置制备FeCl3·6H2O
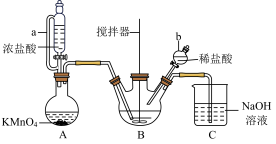
已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/LNa2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
Ⅱ.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
Ⅲ.FeCl3溶液的制备:由装置A制备氯气;向FeCl2的混合液中缓慢通入足量的氯气。
Ⅳ.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
Ⅴ.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
对于上述实验,下列有关装置仪器的说法不正确的是

已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/LNa2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
Ⅱ.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
Ⅲ.FeCl3溶液的制备:由装置A制备氯气;向FeCl2的混合液中缓慢通入足量的氯气。
Ⅳ.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
Ⅴ.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
对于上述实验,下列有关装置仪器的说法不正确的是
| A.装置B中,搅拌器的作用是使反应混合物充分接触 |
| B.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶 |
| C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止污染空气 |
| D.仪器a和仪器b的功能相同,但操作方法不同 |
您最近一年使用:0次
2024-01-16更新
|
151次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高三上学期期中考试化学试卷
名校
7 . 下列反应的离子方程式正确的是
A.食醋除去瓶胆内的水垢: |
| B.氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ |
C. 溶液与体积、等物质的量浓度的 溶液与体积、等物质的量浓度的 溶液混合: 溶液混合: |
D.向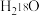 中投入 中投入 固体: 固体: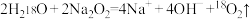 |
您最近一年使用:0次
8 . 铁是日常生活中最为常见的金属,也是用量最大的金属。某化学兴趣小组想通过如下实验来探究铁及其化合物的某些性质。
探究Ⅰ:利用如图来探究铁与水蒸气反应的产物,试回答下列问题(部分装置和仪器已略去)。

(1)装置B中发生反应的化学方程式为___________ 。
(2)装置A、B加热的先后顺序是________ ;石棉绒的作用是________ 。
(3)反应结束后冷却至室温,取一定量B中残留的固体于试管中,加入足量稀盐酸充分溶解后,再加入几滴KSCN溶液,如果溶液没有变红色,能否说明铁与水蒸气反应生成的固体中一定不含+3价的铁,请说明理由______ 。
(4)关于该实验,下列说法不正确 的是________。
探究Ⅱ:利用如图来探究 的制备,希望较长时间内可以观察到B中有白色沉淀出现。
的制备,希望较长时间内可以观察到B中有白色沉淀出现。
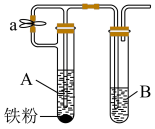
(5)装置A、B中盛放的溶液分别是______ 、________ 。
(6)将B中的白色沉淀置于潮湿的空气中很快就变为红褐色,请用一个化学方程式表示发生该变化的原因______ 。
探究Ⅰ:利用如图来探究铁与水蒸气反应的产物,试回答下列问题(部分装置和仪器已略去)。

(1)装置B中发生反应的化学方程式为
(2)装置A、B加热的先后顺序是
(3)反应结束后冷却至室温,取一定量B中残留的固体于试管中,加入足量稀盐酸充分溶解后,再加入几滴KSCN溶液,如果溶液没有变红色,能否说明铁与水蒸气反应生成的固体中一定不含+3价的铁,请说明理由
(4)关于该实验,下列说法
| A.装置C中盛放的固体可能是碱石灰,起干燥作用 |
B.如果反应后B中残留的固体为黑色纯净物,则该固体可能为 、FeO或 、FeO或 中的一种 中的一种 |
| C.装置D采用向下排空法收集反应产生的气体 |
D.取少许酸性高锰酸钾溶液于试管中,加入(3)中盐酸溶解后的溶液(足量),如果高锰酸钾溶液会褪色,则说明(3)中的溶液一定含有 |
探究Ⅱ:利用如图来探究
 的制备,希望较长时间内可以观察到B中有白色沉淀出现。
的制备,希望较长时间内可以观察到B中有白色沉淀出现。
(5)装置A、B中盛放的溶液分别是
(6)将B中的白色沉淀置于潮湿的空气中很快就变为红褐色,请用一个化学方程式表示发生该变化的原因
您最近一年使用:0次
名校
解题方法
9 . 常温下,下列各组离子一定能在指定溶液中大量共存的是
A. =10﹣12mol•L﹣1的溶液中:Na+、K+、SiO =10﹣12mol•L﹣1的溶液中:Na+、K+、SiO 、Cl﹣ 、Cl﹣ |
B.使甲基橙变黄的溶液中:NH 、Cu2+、NO 、Cu2+、NO 、SO 、SO |
C.由水电离出的c(H+)=1.0×l0﹣13mol•L﹣1的溶液中:Na+、CO 、SO 、SO 、Cl﹣ 、Cl﹣ |
D.使KSCN显红色的溶液中:NH 、K+、Cl﹣、AlO 、K+、Cl﹣、AlO |
您最近一年使用:0次



