解题方法
1 . 各物质的转化关系如下图所示,请完成下列空白。
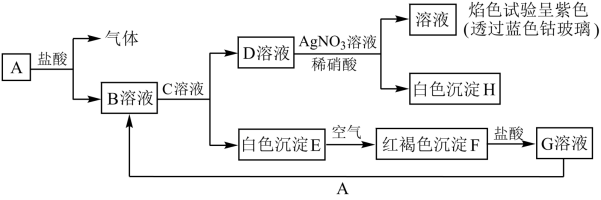
(1)写出B和D 的化学式:B___________ ;D___________ 。
(2)写出E F的化学方程式:
F的化学方程式:___________ 。
(3)向G溶液中加入A,写出反应的离子方程式___________ 。
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子___________ 。

(1)写出B和D 的化学式:B
(2)写出E
 F的化学方程式:
F的化学方程式:(3)向G溶液中加入A,写出反应的离子方程式
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子
您最近一年使用:0次
2 . 根据实验操作和现象得出的结论不正确 的是
| 选项 | 实验操作和现象 | 结论 |
| A | 红热的铁与水蒸气反应后的固体物质,用稀硫酸溶解,滴入几滴硫氰化钾溶液,未显红色 | 固体物质中可能有+3价铁元素 |
| B | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片 | 鲜花褪色,证明氯气具有漂白性 |
| C | 取洁净的铂丝蘸取某溶液,在煤气灯外焰上灼烧,火焰呈黄色 | 溶液中存在Na+,不确定是否含K+ |
| D | 某溶液中滴加AgNO3溶液,出现白色沉淀,再加足量稀HNO3,沉淀不溶解 | 溶液中含有Cl− |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列说法不正确 的是
| A.铝制餐具可用来蒸煮或长时间存放酸性或碱性食物 |
| B.过氧化钠在呼吸面具或潜水艇中可作为氧气的来源 |
| C.氯化铁溶液在工业上可作为制作印刷电路板的腐蚀液 |
| D.碳酸钠和碳酸氢钠溶液均显碱性,可用作食用碱或工业用碱 |
您最近一年使用:0次
解题方法
4 . 铁是人类使用最早的金属之一、运用所学知识,回答下列问题:
(1)电子工业用 溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的化学方程式为
溶液与铜反应的化学方程式为_______ 。
(2)某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了如下实验:
溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有_______ 。
②溶液组成测定:取50.0mL待测溶液,加入足量的 溶液,得到14.35g白色沉淀,则溶液中
溶液,得到14.35g白色沉淀,则溶液中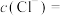
_______  。
。
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:

①滤渣C中物质的化学式为_______ 。
②加入过量D发生反应的离子方程式为_______ 。
③向滤液B和滤液E中通入F的目的是_______ ,该反应的离子方程式为_______ 。
④向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是_______ (填序号)。
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
(1)电子工业用
 溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的化学方程式为
溶液与铜反应的化学方程式为(2)某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了如下实验:
溶液腐蚀铜后所得溶液的组成,进行了如下实验:①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有
②溶液组成测定:取50.0mL待测溶液,加入足量的
 溶液,得到14.35g白色沉淀,则溶液中
溶液,得到14.35g白色沉淀,则溶液中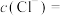
 。
。(3)工程师欲从制造印刷电路板的废液中回收铜,并获得
 溶液,设计如下方案:
溶液,设计如下方案:
①滤渣C中物质的化学式为
②加入过量D发生反应的离子方程式为
③向滤液B和滤液E中通入F的目的是
④向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
您最近一年使用:0次
5 . Ⅰ.中国“奋斗号”载人潜水器在马里亚纳海沟成功坐底深度10909米,挑战了全球海洋最深处。国产新型钛合金、能源供给锂电池等功不可没。磷酸亚铁锂(LiFePO4)可作为锂电池的正极材料,请回答下列问题:
(1)潜水器外壳使用的钛合金
| A.耐高压 | B.耐腐蚀 | C.硬度小 | D.密度小 |
(2)磷酸亚铁锂(LiFePO4)中Fe的化合价为
(3)铁元素的相关信息如图所示,其相对原子质量是

(4)有关铁的性质,说法正确的是________。
| A.在空气中,加热Fe(OH)2可得FeO |
| B.一定条件下,Fe 能与水蒸气反应生成H2 |
| C.常温下,Fe与浓硫酸能反应生成SO2 |
| D.实验室用FeCl3溶液与NaOH溶液反应制备Fe(OH)3胶体 |
(5)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是________。
| A.Fe | B.FeO | C.Fe2O3 | D.Fe3O4 |
(6)要检验Fe3+,可选用的试剂是________。
| A.KSCN 溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
Ⅱ.钠是生活中常见的金属元素,其多种化合物因其特殊性质在生活中都有广泛应用,例如,NaHCO3可用作食品膨松剂、Na2O2可用作供氧剂等。
(7)NaHCO3可用作膨松剂,原因是
(8)下列电离方程式正确的是________。
| A.NaOH = Na+ + O2-+ H+ | B.H2O = H+ + OH- |
C.HClO ClO-+ H+ ClO-+ H+ | D.CH3COONH4 CH3COO-+ NH4+ CH3COO-+ NH4+ |
(9)钠与滴加酚酞的水反应时
| A.钠浮在水面上 | B.钠熔成小球 | C.钠静止在水面上 | D.溶液变为红色 |
(10)Na2O2可作载人潜水器供氧剂,下列关于Na2O2说法正确的是________。
| A.只有离子键 | B.可在常温下由Na与O2反应制得 |
| C.Na2O2与H2O发生化合反应 | D.Na2O2与CO2反应有O2生成 |
您最近一年使用:0次
名校
解题方法
6 . 部分含Fe物质的分类与相应化合价的关系如图所示。下列推断不合理的是

| A.可存在a→e→b的转化 | B.e溶液可与KSCN溶液反应生成红色沉淀 |
| C.能用a制作的容器运输浓硫酸 | D.a可与稀硝酸恰好反应,生成只含b的溶液 |
您最近一年使用:0次
2024-03-21更新
|
325次组卷
|
2卷引用:广东省广州奥林匹克中学2023-2024学年高二下学期4月期中考试化学试题
7 . 根据下列实验操作和现象所得出的结论或解释一定正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 向淀粉-KI溶液中通入Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去 | 还原性:SO2>I->Cl- |
| B | 检验SO2气体中是否混有SO3(g):将气体通入Ba(NO3)2溶液,有白色沉淀生成 | 混有SO3(g) |
| C | 取少量铁与水蒸气反应后的固体于试管中,加足量稀盐酸溶解再滴加KSCN溶液,溶液未变血红色 | 固体产物中不存在三价铁 |
| D | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中,出现白色沉淀 | 元素非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-21更新
|
749次组卷
|
5卷引用:安徽省淮南二中2023-2024学年高一下学期期中教学检测化学试题
8 . 室温下,下列探究方案能达到探究目的的是
| 序号 | 探究方案 | 探究目的 |
| ① | 用不同浓度、等体积的 溶液分别与相同浓度相同体积的 溶液分别与相同浓度相同体积的 溶液反应,观察现象 溶液反应,观察现象 | 探究浓度对反应速率的影响 |
| ② | 用pH计测定同浓度NaClO和NaF溶液的pH,比较溶液pH大小 | 比较HClO与HF的酸性强弱 |
| ③ | 向 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 | 比较CuS和ZnS的溶度积( )的大小 )的大小 |
| ④ | 向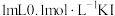 溶液中加入 溶液中加入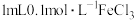 溶液,充分反应后,再加KSCN,观察溶液颜色变化 溶液,充分反应后,再加KSCN,观察溶液颜色变化 | 探究 是否完全反应 是否完全反应 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
解题方法
9 . 铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为__________
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是__________ (用化学方程式表示)
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
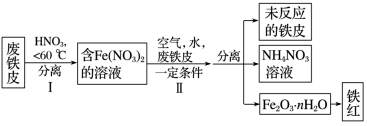
①步骤Ⅰ若要检验是否有Fe3+生成,方法是__________
②步骤Ⅱ中发生反应: ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是__________ (任写一项)。
(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
①K2FeO4中铁元素的化合价__________ ;配平上述反应__________ 。此过程中氧化剂是__________ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是__________ 、__________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若要检验是否有Fe3+生成,方法是
②步骤Ⅱ中发生反应:
 ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH
 ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O①K2FeO4中铁元素的化合价
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近一年使用:0次
10 . 下列“实验结论”与“实验操作及现象”相符的一组是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用光洁无锈的铁丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色 | 该溶液中一定含有钠元素,可能含有钾元素 |
| B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有 |
| C | 向某溶液中滴加氯水后,再滴加 试剂,溶液变成血红色 试剂,溶液变成血红色 | 原溶液中一定含 |
| D | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片,鲜花褪色 | 氯气也具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



