1 . 下列方案设计、现象和结论都正确的是
选项 | 目的 | 方案设计 | 现象和结论 |
A | 探究温度对化学平衡的影响 | 将2mL0.5mol/L的CuCl2溶液加热后置于冷水中,观察现象 | 若溶液由黄绿色变为蓝色,说明降低温度,平衡向逆方向移动: [Cu(H2O)4]2++4Cl-  [CuCl4]2﹣+4H2O [CuCl4]2﹣+4H2O |
B | 判断某卤代烃中的卤素 | 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH水溶液混合后加热,再滴加AgNO3溶液 | 若产生的沉淀为白色,则该卤代烃中含有氯元素 |
C | 探究FeCl3溶液与KI溶液的反应 | 向10mLFeCl3溶液中滴加5mL等浓度的KI溶液,充分反应后,再滴加KSCN溶液,观察现象 | 若溶液最终变为血红色,FeCl3溶液与KI溶液的反应为可逆反应 |
D | 检验食品脱氧剂中还原铁粉是否已变质 | 取脱氧剂包装内固体粉末于试管中,加足量稀盐酸溶解,充分反应后滴加KSCN溶液,振荡,观察溶液颜色变化 | 若溶液未变红色,说明脱氧剂中还原铁粉没有变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-08更新
|
185次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高二下学期4月期中考试化学试题
解题方法
2 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
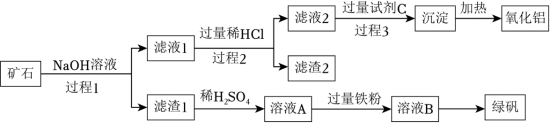
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是___________ 。(答一条)
(2)滤渣1的主要成分是___________ ,举例说明滤渣2的用途___________ 。
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:___________ 。
(4)写出由滤液1生成滤液2的离子方程式___________ 。
(5)用来配制试剂C的物质的电子式为:___________ 。
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为___________ 。
 、
、 、FeO、
、FeO、 等)来制备绿矾(
等)来制备绿矾( )和氧化铝,其工艺流程如图:
)和氧化铝,其工艺流程如图:
回答下列问题:
(1)过程1中能加快矿石与NaOH溶液反应速率的措施是
(2)滤渣1的主要成分是
(3)向溶液A中加入过量铁粉发生反应的离子方程式为:
(4)写出由滤液1生成滤液2的离子方程式
(5)用来配制试剂C的物质的电子式为:
(6)绿矾晶体易被空气中的氧气氧化变质,宜密封保存放置。为探究制备的绿矾样品是否变质,具体的实验操作为
您最近一年使用:0次
名校
3 . 下列实验操作、现象和所得出的结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溶液X与盐酸反应产生的气体通入品红溶液中 | 品红溶液褪色 | 溶液X中一定含有SO |
| B | 将少量碳酸钠溶液滴入足量稀盐酸中 | 有气泡产生 | 非金属性:Cl>C |
| C | 向3 mL KI溶液中滴加几滴溴水,振荡,再滴加 1 mL淀粉溶液 | 溶液显蓝色 | Br2的氧化性比I2强 |
| D | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
172次组卷
|
2卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
4 . 下列实验方案、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 往 溶液中加入Zn片 溶液中加入Zn片 | 短时间内无明显现象 |  的氧化能力比 的氧化能力比 弱 弱 |
| B | 取两份新制氯水,分别滴加 溶液和淀粉KI溶液 溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有+3价铁 |
| D | 取少量 样品溶于蒸馏水,加足量稀盐酸,再加入足量 样品溶于蒸馏水,加足量稀盐酸,再加入足量 溶液 溶液 | 有白色沉淀生成 | 样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将一小块金属钠投入 溶液,钠会浮在溶液上四处游动,同时会有紫红色固体析出 溶液,钠会浮在溶液上四处游动,同时会有紫红色固体析出 | 钠可以置换出铜 |
| B | 向某溶液中加入稀盐酸产生无色无味气体,将该气体通入澄清石灰水,变浑浊 | 溶液一定含有 |
| C | 室温下,向等浓度、等体积的 和 和 溶液中,分别滴加几滴酚酞, 溶液中,分别滴加几滴酚酞, 溶液红色更深 溶液红色更深 | 说明 溶液碱性比 溶液碱性比 强 强 |
| D | 探究脱氧剂中还原铁粉是否变质,可取少量样品溶于盐酸,再滴加KSCN溶液,溶液未变红 | 说明脱氧剂未变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 硫酸亚铁(FeSO4)是中学化学常用试剂,可用于治疗缺铁性贫血症。
(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是___________ (填一种)。
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、铁红、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图所示。___________ 。
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,有气体生成,该反应的离子方程式为___________ 。
③制备摩尔盐时将反应物混合,经___________ 、冷却结晶、过滤、洗涤、干燥得到产品。
用工业废渣(主要含有Fe2O3、FeO、Al2O3及少量Fe)制备绿矾FeSO4·7H2O晶体的流程如下:___________ 。
(4)“溶解”后所得溶液中含有的阳离子为Fe3+和___________ 。
(5)“还原”时选择FeS2而不用Cu粉的原因是___________ 。
(6)测定绿矾中Fe2+的氧化率实验方案如下:
步骤一:称取一定质量的绿矾样品,将其溶于适量的无氧蒸馏水并配成250mL溶液;
步骤二:取步骤一中配得的溶液25.00mL于锥形瓶,并加入适量稀硫酸酸化,逐滴滴加0.0400mol/LKMnO4溶液至恰好完全反应,反应原理为:MnO +Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
+Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
步骤三:另取步骤一中配得的溶液25.00mL于烧杯,加入足量氨水,将沉淀过滤、洗涤、干燥,在空气中灼烧至固体质量不再变化,称得残留红棕色固体的质量为0.4g。(已知: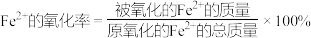 )
)
根据以上数据,计算该绿矾样品中Fe2+的氧化率,写出计算过程:___________ 。
(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、铁红、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图所示。
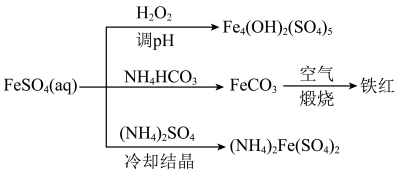
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,有气体生成,该反应的离子方程式为
③制备摩尔盐时将反应物混合,经
用工业废渣(主要含有Fe2O3、FeO、Al2O3及少量Fe)制备绿矾FeSO4·7H2O晶体的流程如下:

(4)“溶解”后所得溶液中含有的阳离子为Fe3+和
(5)“还原”时选择FeS2而不用Cu粉的原因是
(6)测定绿矾中Fe2+的氧化率实验方案如下:
步骤一:称取一定质量的绿矾样品,将其溶于适量的无氧蒸馏水并配成250mL溶液;
步骤二:取步骤一中配得的溶液25.00mL于锥形瓶,并加入适量稀硫酸酸化,逐滴滴加0.0400mol/LKMnO4溶液至恰好完全反应,反应原理为:MnO
 +Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
+Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;步骤三:另取步骤一中配得的溶液25.00mL于烧杯,加入足量氨水,将沉淀过滤、洗涤、干燥,在空气中灼烧至固体质量不再变化,称得残留红棕色固体的质量为0.4g。(已知:
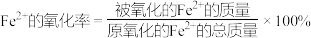 )
)根据以上数据,计算该绿矾样品中Fe2+的氧化率,写出计算过程:
您最近一年使用:0次
名校
7 . 为探究某食品包装袋内的一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸中,进行下列实验,其中结论正确的是
| A.向溶液中滴加KSCN溶液呈红色,说明不含Fe2+,样品完全变质 |
| B.向溶液中通入氯气,然后再加入KSCN溶液呈红色,说明原溶液中含有Fe3+样品变质 |
| C.若滴加KSCN溶液未变红色,再滴加氯水变红色,则说明铁样品粉未变质 |
| D.向溶液中滴加足量的NaOH溶液,观察到红褐色沉淀,则说明样品完全变质 |
您最近一年使用:0次
2023-01-26更新
|
487次组卷
|
4卷引用:上海市奉贤区曙光中学2022-2023学年高一下学期期中考试化学试题
名校
8 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:___________ 。
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
(2)将补全下列实验操作步骤正确排序da___________ e(填标号);重复上述操作步骤,直至A恒重,记为m3g。
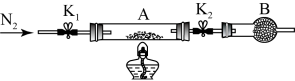
a、点燃酒精灯,加热 b、熄灭酒精灯 c、关闭K1和K2 d、打开K1和K2,缓缓通入N2 e、称量A f、冷却至室温
(3)缓缓通入N2的目的是___________ 。
为探究硫酸亚铁的分解产物,将(2)已恒重的装置A(取出ag后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
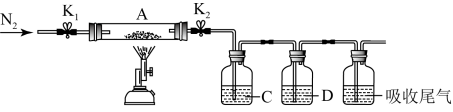
(4)①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为___________ 、___________ 。
②写出硫酸亚铁高温分解反应的化学方程式___________ 。
(5)为了测定A中样品的纯度,将取出ag样品溶于水,配制成500mL溶液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
在滴定的过程中,当___________ 即为滴定终点。
(6)上表中第一次实验中记录数据明显大于后两次,其原因可能是___________(填字母)。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由实验现象可推知:
为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
(2)将补全下列实验操作步骤正确排序da

a、点燃酒精灯,加热 b、熄灭酒精灯 c、关闭K1和K2 d、打开K1和K2,缓缓通入N2 e、称量A f、冷却至室温
(3)缓缓通入N2的目的是
为探究硫酸亚铁的分解产物,将(2)已恒重的装置A(取出ag后)接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

(4)①C、D中的溶液依次为BaCl2、品红。C、D中可观察到的现象分别为
②写出硫酸亚铁高温分解反应的化学方程式
(5)为了测定A中样品的纯度,将取出ag样品溶于水,配制成500mL溶液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
(6)上表中第一次实验中记录数据明显大于后两次,其原因可能是___________(填字母)。
| A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积 |
| B.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗 |
| D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低 |
您最近一年使用:0次
2022-12-10更新
|
98次组卷
|
2卷引用:四川省泸县第一中学2022-2023学年高二下学期5月期中考试化学试题
名校
解题方法
9 . 以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体FeSO4•7H2O的工艺流程如图:
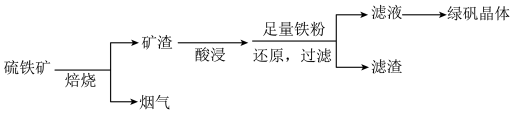
(1)焙烧时黄铁矿要粉碎,其目的是______ 。
(2)由滤液得到绿矾晶体的操作是______ 、______ 、过滤、洗涤、干燥。
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式______ 。
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是______ (写化学式)。
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式______ 。
(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为______ 。

(1)焙烧时黄铁矿要粉碎,其目的是
(2)由滤液得到绿矾晶体的操作是
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO
 +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O
 +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
您最近一年使用:0次
名校
10 . 根据实验操作和现象,不能得出相应结论的是
A.未知溶液中滴加 溶液出现不溶于硝酸的白色沉淀,说明该溶液中存在 溶液出现不溶于硝酸的白色沉淀,说明该溶液中存在 或 或 |
| B.将FeNO32样品溶于稀硫酸,滴加KSCN溶液变红,不能说明FeNO32样品溶于稀硫酸前已氧化变质 |
C.将充满 的密闭玻璃球没泡在热水中,红色加深,则 的密闭玻璃球没泡在热水中,红色加深,则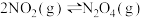 ,△H<0 ,△H<0 |
D.等体积 的 的 和 和 ,分别与足量的 ,分别与足量的 反应, 反应, 放出的氢气多,则酸性: 放出的氢气多,则酸性: |
您最近一年使用:0次
2022-11-03更新
|
202次组卷
|
2卷引用:山东师范大学附属中学2022-2023学年高二上学期期中水平测试化学试题



