12-13高一上·福建·期末
解题方法
1 . 甲、乙、丙三种物质之间有如下转化关系

(1)若甲是不溶于水的白色固体氧化物,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是_______ (填化学式);写出乙→丙转化的离子方程式:_______ 。
(2)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是_______ (填化学式);写出 甲→乙转化的离子方程式_______ 。

(1)若甲是不溶于水的白色固体氧化物,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是
(2)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是
您最近一年使用:0次
2016-12-09更新
|
967次组卷
|
4卷引用:2015-2016学年河北省武邑中学高一下学期周考化学试卷
2015-2016学年河北省武邑中学高一下学期周考化学试卷(已下线)2011-2012学年福建省师大附中高一上学期期末考试化学试卷(已下线)2012-2013学年山西省忻州一中高一上学期期末联考化学试卷(B)2015-2016学年山西省孝义市高一上学期期末考试化学试卷
2011·河北邢台·一模
解题方法
2 . 以黄铜矿(CuFeS2)为原料冶炼铜的反应为:
8CuFeS2+21O2 8Cu+4FeO3+2Fe2O3+16SO2
8Cu+4FeO3+2Fe2O3+16SO2
(1)若Cu为+2价,则反应中每生成1molCu需要转移_____________ mol电子。
(2)为综合利用炉气中的大量SO2,下列方案合理的是___________ 。
a.用浓硫酸吸收 b.用于制备硫酸
c.高空排放 d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有_________ ,一定没有______ 。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有_________ ,写出通入过量的CO2所发生反应的离子方程式:______________ 。
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有_____________ ,写出此步操作中得到红色物质所发生反应的离子方程式____________ 。
8CuFeS2+21O2
 8Cu+4FeO3+2Fe2O3+16SO2
8Cu+4FeO3+2Fe2O3+16SO2(1)若Cu为+2价,则反应中每生成1molCu需要转移
(2)为综合利用炉气中的大量SO2,下列方案合理的是
a.用浓硫酸吸收 b.用于制备硫酸
c.高空排放 d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有
您最近一年使用:0次
14-15高三上·陕西西安·阶段练习
名校
3 . 铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为___________ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___ 。
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
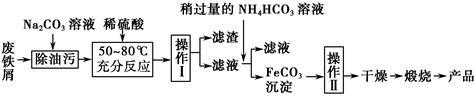
回答下列问题:
①操作Ⅰ的名称是________ ;操作Ⅱ的名称是________ ;操作Ⅱ的方法为_____________________ 。
②请写出生成FeCO3沉淀的离子方程式:____________________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是
②请写出生成FeCO3沉淀的离子方程式:
您最近一年使用:0次
2016-12-08更新
|
541次组卷
|
5卷引用:河北省承德市第二中学2016-2017学年高二下学期第一次月考化学试题
12-13高一上·河北邢台·阶段练习
名校
解题方法
4 . (1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,用化学方程式表示该反应的原理.___________________________________________
(2)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
___________________________________
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,该反应的离子方程式为______________________ ;用此溶液进行以下反应,取少量溶液于一支试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为____________________ 。
(2)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,该反应的离子方程式为
您最近一年使用:0次



