2014高三·全国·专题练习
名校
解题方法
1 . 某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)。

(1)MgCO3的分解产物为____________________________________________________ 。
(2)装置C的作用是__________________________ ,处理尾气的方法为_____________ 。
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
①乙组得到的黑色粉末是____________ 。
②甲组步骤1中反应的离子方程式为_________________________________________ 。
③乙组步骤4中,溶液变血红的原因为_______________________________________ ;溶液褪色可能的原因及其验证方法为________________________________________ 。
④从实验安全考虑,上图装置还可采取的改进措施是__________________________ 。

(1)MgCO3的分解产物为
(2)装置C的作用是
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变血红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变血红,后褪色 |
②甲组步骤1中反应的离子方程式为
③乙组步骤4中,溶液变血红的原因为
④从实验安全考虑,上图装置还可采取的改进措施是
您最近一年使用:0次
2023-07-06更新
|
666次组卷
|
12卷引用:贵州省习水县一中2018-2019学年高一上学期12月份考试化学试题
贵州省习水县一中2018-2019学年高一上学期12月份考试化学试题贵州省惠水县第一高级中学2019-2020学年高一上学期期末考试化学试题(已下线)2014届高考化学二轮冲刺非选择题增分专练 综合实验设计练习卷2015届广东省广州市十三中高三上学期期中理综化学试卷2016届广西桂林市第十八中学高三第一次月考化学试卷云南省玉溪市新平彝族傣族自治县第三中学2019-2020学年高一上学期期中考试化学试题云南省永平县第二中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修一第三章《金属及其化合物》测试卷2(已下线)第2讲 离子反应和离子方程式(已下线)第6讲 铁及其重要化合物(已下线)专题突破卷12 化学实验基础(一)-2024年高考化学一轮复习考点通关卷(新教材新高考)江西省宜春市百树学校2023-2024学年高三上学期暑期阶段测试化学试卷
2 . 下列物质的性质与用途对应关系不正确 的是
| A.铜能导电可用于制作导线 |
| B.浓硫酸具有氧化性可用作干燥剂 |
| C.盐酸与Fe2O3反应可用于除铁锈 |
| D.氯气与Ca(OH)2反应可用于制漂粉精 |
您最近一年使用:0次
2021-06-27更新
|
335次组卷
|
3卷引用:贵州省2020年12月学业水平考试化学试题
名校
解题方法
3 . 下列离子方程式的书写正确的是
| A.氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O |
B.氢氧化钡溶液与硫酸镁溶液混合:Ba2++ = BaSO4↓ = BaSO4↓ |
C.向碳酸氢钠溶液中滴加稀盐酸: +2H+= H2O+CO2↑ +2H+= H2O+CO2↑ |
| D.氢氧化铜和稀盐酸反应:H++OH-= H2O |
您最近一年使用:0次
2021-06-20更新
|
172次组卷
|
8卷引用:贵州省贵阳市第六中学2019—2020学年高一上学期期中考试化学试题
名校
解题方法
4 . 某物质溶于盐酸后,再向溶液中滴加KSCN溶液,结果溶液颜色无变化,然后加入新制的氯水后溶液呈红色,则这种物质是
| A.FeCl3 | B.FeCl2 | C.Fe(OH)3 | D.Fe3O4 |
您最近一年使用:0次
2021-03-01更新
|
103次组卷
|
2卷引用:贵州省贵阳市清镇养正学校2020-2021学年高一上学期第三次月考化学试题
名校
解题方法
5 . “材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请回答下列问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:

①写出步骤I的化学方程式:______ 。
②步骤II经过冷凝得到的SiHCl3(沸点为33.0℃)中含有少量的SiCl4(沸点为57.6℃)和HCl(沸点为-84.7℃),提纯SiHCl3的实验方法是______ ,所用到的玻璃仪器除酒精灯、温度计、蒸馏烧瓶、锥形瓶外还需要______ 。
(2)磁性材料。这种黑色材料含有某种铁的氧化物,请写出该氧化物溶于稀硫酸溶液的化学方程式______ ,简述检验所得溶液中较低价态阳离子的实验操作方法______ 。
(3)高分子材料。一种新型高效净水剂[Al Fe (OH)n Cl6-n]m属于无机高分子材料,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为______ 。
(4)消毒材料。棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,补充完整并配平下列反应方程式:______ 。
______Cl2+______Na2CO3+______=______NaHCO3+______NaCl+______Cl2O
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:

①写出步骤I的化学方程式:
②步骤II经过冷凝得到的SiHCl3(沸点为33.0℃)中含有少量的SiCl4(沸点为57.6℃)和HCl(沸点为-84.7℃),提纯SiHCl3的实验方法是
(2)磁性材料。这种黑色材料含有某种铁的氧化物,请写出该氧化物溶于稀硫酸溶液的化学方程式
(3)高分子材料。一种新型高效净水剂[Al Fe (OH)n Cl6-n]m属于无机高分子材料,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为
(4)消毒材料。棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,补充完整并配平下列反应方程式:
______Cl2+______Na2CO3+______=______NaHCO3+______NaCl+______Cl2O
您最近一年使用:0次
14-15高一上·吉林长春·期中
名校
解题方法
6 . Fe2O3又称铁红,请根据要求完成下列问题.
(1)Fe2O3固体(红棕色)属于_____ (填纯净物或者混合物).将其加入适量盐酸,反应的化学方程式_____
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式_____
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现_____ 色,即可制得Fe(OH)3胶体.
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到_____ 烧杯的液体中产生了丁达尔效应.
(1)Fe2O3固体(红棕色)属于
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
2020-01-12更新
|
429次组卷
|
15卷引用:2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷
(已下线)2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷云南省玉溪市通海县第二中学2019-2020学年高一上学期12月月考化学试题安徽省滁州市定远县育才学校2019-2020学年高一上学期期中考试(普通班)化学试题安徽省滁州市定远县重点中学2018-2019学年高一上学期期末考试化学试题人教版高中化学必修1第二章《化学物质及其变化》测试卷2人教版高一化学必修1第二章《化学物质及其变化》测试卷云南省绥江县第三中学2019-2020学年高一上学期期末考试化学试题安徽安庆宿松县第二中学2019-2020学年高一11月月考化学试题湖南省湘阴县知源学校2020-2021学年高一上学期10月月考化学试题贵州省毕节市威宁第四中学2021-2022学年高一上学期第一次月考化学试题江苏省海安市南莫中学2021-2022学年高一上学期第一次月考备考金卷A卷化学试题吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(理)试题河北省石家庄藁城新冀明中学2021-2022学年高一上学期第一次月考化学试题四川省广元市八二一中学2021-2022学年高一上学期期中考试化学试题(已下线)【定心卷】3.1.2 铁的重要化合物随堂练习-人教版2023-2024学年必修第一册
解题方法
7 . A~G各物质间的关系如下图,其中B、D为气态单质。

请回答下列问题:
(1)物质C和E的名称分别为________ 、________ ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为__________________________ ;
若只能在加热情况下进行,则反应物A应为________ ;
(3)写出D转化为G的化学方程式_____________________________________ ;
(4)新配制的F溶液应加入________ 以防止其转化为G。检验G溶液中阳离子的常用试剂是________ ,实验现象为________________________________________ 。

请回答下列问题:
(1)物质C和E的名称分别为
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为
若只能在加热情况下进行,则反应物A应为
(3)写出D转化为G的化学方程式
(4)新配制的F溶液应加入
您最近一年使用:0次
8 . 氧化铁和氧化亚铁都能与氢碘酸反应,下列相关叙述中正确的是( )
| A.都有铁盐生成 | B.都有亚铁盐生成 |
| C.都是氧化还原反应 | D.反应中都无电子转移 |
您最近一年使用:0次
2019-09-26更新
|
144次组卷
|
3卷引用:贵州省道真县民族中学2019-2020学年上学期开学考试 高二 化学
贵州省道真县民族中学2019-2020学年上学期开学考试 高二 化学贵州省黎平第二中学2019-2020学年高一上学期期末考试化学试题(已下线)3.1.1 铁及其化合物练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)
9 . 用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
| A.氧化铜 | B.氧化铁 | C.四氧化三铁 | D.二氧化锰 |
您最近一年使用:0次
2018-12-23更新
|
137次组卷
|
3卷引用:贵州省息烽县一中2018-2019学年高一上学期11月考试化学试题
名校
解题方法
10 . 某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O)晶体,设计了如下流程:
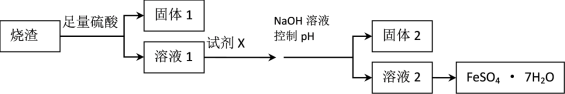
已知:(1)常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
(2)七水合硫酸亚铁(FeSO4·7H2O)的溶解度
(1)溶解烧渣选用足量硫酸,写出Fe2O3与硫酸反应的离子方程式_______________ ;检验溶液1中含有Fe3+的实验方法是___________________ ;
(2)固体1是制作单晶硅的主要原料,写出该反应的化学方程式___________________ ;
(3)试剂X是__________________ ;固体2是___________________ ;
(4)加入NaOH溶液控制pH应不超过_________________ ;
(5)从溶液2中获得晶体的的方法为______________ , _____________ 过滤、洗涤、干燥。
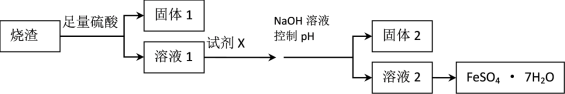
已知:(1)常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
| 开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Al3+ | 3.3 | 5.0 |
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| FeSO4·7H2O溶解度(g) | 15.5 | 26.5 | 32.9 | 40.2 | 48.9 |
(2)固体1是制作单晶硅的主要原料,写出该反应的化学方程式
(3)试剂X是
(4)加入NaOH溶液控制pH应不超过
(5)从溶液2中获得晶体的的方法为
您最近一年使用:0次
2018-10-06更新
|
98次组卷
|
2卷引用:贵州省遵义市航天高级中学2018-2019学年高二(理)上学期第一次月考化学试题



