2014高三·全国·专题练习
名校
解题方法
1 . 某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)。

(1)MgCO3的分解产物为____________________________________________________ 。
(2)装置C的作用是__________________________ ,处理尾气的方法为_____________ 。
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
①乙组得到的黑色粉末是____________ 。
②甲组步骤1中反应的离子方程式为_________________________________________ 。
③乙组步骤4中,溶液变血红的原因为_______________________________________ ;溶液褪色可能的原因及其验证方法为________________________________________ 。
④从实验安全考虑,上图装置还可采取的改进措施是__________________________ 。

(1)MgCO3的分解产物为
(2)装置C的作用是
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变血红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变血红,后褪色 |
②甲组步骤1中反应的离子方程式为
③乙组步骤4中,溶液变血红的原因为
④从实验安全考虑,上图装置还可采取的改进措施是
您最近一年使用:0次
2023-07-06更新
|
666次组卷
|
12卷引用:2015届广东省广州市十三中高三上学期期中理综化学试卷
2015届广东省广州市十三中高三上学期期中理综化学试卷(已下线)2014届高考化学二轮冲刺非选择题增分专练 综合实验设计练习卷2016届广西桂林市第十八中学高三第一次月考化学试卷贵州省习水县一中2018-2019学年高一上学期12月份考试化学试题云南省玉溪市新平彝族傣族自治县第三中学2019-2020学年高一上学期期中考试化学试题云南省永平县第二中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修一第三章《金属及其化合物》测试卷2贵州省惠水县第一高级中学2019-2020学年高一上学期期末考试化学试题(已下线)第2讲 离子反应和离子方程式(已下线)第6讲 铁及其重要化合物(已下线)专题突破卷12 化学实验基础(一)-2024年高考化学一轮复习考点通关卷(新教材新高考)江西省宜春市百树学校2023-2024学年高三上学期暑期阶段测试化学试卷
名校
解题方法
2 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。铁元素的价类二维图如图,其中的箭头表示部分物质的转化关系,下列说法正确的是
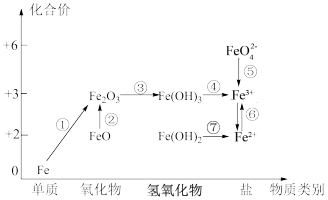

| A.铁与高温水蒸气的反应可实现上述转化① |
| B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末 |
| C.加热Fe(OH)3可转化为Fe2O3,加水溶解可实现转化④ |
D.由图可预测:高铁酸盐(FeO )具有强氧化性,可用于消毒。FeO )具有强氧化性,可用于消毒。FeO 与水反应最终可生成Fe(OH)3胶体,从而吸附水中的悬浮物,故高铁酸盐可用作净水剂 与水反应最终可生成Fe(OH)3胶体,从而吸附水中的悬浮物,故高铁酸盐可用作净水剂 |
您最近一年使用:0次
2022-02-19更新
|
708次组卷
|
15卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题安徽省砀山县第二中学2019-2020学年高一上学期第二次月考化学试题(已下线)【南昌新东方】铁路一中 2019-2020 高一(上)期末人教版(2019)高一必修第一册 第三章素养检测宁夏石嘴山市第三中学2020-2021学年高一上学期第二次月考化学试题黑龙江省鹤岗市第一中学2020-2021学年高一上学期12月月考化学试题山西省沁县中学2020-2021学年高一上学期第二次月考化学试题广东省广州市外国语学校等三校2020-2021学年高一上学期期末联考化学试题广东省广州市第七中学2022-2023学年高一上学期综合练习问卷化学试题吉林省长春外国语学校2021-2022学年高一上学期第二次月考化学试题湖北省恩施州高中教育联盟2021-2022学年高一上学期期末考试化学试题湖南省湘阴县知源高级中学2022-2023学年高三上学期第二次月考化学试题河北省石家庄外国语学校2022-2023学年高一上学期期中考试化学试题湖南省株洲市第一中学2022-2023学年高三上学期第五次月考化学试题湖南省衡阳市第八中学2022-2023学年高一下学期开学考试化学试题
3 . 砖瓦是用含铁元素等杂质的粘土隔绝空气烧制而成的。当烧窑作业临近结束时,若用淋水的办法来降温,则砖呈青色,称青砖;若用捅开窑顶自然冷却的办法,则砖呈红色,称红砖。下列有关说法中,不正确的是
| A.砖瓦的主要成分是二氧化硅 |
| B.淋水的目的是在窑内产生还原性气氛 |
| C.青砖中铁元素主要以氧化亚铁形式存在 |
| D.红砖中铁元素主要以氧化铁形式存在 |
您最近一年使用:0次
20-21高三上·广东·阶段练习
4 . NiSO4·6H2O广泛应用于镀镍电镀液、催化剂和金属着色剂。某科研小组用富含镍(NiS)的工业废渣(含SiO2、FeO、Al2O3等杂质)制备NiSO4·6H2O,设计流程图如下:

已知:Ksp[Ni(OH)2]=1.0×10-15,Ksp[Fe(OH)2]=1.0×10-16,Ksp[Al(OH)3]=1.0×10-34,Ksp[Fe(OH)3]=1.0×10-39。
根据要求回答下列问题:
(1)酸浸过程中,1 mol NiS失去8NA个电子,同时生成一种无色有毒气体,写出该反应的化学方程式:_______ 。
(2)“氧化”保持滤液温度在40 ℃左右,加入6%的H2O2溶液,加入H2O2溶液的目的是_______ ,若上述流程省去“氧化”步骤,后果是_______ 。
(3)常温下,调节pH除去铁和铝元素,若溶液中c(Ni2+)=0.1 mol·L−1,溶液的pH范围应调节为4.3~_______ 之间。
(4)小火煮沸的作用是使沉淀颗粒长大,这样做有利于_______ 。
(5)沉镍后,加入硫酸发生反应的离子方程式为_______ 。
(6)为得到NiSO4·6H2O,操作X为_______ 。

已知:Ksp[Ni(OH)2]=1.0×10-15,Ksp[Fe(OH)2]=1.0×10-16,Ksp[Al(OH)3]=1.0×10-34,Ksp[Fe(OH)3]=1.0×10-39。
根据要求回答下列问题:
(1)酸浸过程中,1 mol NiS失去8NA个电子,同时生成一种无色有毒气体,写出该反应的化学方程式:
(2)“氧化”保持滤液温度在40 ℃左右,加入6%的H2O2溶液,加入H2O2溶液的目的是
(3)常温下,调节pH除去铁和铝元素,若溶液中c(Ni2+)=0.1 mol·L−1,溶液的pH范围应调节为4.3~
(4)小火煮沸的作用是使沉淀颗粒长大,这样做有利于
(5)沉镍后,加入硫酸发生反应的离子方程式为
(6)为得到NiSO4·6H2O,操作X为
您最近一年使用:0次
名校
5 . 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示。下列推断不合理的是
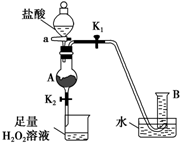

| A.烧杯中H2O2溶液的作用是将Fe2+氧化为Fe3+ |
| B.A中存在氧化铁与盐酸生成氯化铁的反应 |
| C.B中收集到的气体是氢气 |
| D.将反应后的溶液放入烧杯中再通入少量SO2, 则溶液颜色立即由棕黄色变为浅绿色 |
您最近一年使用:0次
2021-04-02更新
|
442次组卷
|
13卷引用:2017届广东省深圳市三校高三上学期第一次联考化学卷
2017届广东省深圳市三校高三上学期第一次联考化学卷吉林省实验中学2017-2018学年高一上学期期末考试化学试题(已下线)2019年4月21日 《每日一题》 三轮复习-每周一测(已下线)【南昌新东方】江西省南昌市第三中学2019-2020学年度高三上学期11月月考化学试题四川省成都市实验中学2020届高三下学期第二次周考理科综合化学试题广东省揭阳市揭东县2020-2021学年高一上学期期末考试化学试题(已下线)【浙江新东方】双师155高一下.江苏省昆山市陆家高级中学、柏庐高级中学、周市高级中学2020-2021学年高一下学期6月联合考试化学试题安徽省涡阳一中2020-2021年高一上学期期末考试化学试题陕西省汉中市2022届高三第一次校际联考化学试题(已下线)专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)甘肃省会宁县第一中学2021-2022学年高一上学期期末考试化学试题山东省济宁市第一中学2022-2023学年高一上学期期末教学质量线上测试化学试题
解题方法
6 . A、B、C、D为为中学常见单质。通常状况下,A为固体,能被磁铁吸收,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如图所示(其中某些反应条件和部分反应物已略去)。请回答下列问题:
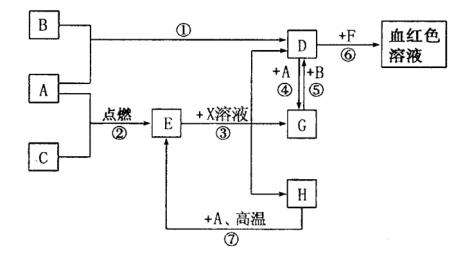
(1)写出下列物质的化学式:A___________ 、X___________
(2)反应⑥说明D溶液中含有___________ 离子
(3)反应⑦的化学方程式是___________
(4)反应③离子方程式是___________
(5)反应④离子方程式是___________

(1)写出下列物质的化学式:A
(2)反应⑥说明D溶液中含有
(3)反应⑦的化学方程式是
(4)反应③离子方程式是
(5)反应④离子方程式是
您最近一年使用:0次
名校
解题方法
7 . 下列说法不正确的是
| A.铁和水蒸气反应生成Fe(OH)3和H2 |
| B.铁的所有氧化物都是碱性氧化物 |
| C.氧化镁、氧化铝的熔点很高,都是耐高温材料 |
| D.Na2O2中阴、阳离子的个数比为1∶2 |
您最近一年使用:0次
名校
解题方法
8 . 纵观古今,化学与生活皆有着密切联系。下列说法错误的是
| A.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏土 |
| B.“水声冰下咽,沙路雪中平”描述的是水的三态变化:“冰,水为之,而寒于水”,说明冰转化为水吸热 |
| C.《天工开物》记载制造青瓦“窑泥周寒其孔,浇水转釉”,红瓦转化为青瓦的原因是Fe2O3转化为其他铁的氧化物 |
| D.“春蚕到死丝方尽,蜡炬成灰泪始干” ,古代的蜡是高级脂肪酸酯,属于高分子聚合物 |
您最近一年使用:0次
2020-12-20更新
|
326次组卷
|
2卷引用:广东省深圳市高级中学2021届高三第三次阶段性测试(10月)化学试题
名校
9 . 纳米级 Fe3O4可用于以太阳能为热源分解水制H2,过程如下图所示。下列说法正确的是:
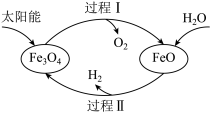

A.过程Ⅰ的反应为:6FeO+O2 2Fe3O4 2Fe3O4 |
| B.过程Ⅱ中H2为还原剂 |
C.整个过程的总反应为:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
| D.FeO 是过程Ⅰ的氧化产物 |
您最近一年使用:0次
2020-11-09更新
|
539次组卷
|
13卷引用:北京市怀柔区2019-2020学年高一上学期期末考试化学试题
北京市怀柔区2019-2020学年高一上学期期末考试化学试题北京市第一七一中学 2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw78广东省汕头市潮阳区2020-2021学年高一上学期期末考试化学试题广东省普宁市华侨中学2021-2022学年高一上学期期中考试化学试题广东省潮州市潮安区2021-2022学年高一上学期期末考试化学试题广东省惠州中学2021-2022学年高一上学期12月月考化学(A卷)试题辽宁省沈阳市重点高中协作校2021-2022学年高一上学期期中测试化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期期中线上考试化学试题浙江省余姚中学2022-2023学年高一上学期期中考试化学试题云南省玉溪市2022-2023学年高一上学期期末考试化学试题山西省大同市2022-2023学年高一上学期11月期中考试化学试题作业(十九) 铁及其化合物之间的转化关系
名校
解题方法
10 . 下列离子方程式正确的是
| A.Fe2O3溶于HI溶液中:Fe2O3+6H+=2Fe3++3H2O |
B.CO2通入足量的NaAlO2液中: +CO2+2H2O=Al(OH)3↓+ +CO2+2H2O=Al(OH)3↓+ |
C.少量NaHCO3溶液与Ca(OH)2溶液反应:Ca2++2OH-+2 =CaCO3↓+ =CaCO3↓+ +2H2O +2H2O |
D.溶液中NH4Al(SO4)2与Ba(OH)2以物质的量之比1:2反应: +Al3++2 +Al3++2 +2Ba2++4OH-=NH3∙H2O+Al(OH)3 ↓+2BaSO4 ↓ +2Ba2++4OH-=NH3∙H2O+Al(OH)3 ↓+2BaSO4 ↓ |
您最近一年使用:0次



