名校
解题方法
1 . 把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经分析,该溶液中无 Fe3+,且生成的 Fe2+与反应生成的H2的物质的量之比为 3:1,则原混合物中Fe2O3与Fe的物质的量之比为
| A.1:1 | B.2:5 | C.4:1 | D.3:1 |
您最近一年使用:0次
2021-04-17更新
|
470次组卷
|
5卷引用:江苏省苏州第十中学2019-2020学年高一上学期12月月考化学试卷
名校
2 . 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示。下列推断不合理的是
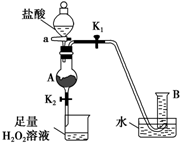

| A.烧杯中H2O2溶液的作用是将Fe2+氧化为Fe3+ |
| B.A中存在氧化铁与盐酸生成氯化铁的反应 |
| C.B中收集到的气体是氢气 |
| D.将反应后的溶液放入烧杯中再通入少量SO2, 则溶液颜色立即由棕黄色变为浅绿色 |
您最近一年使用:0次
2021-04-02更新
|
442次组卷
|
13卷引用:2017届广东省深圳市三校高三上学期第一次联考化学卷
2017届广东省深圳市三校高三上学期第一次联考化学卷吉林省实验中学2017-2018学年高一上学期期末考试化学试题(已下线)2019年4月21日 《每日一题》 三轮复习-每周一测(已下线)【南昌新东方】江西省南昌市第三中学2019-2020学年度高三上学期11月月考化学试题四川省成都市实验中学2020届高三下学期第二次周考理科综合化学试题陕西省汉中市2022届高三第一次校际联考化学试题广东省揭阳市揭东县2020-2021学年高一上学期期末考试化学试题(已下线)【浙江新东方】双师155高一下.江苏省昆山市陆家高级中学、柏庐高级中学、周市高级中学2020-2021学年高一下学期6月联合考试化学试题安徽省涡阳一中2020-2021年高一上学期期末考试化学试题(已下线)专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)甘肃省会宁县第一中学2021-2022学年高一上学期期末考试化学试题山东省济宁市第一中学2022-2023学年高一上学期期末教学质量线上测试化学试题
名校
解题方法
3 . A~E是中学常见的5种化合物,A、B是氧化物,X、Y是生活中常见的金属单质,它们之间的转化关系如下图所示。

则下列说法正确的是

则下列说法正确的是
| A.A常用作红色的油漆和涂料 |
| B.用KSCN溶液检验E溶液中的金属阳离子 |
C.X与A反应的化学方程式是Al2O3+2Fe Fe2O3+2Al Fe2O3+2Al |
| D.化合物B和C既能与强酸反应又能与强碱反应 |
您最近一年使用:0次
解题方法
4 . 铁是生产、生活中应用很广泛的一种金属。下列是与铁的性质有关的部分实验图,请回答下列问题。

(1)A中细铁丝燃烧生成黑色固体物质的化学式是___ 。
(2)B中铁钉最易生锈的部位是___ (填“a”、“b”或“c”)。
(3)C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是___ 。
(4)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比___ (填“增大”、“不变”或“减小”)。

(1)A中细铁丝燃烧生成黑色固体物质的化学式是
(2)B中铁钉最易生锈的部位是
(3)C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是
(4)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比
您最近一年使用:0次
2020-10-21更新
|
84次组卷
|
3卷引用:陕西省榆林市第十二中学2020-2021学年高一上学期第一次月考化学试题
陕西省榆林市第十二中学2020-2021学年高一上学期第一次月考化学试题陕西省榆林市第十二中学2020-2021学年高一上学期第二次月考化学试题(已下线)易错专题21 铁单质的性质-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)
名校
5 . 关于如图所示的转化过程的分析错误的是
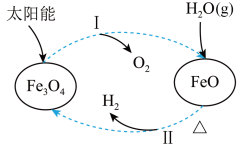
| A.Fe3O4中铁元素的化合价为+2、+3 |
| B.过程Ⅰ中每消耗58g Fe3O4转移1mol电子 |
C.过程Ⅱ中化学方程式为3FeO+H2O(g) Fe3O4+H2 Fe3O4+H2 |
| D.该过程总反应为2H2O(g)=O2+2H2 |
您最近一年使用:0次
2020-10-10更新
|
609次组卷
|
16卷引用:2019年陕西省汉中市高考第一次模拟化学试题
2019年陕西省汉中市高考第一次模拟化学试题山东济宁市兖州区2020届高三网络模拟考试化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(一)菏泽一中2020届高三3月份化学质量检测肥城一中2020届高三3月份在线检测化学试题上海市建平中学2021届高三上学期9月月考化学试题山东省济钢高级中学2021届高三10月质量检测化学试题高一必修第一册(苏教2019)专题4 专题综合检测卷福建省长泰县第一中学2021届高三上学期11月考试化学试题河北师范大学田家炳中学2020-2021学年高一上学期第3次月考化学试题甘肃省嘉峪关市第一中学2021届高三上学期二模考试化学试题(已下线)第12周 晚练题-备战2022年高考化学周测与晚练(新高考专用)江苏省镇江市句容市南京人民中学等三市四校联考2022-2023学年高一下学期4月月考化学试题江苏省无锡市辅仁高级中学2023-2024学年高一上学期期末复习化学模块综合试卷(一)11.2024年苏州木渎高级中学高一3月月考江苏省苏州第十中学校2023-2024学年高一下学期3月月考化学试题
名校
6 . 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成。(提示:铝与氧化铁发生的反应称为铝热反应)
②另取20g A全部溶于0.15L 6.0mol·L-1盐酸中,得溶液C。
③将①中得到的单质B和溶液C反应,放出气体1.12L(标准状况下),同时生成溶液D,还残留固体B。
④用KSCN溶液检验时,溶液D不变色。
(1)反应①的产物中的单质B是________ ,反应方程为____________ 。若将单质B溶于盐酸中,再向所得溶液中滴加足量的NaOH溶液后振荡,可看到的现象为___________ ,此过程用化学方程可以表示为______________ 。
(2)②所发生各反应的离子方程式是:___________________ 和___________________ 。
(3)若溶液D的体积仍为0.15L,则该溶液中c(Mg2+)为________ ,c(Fe2+)为________ 。
①取适量A进行铝热反应,产物中有单质B生成。(提示:铝与氧化铁发生的反应称为铝热反应)
②另取20g A全部溶于0.15L 6.0mol·L-1盐酸中,得溶液C。
③将①中得到的单质B和溶液C反应,放出气体1.12L(标准状况下),同时生成溶液D,还残留固体B。
④用KSCN溶液检验时,溶液D不变色。
(1)反应①的产物中的单质B是
(2)②所发生各反应的离子方程式是:
(3)若溶液D的体积仍为0.15L,则该溶液中c(Mg2+)为
您最近一年使用:0次
名校
解题方法
7 . (1)钠与氧气的反应会因条件不同而导致现象不同,产物不同,反应的实质也不同。据此回答下列问题:
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:__________________ 。
②钠在空气中受热所发生反应的化学方程式是__________________ 。
③将4.6克钠投入足量水中,标况下生成气体的体积是__________ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为____________ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为___________________________________ 。
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:___________________________________ 。
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是_______ 。
②写出磁石的主要成分和盐酸反应的离子方程式______________ 。
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:
②钠在空气中受热所发生反应的化学方程式是
③将4.6克钠投入足量水中,标况下生成气体的体积是
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是
②写出磁石的主要成分和盐酸反应的离子方程式
您最近一年使用:0次
13-14高二上·黑龙江牡丹江·期末
名校
8 . 在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过水。以下叙述正确的是
| A.分别还原amolFe2O3所需H2、Al、CO的物质的量之比为3:2:3 |
| B.检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
| C.铝热剂就是单指Fe2O3粉末和铝粉的混合物 |
| D.明矾属于硫酸盐,含结晶水,属于混合物 |
您最近一年使用:0次
2019-05-09更新
|
299次组卷
|
15卷引用:陕西省西安市第八十三中学高三年级2017-2018学年第三阶段考试化学试题
陕西省西安市第八十三中学高三年级2017-2018学年第三阶段考试化学试题(已下线)2012-2013学年黑龙江省牡丹江一中高二上学期期末化学试卷(已下线)2014届安徽六校教育研究会高三第一次联考化学试卷河南省周口市中英文学校2018届高三上学期开学摸底考试化学试题甘肃省武威市第六中学2018届高三上学期第二次阶段性过关考试化学试题广西灵山县第二中学2018届高三上学期开学考试化学试题江西省临川区第一中学2018届高三上学期第二次月考化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题1湖南省永州市祁阳县高考补习学校2018届高三上学期第二次月考化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题2云南省玉溪市通海县第二中学2019届高三9月月考化学试题【全国百强校】河北省邢台市第一中学2018-2019学年高一下学期期中考试化学试题辽宁省本溪市2019-2020学年高一下学期寒假验收考试化学试题(已下线)专题07 铁及其化合物(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学课后-8.1.1 金属矿物 海水资源的开发利用-人教2019必修第二册
名校
9 . 下列说法正确的是
| A.赤铁矿的主要成分是Fe3O4 |
| B.Fe2O3为碱性氧化物,可与水反应生成Fe(OH)3 |
| C.铁锈的主要成分是Fe2O3 |
| D.Fe3O4中铁元素有+2价和+3价,Fe3O4是混合物 |
您最近一年使用:0次
2019-01-01更新
|
419次组卷
|
10卷引用:云南省昭通市威信县第一中学2018-2019学年高一上学期12月份考试化学试题
云南省昭通市威信县第一中学2018-2019学年高一上学期12月份考试化学试题云南省玉溪市新平彝族傣族自治县第三中学2019-2020学年高一上学期期中考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷3(已下线)3.1.1 铁的单质 铁的氧化物练习(2)——《高中新教材同步备课》(人教版 必修第一册)吉林省长春外国语学校2020-2021学年高一上学期第二次月考化学(文)试题陕西省西安市阎良区关山中学2021-2022学年高一上学期第三次质量检测化学(理科)试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2021-2022学年高一上学期第二次月考化学试题云南省景东彝族自治县第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)西藏拉萨市部分学校2023-2024学年高一上学期12月期末联考化学试题
10 . 下列各组物质反应后,再滴入KSCN溶液,显红色的是
| A.CuCl2溶液中加入铁粉 | B.单质Fe与过量稀盐酸反应后的溶液中再加入少量氯水 |
| C.向FeO中加入稀硫酸 | D.Fe(OH)3与过量稀盐酸反应后的溶液中再加入过量铁粉 |
您最近一年使用:0次
2018-01-24更新
|
202次组卷
|
3卷引用:陕西省黄陵中学2017-2018学年高一(普通班)下学期开学考试化学试题
陕西省黄陵中学2017-2018学年高一(普通班)下学期开学考试化学试题天津市红桥区2017-2018学年高一上学期期末考试化学试题(已下线)2018年11月9日 ——《每日一题》人教必修1Fe2+和Fe3+的检验



