解题方法
1 . 某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下:提出猜想
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
(1)I.解决问题1
a.需用到的药品除1mol•L﹣1CuSO4溶液、稀硫酸外还需________ (填试剂的化学式)溶液.
b.用胆矾晶体配制1mol•L﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有________ (填仪器名称).
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
②________ .
(2)Ⅱ.解决问题2
取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:________ .
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜________ (填稳定或不稳定),溶液中正一价铜比正二价铜________ (填稳定或不稳定).
(3)Ⅲ.解决问题3设计如下装置(夹持装置未画出):
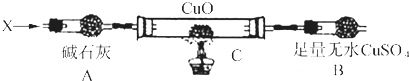
当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是________ .
b.X的化学式为________ .
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
(1)I.解决问题1
a.需用到的药品除1mol•L﹣1CuSO4溶液、稀硫酸外还需
b.用胆矾晶体配制1mol•L﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
②
(2)Ⅱ.解决问题2
取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜
(3)Ⅲ.解决问题3设计如下装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是
b.X的化学式为
您最近一年使用:0次
2 . 实验室用粗铜(含杂质Fe)制备氯化铜。
(1)采用如下图所示的装置进行实验(部分仪器和夹持、加热装置已略去)。
①仪器A的名称是________________ ;
②实验开始前,需要做的操作是____________________ 。
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为______ (填“是”或“否”)必需。原因_______________________________________ 。
④实验过程中,装置C内的现象是___________________________________ 。
⑤氢氧化钠溶液的作用是______________________________ ,其中发生反应的主要离子方程式___________________________ 、________________________ 。
(2)若将C中所得固体加稀硫酸溶解。取少量溶液于小试管中,滴加2滴KSCN溶液,无现象。请用必要的文字和离子方程式解释出现这一现象的原因_________________ 。
(1)采用如下图所示的装置进行实验(部分仪器和夹持、加热装置已略去)。

①仪器A的名称是
②实验开始前,需要做的操作是
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为
④实验过程中,装置C内的现象是
⑤氢氧化钠溶液的作用是
(2)若将C中所得固体加稀硫酸溶解。取少量溶液于小试管中,滴加2滴KSCN溶液,无现象。请用必要的文字和离子方程式解释出现这一现象的原因
您最近一年使用:0次
名校
解题方法
3 . 碱式氯化镁(MgOHCl)常用作塑料添加剂,工业上制备方法较多,其中利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁的工艺属于我国首创。某中学科研小组根据该原理设计如下装置图进行相关实验,装置C中CuO的质量为8.0g。
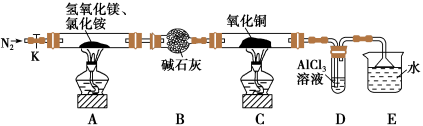
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:___________ 。
(2)装置D中生成沉淀,发生反应的离子方程式为___________ 。
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:_______ 。
(4)若测得碱石灰的质量增加了ag,则得到碱式氯化镁的质量为___________ g。
(5)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,该反应中转移电子的物质的量为___ mol,写出装置C中发生的化学反应方程式_____ 。

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:
(2)装置D中生成沉淀,发生反应的离子方程式为
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:
(4)若测得碱石灰的质量增加了ag,则得到碱式氯化镁的质量为
(5)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,该反应中转移电子的物质的量为
您最近一年使用:0次
4 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产。某化学兴趣小组在实验室利用如图装置制备氨气并探究相关性质。
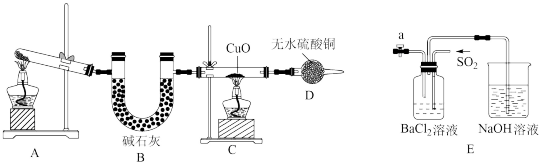
(1)该实验中A装置制备 的化学方程式是
的化学方程式是_______ 。
(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是_______ (填装置序号)。
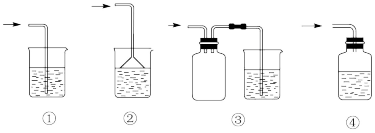
(3)若将D与a相连,在E中产生白色沉淀。其化学式为:_______ 。若向a处单独通入_______ (填下列气体字母编号),在E中也会产生白色沉淀。
A. B.
B. C.
C. D.
D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:_______ ;若充分反应后红色固体有剩余,再加入下列的_______ (填字母)试剂,固体又可以继续溶解。
A.稀 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
②已知 也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:_______ 。

(1)该实验中A装置制备
 的化学方程式是
的化学方程式是(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是

(3)若将D与a相连,在E中产生白色沉淀。其化学式为:
A.
 B.
B. C.
C. D.
D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:
A.稀
 B.
B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液②已知
 也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
也为红色固体,若反应前C中CuO质量为8g。反应后C中红色固体质量为6.8g,则C中发生的总反应化学方程式为:
您最近一年使用:0次
2022-07-13更新
|
323次组卷
|
3卷引用:辽宁省抚顺市六校协作体2021-2022学年高一下学期期末考试化学试题
名校
解题方法
5 . Li-CuO二次电池的比能量高、工作温度宽,性能优异,广泛用于军事和空间领域。
(1)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量由大到小的顺序为:__________________ 。
(2)通过如下过程制备CuO。

①过程I,H2O2的作用是________________________ 。
②过程II产生Cu2(OH)2CO3的离子方程式是_______________________ 。
③过程II,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。

二者比值为1:0.8时,产品中可能含有的杂质是________________________ 。
(3)Li-CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理为:2Li+CuO=Li2O+Cu装置示意图如下。放电时,正极的电极反应式是______________________ 。

(1)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量由大到小的顺序为:
(2)通过如下过程制备CuO。

①过程I,H2O2的作用是
②过程II产生Cu2(OH)2CO3的离子方程式是
③过程II,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。

二者比值为1:0.8时,产品中可能含有的杂质是
(3)Li-CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理为:2Li+CuO=Li2O+Cu装置示意图如下。放电时,正极的电极反应式是

您最近一年使用:0次



