解题方法
1 . 氯乙烯是用途广泛的石油化工产品,工业上常利用乙烯氧氯化法生产:

已知:ⅰ.
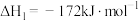
ⅱ.
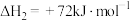
ⅲ.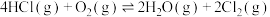
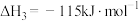
回答下列问题:
(1)
___________  。
。
(2)已知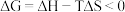 ,反应可自发进行。若
,反应可自发进行。若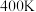 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ___________ (“能”或“不能”)自发进行。
(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有___________ 。
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化
(4)向 密闭容器中初始投入
密闭容器中初始投入 、
、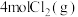 和
和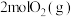 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时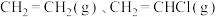 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。___________ 和___________ 的体积分数随温度的变化。
②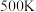 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的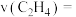
___________ ,该反应的平衡常数
___________ 。
(5) 时,控制进料浓度
时,控制进料浓度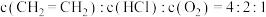 。容器中发生反应
。容器中发生反应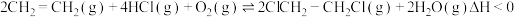 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为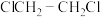 的转化率大小来体现)
的转化率大小来体现)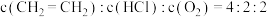 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的___________ (填“上”或“下”)方。
②因受现有工业设备限制,需保持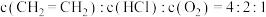 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大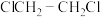 的选择性,可选择从
的选择性,可选择从___________ 方向进一步展开研究。

已知:ⅰ.

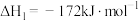
ⅱ.

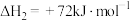
ⅲ.
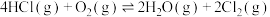
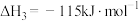
回答下列问题:
(1)

 。
。(2)已知
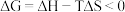 ,反应可自发进行。若
,反应可自发进行。若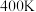 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化

(4)向
 密闭容器中初始投入
密闭容器中初始投入 、
、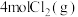 和
和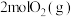 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时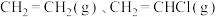 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。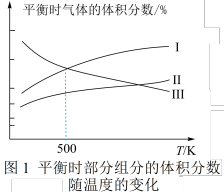
②
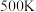 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的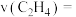

(5)
 时,控制进料浓度
时,控制进料浓度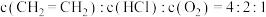 。容器中发生反应
。容器中发生反应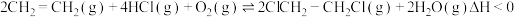 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为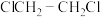 的转化率大小来体现)
的转化率大小来体现)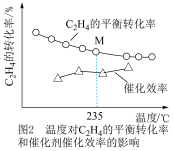
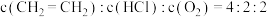 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的②因受现有工业设备限制,需保持
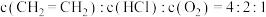 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大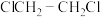 的选择性,可选择从
的选择性,可选择从
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 氢能作为清洁能源是题佳碳中和能源载体,为应对气候变化全球掀起了氢能发展热潮,制备氢气有多种途径。
I.甲醇产生氢气的反应为: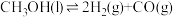

(1)已知相关物质的标准熵数值如表:
该反应能自发进行的最低温度为_______ K。(精确至 )
)
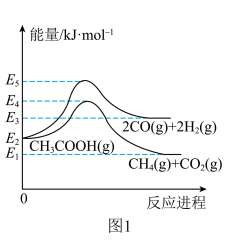
Ⅱ.乙酸制氢过程发生如下反应:
反应I: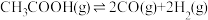
反应Ⅱ: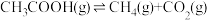
(2)已知反应: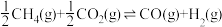
①由图1可得,
_______  。
。_______ 。
A.混合气体密度不变时,反应达到平衡 B.加入 ,可提高
,可提高 的转化率
的转化率
C.加入催化剂,可提高 的平衡产率 D.充入Ar,对
的平衡产率 D.充入Ar,对 的产率不产生影响
的产率不产生影响
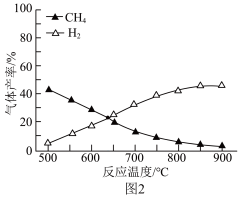
(3)在容积相同的密闭容器中,加入等量乙酸蒸气(只发生反应I和Ⅱ),在相同时间测得温度与气体产率的关系如图2所示。约650℃之前,氢气产率低于甲烷的可能原因是_______ 。(答出一点即可) 为
为_______ 。(用平衡分压代替平衡浓度计算)
Ⅲ.热分解也可制氢,其原理是: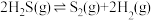 。
。
(5)不同温度和压强下, 的平衡转化率变化如图。生成物
的平衡转化率变化如图。生成物 的状态为
的状态为_______ (填“气态”或“非气态”),
_______  (填“>”或“<”)。
(填“>”或“<”)。
I.甲醇产生氢气的反应为:
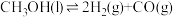

(1)已知相关物质的标准熵数值如表:
| 化学式 |  |  |  |
标准熵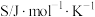 |  | 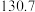 | 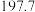 |
 )
)Ⅱ.乙酸制氢过程发生如下反应:
反应I:
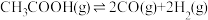
反应Ⅱ:
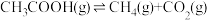
(2)已知反应:
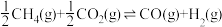
①由图1可得,

 。
。
A.混合气体密度不变时,反应达到平衡 B.加入
 ,可提高
,可提高 的转化率
的转化率C.加入催化剂,可提高
 的平衡产率 D.充入Ar,对
的平衡产率 D.充入Ar,对 的产率不产生影响
的产率不产生影响(3)在容积相同的密闭容器中,加入等量乙酸蒸气(只发生反应I和Ⅱ),在相同时间测得温度与气体产率的关系如图2所示。约650℃之前,氢气产率低于甲烷的可能原因是
 为
为Ⅲ.热分解也可制氢,其原理是:
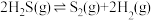 。
。(5)不同温度和压强下,
 的平衡转化率变化如图。生成物
的平衡转化率变化如图。生成物 的状态为
的状态为
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解题方法
3 . 回答下列问题。
(1)分别向 的
的 溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应时的热效应分别为
溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应时的热效应分别为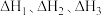 ,下列关系正确的是
,下列关系正确的是___________ (填序号)。
① ②
② ③
③
原因是___________ 。
有 四个体积均为
四个体积均为 的恒容密闭容器,在A、B、C中按不同投料比
的恒容密闭容器,在A、B、C中按不同投料比 充入
充入 和
和 (如下表),加入催化剂发生反应:
(如下表),加入催化剂发生反应: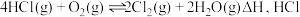 的平衡转化率
的平衡转化率 与Z和温度
与Z和温度 的关系如图所示。
的关系如图所示。
(2)该反应的
___________ 0,a___________ 4.(填“>”“=”或“<”)
(3) 该反应的平衡常数的值为
该反应的平衡常数的值为___________ 。若起始时,在容器D中充入 和
和 达平衡时容器中
达平衡时容器中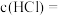
___________  。
。
(4)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程如图所示,其中吸附在金催化剂表面上的物种用·标注。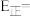
___________  ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:___________ 。
(1)分别向
 的
的 溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应时的热效应分别为
溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应时的热效应分别为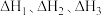 ,下列关系正确的是
,下列关系正确的是①
 ②
② ③
③
原因是
有
 四个体积均为
四个体积均为 的恒容密闭容器,在A、B、C中按不同投料比
的恒容密闭容器,在A、B、C中按不同投料比 充入
充入 和
和 (如下表),加入催化剂发生反应:
(如下表),加入催化剂发生反应: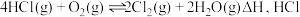 的平衡转化率
的平衡转化率 与Z和温度
与Z和温度 的关系如图所示。
的关系如图所示。
| 容器 | 起始时 | ||
 | 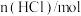 | Z | |
| A | 300 | 0.25 | a |
| B | 300 | 0.25 | b |
| C | 300 | 0.25 | 4 |
| D | 300 | ||
(2)该反应的

(3)
 该反应的平衡常数的值为
该反应的平衡常数的值为 和
和 达平衡时容器中
达平衡时容器中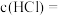
 。
。(4)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程如图所示,其中吸附在金催化剂表面上的物种用·标注。
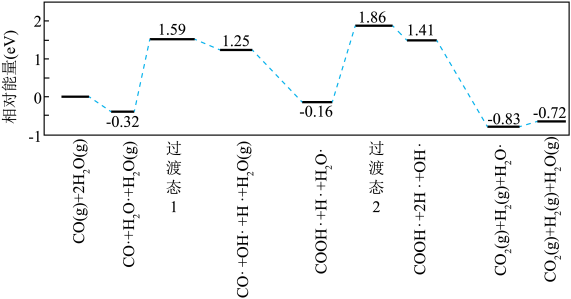
 ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:
您最近一年使用:0次
4 . 向丙烷脱氢制丙烯的反应体系中加入 ,可以提高丙烷的利用率。在相同温度下,分别将投料比相同的
,可以提高丙烷的利用率。在相同温度下,分别将投料比相同的 、
、 混合气体以相同流速持续通过同种催化剂表面,
混合气体以相同流速持续通过同种催化剂表面, 转化率和
转化率和 选择性随通入气体时间的变化如图:
选择性随通入气体时间的变化如图:
I.反应①
反应②
Ⅱ.反应体系中存在 的裂解和生成积炭等副反应。
的裂解和生成积炭等副反应。
Ⅲ. 的选择性
的选择性
下列说法正确的是
 ,可以提高丙烷的利用率。在相同温度下,分别将投料比相同的
,可以提高丙烷的利用率。在相同温度下,分别将投料比相同的 、
、 混合气体以相同流速持续通过同种催化剂表面,
混合气体以相同流速持续通过同种催化剂表面, 转化率和
转化率和 选择性随通入气体时间的变化如图:
选择性随通入气体时间的变化如图:
I.反应①

反应②

Ⅱ.反应体系中存在
 的裂解和生成积炭等副反应。
的裂解和生成积炭等副反应。Ⅲ.
 的选择性
的选择性
下列说法正确的是
A. |
B.30min内,两体系中 选择性相同,生成 选择性相同,生成 的速率也相同 的速率也相同 |
C.iii中的 转化率高于iv中的,是因为反应②使反应①的平衡正向移动 转化率高于iv中的,是因为反应②使反应①的平衡正向移动 |
D.iii、iv对比,150min后iv中 转化率为0,可能是因为积炭使催化剂失效 转化率为0,可能是因为积炭使催化剂失效 |
您最近一年使用:0次
5 .  和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。
Ⅰ.
Ⅱ.
Ⅲ.
(1) =
=___________ 。
(2)① =1:1对应图中曲线
=1:1对应图中曲线___________ (填序号)。
②900K下,曲线b、c、d的平衡转化率显著大于a的原理为___________ 。
(3)900K,将 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。
①下列说法正确的是___________ (填序号)。
A.通入氩气可提高 的平衡转化率
的平衡转化率
B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡
D.改善催化剂的性能可提高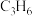 生产效率
生产效率
②若初始压强为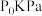 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
=___________  ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=___________ 。
(4)利用反应 可制备高纯Ni。
可制备高纯Ni。
① 晶体中不存在的作用力有
晶体中不存在的作用力有___________ 。
A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
② 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是___________ ,判断依据是___________ 。
 和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。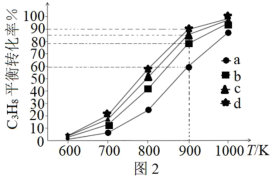
Ⅰ.

Ⅱ.

Ⅲ.

(1)
 =
=(2)①
 =1:1对应图中曲线
=1:1对应图中曲线②900K下,曲线b、c、d的平衡转化率显著大于a的原理为
(3)900K,将
 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。①下列说法正确的是
A.通入氩气可提高
 的平衡转化率
的平衡转化率B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当
 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡D.改善催化剂的性能可提高
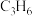 生产效率
生产效率②若初始压强为
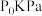 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
= ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=(4)利用反应
 可制备高纯Ni。
可制备高纯Ni。①
 晶体中不存在的作用力有
晶体中不存在的作用力有A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
②
 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是
您最近一年使用:0次
名校
解题方法
6 . 甲烷干重整(DRM)以温室气体CH4和CO2为原料在催化条件下生成合成气CO和H2。体系中发生的反应有
ⅰ.
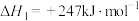
ⅱ.

ⅲ.

ⅳ.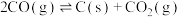

(1)
___________  。
。
(2)___________ (填“高温”或“低温”)有利于反应ⅰ自发进行。
(3)起始投入CH4和CO2各1kmol,DRM反应过程中所有物质在100kPa下的热力学平衡数据如图所示。___________ (填“升高”、“不变”或“降低”),理由是___________ 。
②625℃时,起始投入CH4、CO2、H2、CO、H2O各0.5kmol,此时反应ⅱ的
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③625℃时,反应体系经过t min达到平衡状态,测得甲烷的平衡转化率为 。0~t min生成CO的平均速率为
。0~t min生成CO的平均速率为___________  ;用物质的量分数表示反应i的平衡常数
;用物质的量分数表示反应i的平衡常数
___________ (用含 的表达式表示,列计算式即可)。
的表达式表示,列计算式即可)。
ⅰ.

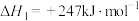
ⅱ.


ⅲ.


ⅳ.
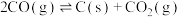

(1)

 。
。(2)
(3)起始投入CH4和CO2各1kmol,DRM反应过程中所有物质在100kPa下的热力学平衡数据如图所示。
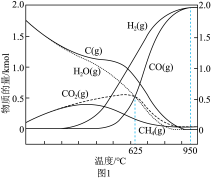
②625℃时,起始投入CH4、CO2、H2、CO、H2O各0.5kmol,此时反应ⅱ的

 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。③625℃时,反应体系经过t min达到平衡状态,测得甲烷的平衡转化率为
 。0~t min生成CO的平均速率为
。0~t min生成CO的平均速率为 ;用物质的量分数表示反应i的平衡常数
;用物质的量分数表示反应i的平衡常数
 的表达式表示,列计算式即可)。
的表达式表示,列计算式即可)。
您最近一年使用:0次
7 .  可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:
反应1:
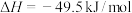
反应2:
 (副反应)
(副反应)
(1) ,该反应的ΔH=
,该反应的ΔH=___________ kJ/mol。
(2)将 和
和 按物质的量之比1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得
按物质的量之比1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图[选择性为目标产物在总产物(
、CO选择性(S)的变化如图[选择性为目标产物在总产物( 和CO)中的比率]。
和CO)中的比率]。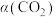 随温度变化趋势的是曲线
随温度变化趋势的是曲线___________ (填“a”、“b”或“c”)。
②随着温度升高,a、b、c三条曲线接近重合的原因是___________ 。
③P点对应的反应2的平衡常数
___________ (结果保留2位有效数字,已知:分压=总压×该组分物质的量分数,对于反应 的
的 ,其中
,其中 ,
,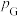 、
、 、
、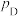 、
、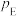 为各组分的平衡分压)。
为各组分的平衡分压)。
(3)最近,中科院研究出首例在室温条件超快传输的氢负离子导体 ,将带来系列技术变革。某小组据此设计了如图装置,以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如图装置,以电化学方法进行反应1。___________ (填“正极”或“负极”)。
②生成 的电极反应式为
的电极反应式为___________ 。
③若反应2(副反应)也同时发生,出口Ⅱ为CO、 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为___________ (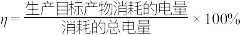 )。
)。
 可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:反应1:

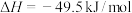
反应2:

 (副反应)
(副反应)(1)
 ,该反应的ΔH=
,该反应的ΔH=(2)将
 和
和 按物质的量之比1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得
按物质的量之比1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图[选择性为目标产物在总产物(
、CO选择性(S)的变化如图[选择性为目标产物在总产物( 和CO)中的比率]。
和CO)中的比率]。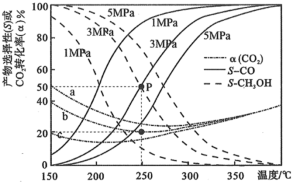
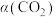 随温度变化趋势的是曲线
随温度变化趋势的是曲线②随着温度升高,a、b、c三条曲线接近重合的原因是
③P点对应的反应2的平衡常数

 的
的 ,其中
,其中 ,
,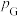 、
、 、
、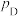 、
、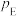 为各组分的平衡分压)。
为各组分的平衡分压)。(3)最近,中科院研究出首例在室温条件超快传输的氢负离子导体
 ,将带来系列技术变革。某小组据此设计了如图装置,以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如图装置,以电化学方法进行反应1。
②生成
 的电极反应式为
的电极反应式为③若反应2(副反应)也同时发生,出口Ⅱ为CO、
 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为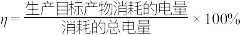 )。
)。
您最近一年使用:0次
8 . 乙烯和丙烯都是重要的化工原料,甲醇和丙烷共反应制备乙烯和丙烯可大幅度降低能耗,该反应体系中存在如下反应:
I.C3H8(g) C3H6(g)+H2(g) ΔH1=+124.20kJ/mol
C3H6(g)+H2(g) ΔH1=+124.20kJ/mol
Ⅱ.C3H8(g) CH4(g)+C2H4(g) ΔH2=+81.25 kJ/mol
CH4(g)+C2H4(g) ΔH2=+81.25 kJ/mol
Ⅲ.CH4(g)+C2H4(g) C3H6(g)+H2(g) ΔH3
C3H6(g)+H2(g) ΔH3
Ⅳ.CH3OH(g)+H2(g) CH4(g)+H2O(g) ΔH4=-115.93 kJ/mol
CH4(g)+H2O(g) ΔH4=-115.93 kJ/mol
(1)ΔH3=___________ 。
(2)630℃时,向盛有催化剂的真空容器中充入1molC3H8(g),保持容器压强为0.1MPa,进行反应,当反应达到平衡时,C3H8(g)的转化率为60%,C2H4(g)的平衡分压为0.0125MPa。
①此时p(C3H6)=___________ ,反应Ⅱ的分压平衡常数为Kp=___________ MPa。
②若向上述平衡体系中充入N2(g),再次达到平衡时C3H8(g)的转化率___________ (填“>”“<”或“=”)60%,其原因为___________ 。此时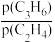 将会
将会___________ (填“变大”“变小”或“不变”)。
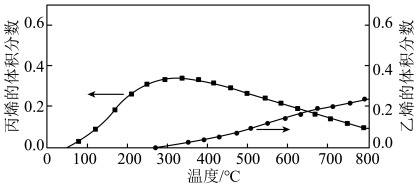
(3)若向盛有催化剂的真空容器中按物质的量之比4:1:1充入C3H8(g)、CH3OH(g)和H2O(g),仍在容器压强为0.1MPa下进行反应,平衡体系中C2H4(g)和C3H6(g)的体积分数随温度(T)的变化如图所示。解释300℃后,C3H6(g)的体积分数随温度(T)的变化的原因为___________ ;甲醇的作用为___________ 。
I.C3H8(g)
 C3H6(g)+H2(g) ΔH1=+124.20kJ/mol
C3H6(g)+H2(g) ΔH1=+124.20kJ/molⅡ.C3H8(g)
 CH4(g)+C2H4(g) ΔH2=+81.25 kJ/mol
CH4(g)+C2H4(g) ΔH2=+81.25 kJ/molⅢ.CH4(g)+C2H4(g)
 C3H6(g)+H2(g) ΔH3
C3H6(g)+H2(g) ΔH3Ⅳ.CH3OH(g)+H2(g)
 CH4(g)+H2O(g) ΔH4=-115.93 kJ/mol
CH4(g)+H2O(g) ΔH4=-115.93 kJ/mol(1)ΔH3=
(2)630℃时,向盛有催化剂的真空容器中充入1molC3H8(g),保持容器压强为0.1MPa,进行反应,当反应达到平衡时,C3H8(g)的转化率为60%,C2H4(g)的平衡分压为0.0125MPa。
①此时p(C3H6)=
②若向上述平衡体系中充入N2(g),再次达到平衡时C3H8(g)的转化率
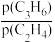 将会
将会(3)若向盛有催化剂的真空容器中按物质的量之比4:1:1充入C3H8(g)、CH3OH(g)和H2O(g),仍在容器压强为0.1MPa下进行反应,平衡体系中C2H4(g)和C3H6(g)的体积分数随温度(T)的变化如图所示。解释300℃后,C3H6(g)的体积分数随温度(T)的变化的原因为
您最近一年使用:0次
9 . 丙烷脱氢制丙烯是较为理想的丙烯生产渠道。
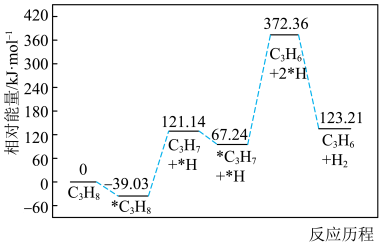
(1)丙烷直接催化脱氢。在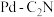 催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图所示(*表示催化剂表面吸附位点,如
催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图所示(*表示催化剂表面吸附位点,如 表示吸附在催化剂表面的
表示吸附在催化剂表面的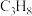 )。
)。 的
的
_______  。
。
②该反应历程共分五步,其中速率控制步骤为第_______ 步。
③研究表明,实际生产中除使用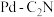 催化剂外,还需控制反应温度在
催化剂外,还需控制反应温度在 选择温度为
选择温度为 的原因是
的原因是_______ 。
(2) 氧化丙烷脱氢。
氧化丙烷脱氢。 下,将不同组分的原料混合气以相同流速通过装有催化剂的反应床,测得
下,将不同组分的原料混合气以相同流速通过装有催化剂的反应床,测得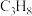 转化率和
转化率和 选择性(
选择性( 选择性
选择性 )随时间的变化关系如图所示,图中
)随时间的变化关系如图所示,图中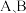 分别代表
分别代表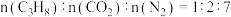 、
、 的两种原料气。
的两种原料气。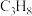 转化率和
转化率和 选择性均有所提升,且在反应床出口检测到
选择性均有所提升,且在反应床出口检测到 。研究表明,
。研究表明, 氧化丙烷脱氢经历了以下两个反应:Ⅰ.
氧化丙烷脱氢经历了以下两个反应:Ⅰ. ;Ⅱ.
;Ⅱ._______ 。(填化学方程式)
②反应进行至4小时后,B组分原料气的反应几乎无法进行,而A组分原料气的反应仍保持相对优异的稳定性,其可能原因是_______ 。
(3)丙烷燃料电池脱氢。一种质子导体燃料电池采用 材料作阳极催化层,在阳极侧注入燃料气
材料作阳极催化层,在阳极侧注入燃料气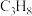 ,阴极侧直接暴露于空气中,在
,阴极侧直接暴露于空气中,在 下可实现丙烷高效脱氢制丙烯,装置如图所示。
下可实现丙烷高效脱氢制丙烯,装置如图所示。_______ 。
②与 氧化丙烷脱氢相比,丙烷燃料电池脱氢制丙烯工艺的优点是
氧化丙烷脱氢相比,丙烷燃料电池脱氢制丙烯工艺的优点是_______ 。
(1)丙烷直接催化脱氢。在
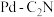 催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图所示(*表示催化剂表面吸附位点,如
催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图所示(*表示催化剂表面吸附位点,如 表示吸附在催化剂表面的
表示吸附在催化剂表面的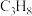 )。
)。
 的
的
 。
。②该反应历程共分五步,其中速率控制步骤为第
③研究表明,实际生产中除使用
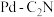 催化剂外,还需控制反应温度在
催化剂外,还需控制反应温度在 选择温度为
选择温度为 的原因是
的原因是(2)
 氧化丙烷脱氢。
氧化丙烷脱氢。 下,将不同组分的原料混合气以相同流速通过装有催化剂的反应床,测得
下,将不同组分的原料混合气以相同流速通过装有催化剂的反应床,测得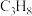 转化率和
转化率和 选择性(
选择性( 选择性
选择性 )随时间的变化关系如图所示,图中
)随时间的变化关系如图所示,图中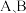 分别代表
分别代表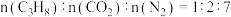 、
、 的两种原料气。
的两种原料气。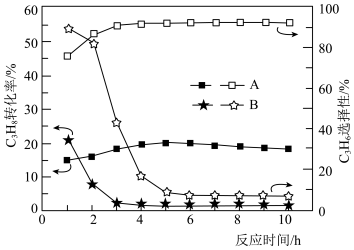
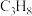 转化率和
转化率和 选择性均有所提升,且在反应床出口检测到
选择性均有所提升,且在反应床出口检测到 。研究表明,
。研究表明, 氧化丙烷脱氢经历了以下两个反应:Ⅰ.
氧化丙烷脱氢经历了以下两个反应:Ⅰ. ;Ⅱ.
;Ⅱ.②反应进行至4小时后,B组分原料气的反应几乎无法进行,而A组分原料气的反应仍保持相对优异的稳定性,其可能原因是
(3)丙烷燃料电池脱氢。一种质子导体燃料电池采用
 材料作阳极催化层,在阳极侧注入燃料气
材料作阳极催化层,在阳极侧注入燃料气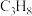 ,阴极侧直接暴露于空气中,在
,阴极侧直接暴露于空气中,在 下可实现丙烷高效脱氢制丙烯,装置如图所示。
下可实现丙烷高效脱氢制丙烯,装置如图所示。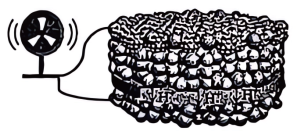
②与
 氧化丙烷脱氢相比,丙烷燃料电池脱氢制丙烯工艺的优点是
氧化丙烷脱氢相比,丙烷燃料电池脱氢制丙烯工艺的优点是
您最近一年使用:0次
10 . 草酸二甲酯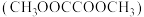 的热催化加氢是生产乙二醇
的热催化加氢是生产乙二醇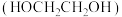 、乙醇酸甲酯
、乙醇酸甲酯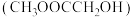 的重要工艺,主要反应如下:
的重要工艺,主要反应如下:
 .
.
 .
.
 .
.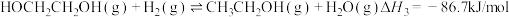
回答下列问题:
(1)草酸二甲酯热催化加氢生成乙二醇反应的 。
。
(2)计算表明,反应 在研究的温度范围内平衡常数大于
在研究的温度范围内平衡常数大于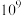 ,可以认为反应Ⅲ几乎不可逆,为了限制反应
,可以认为反应Ⅲ几乎不可逆,为了限制反应 对乙二醇产率的影响,可采取的最佳措施是___________(填标号)。
对乙二醇产率的影响,可采取的最佳措施是___________(填标号)。
(3)在选定催化剂后研究投料比和压强对反应平衡的影响。测得在 、
、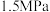 的等温等压条件下,原料草酸二甲酯的转化率
的等温等压条件下,原料草酸二甲酯的转化率 及产物的选择性
及产物的选择性 投料比的变化关系如图甲所示(
投料比的变化关系如图甲所示(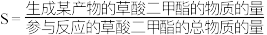 )。
)。___________ ;当投料比为60时,若草酸二甲酯的转化率为 ,且该条件下不发生反应
,且该条件下不发生反应 ,则最终收集的流出气中甲醇蒸气的分压为
,则最终收集的流出气中甲醇蒸气的分压为___________  (保留小数点后两位)。
(保留小数点后两位)。
(4)在等压 、投料比为50的条件下,
、投料比为50的条件下, 及各产物的选择性
及各产物的选择性 随温度变化关系如图乙所示。当反应温度高于
随温度变化关系如图乙所示。当反应温度高于 时,乙二醇的选择性降低,原因是
时,乙二醇的选择性降低,原因是___________ ;根据图乙数据,画出乙醇酸甲酯的产率随温度的变化图像___________ (标出产率最高时的数据)。
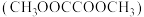 的热催化加氢是生产乙二醇
的热催化加氢是生产乙二醇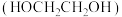 、乙醇酸甲酯
、乙醇酸甲酯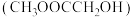 的重要工艺,主要反应如下:
的重要工艺,主要反应如下: .
.
 .
.
 .
.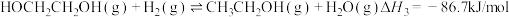
回答下列问题:
(1)草酸二甲酯热催化加氢生成乙二醇反应的
 。
。(2)计算表明,反应
 在研究的温度范围内平衡常数大于
在研究的温度范围内平衡常数大于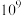 ,可以认为反应Ⅲ几乎不可逆,为了限制反应
,可以认为反应Ⅲ几乎不可逆,为了限制反应 对乙二醇产率的影响,可采取的最佳措施是___________(填标号)。
对乙二醇产率的影响,可采取的最佳措施是___________(填标号)。| A.升高反应体系的温度 | B.适当增大反应投料中氢气的比例 |
| C.增大反应体系的压强 | D.选择合适的催化剂进行反应 |
(3)在选定催化剂后研究投料比和压强对反应平衡的影响。测得在
 、
、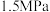 的等温等压条件下,原料草酸二甲酯的转化率
的等温等压条件下,原料草酸二甲酯的转化率 及产物的选择性
及产物的选择性 投料比的变化关系如图甲所示(
投料比的变化关系如图甲所示(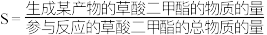 )。
)。
 ,且该条件下不发生反应
,且该条件下不发生反应 ,则最终收集的流出气中甲醇蒸气的分压为
,则最终收集的流出气中甲醇蒸气的分压为 (保留小数点后两位)。
(保留小数点后两位)。(4)在等压
 、投料比为50的条件下,
、投料比为50的条件下, 及各产物的选择性
及各产物的选择性 随温度变化关系如图乙所示。当反应温度高于
随温度变化关系如图乙所示。当反应温度高于 时,乙二醇的选择性降低,原因是
时,乙二醇的选择性降低,原因是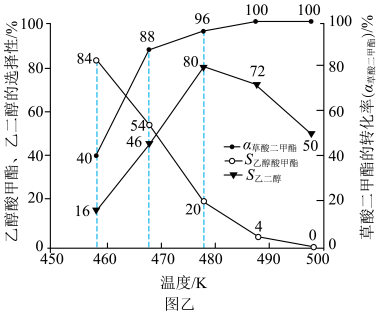
您最近一年使用:0次
昨日更新
|
63次组卷
|
2卷引用:山东省实验中学2024届高三下学期5月针对性考试化学试题



