解题方法
1 . 回答下列问题:
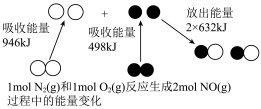
(1)汽车尾气中NO生成过程的能量变化如图所示。1molN2和1molO2完全反应生成NO会_______ (填“吸收”或“放出”)_______ kJ能量。 。已知增大催化剂的比表面积可提高反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
①表中a=_______ 。
②能验证温度对化学反应速率影响规律的是实验_______ (填实验编号)。
③实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线_______ (填“甲”或“乙”)。 ,不能说明该反应已达到平衡状态的是_______(填字母)。
,不能说明该反应已达到平衡状态的是_______(填字母)。
(1)汽车尾气中NO生成过程的能量变化如图所示。1molN2和1molO2完全反应生成NO会
 。已知增大催化剂的比表面积可提高反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。| 实验编号 | T/℃ | NO初始浓度/( ) ) | CO初始浓度/( ) ) | 催化剂的比表面积/(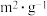 ) ) |
| I | 280 |  |  | 82 |
| II | 280 |  |  | 124 |
| III | 350 | a |  | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线

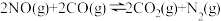 ,不能说明该反应已达到平衡状态的是_______(填字母)。
,不能说明该反应已达到平衡状态的是_______(填字母)。| A.容器内温度不再变化 |
| B.容器内的气体压强保持不变 |
| C.2v逆(NO)=v正(N2) |
| D.容器内混合气体的密度保持不变 |
您最近一年使用:0次
名校
解题方法
2 . 随着页岩气的成功开采,其重要成分丙烷成为了一种价廉的化工原料。工业上由丙烷制丙烯可采用直接脱氢: 或氧化脱氢:
或氧化脱氢: 。回答下列问题:
。回答下列问题:
(1)25°C、101kPa,丙烷、丙烯、氢气的燃烧热分别为 、
、 、
、 ,则直接脱氢反应
,则直接脱氢反应 的
的
______  ,该反应在
,该反应在______ (填“高温”“低温”或“任意温度”)条件下能自发进行。
(2) 催化下,丙烷直接脱氢反应历程与相对能量及活化能如下图所示(*表示吸附在催化剂表面的物种,TS表示过渡态,e、f未标注)。
催化下,丙烷直接脱氢反应历程与相对能量及活化能如下图所示(*表示吸附在催化剂表面的物种,TS表示过渡态,e、f未标注)。______ (填“路径1”或“路径2”),该路径的决速步是______ (填“b→c”“c→d”或“d→e”)。
②压强分别为0.1MPa和0.01MPa,平衡时丙烷和丙烯的物质的量分数与温度的关系如图所示。其中,表示0.1MPa时丙烯的物质的量分数的曲线是______ 。 和
和 ,发生直接脱氢和氧化脱氢反应,起始时容器内压强为
,发生直接脱氢和氧化脱氢反应,起始时容器内压强为 ,反应
,反应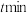 时达到平衡状态,测得丙烯(
时达到平衡状态,测得丙烯( )、CO的分压分别为
)、CO的分压分别为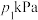 、
、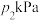 ,则
,则 内用丙烷表示的反应速率
内用丙烷表示的反应速率
______  ,用分压表示的丙烯氧化脱氢反应的平衡常数
,用分压表示的丙烯氧化脱氢反应的平衡常数
______  (用含
(用含 、
、 、
、 的计算式表示)。
的计算式表示)。
 或氧化脱氢:
或氧化脱氢: 。回答下列问题:
。回答下列问题:(1)25°C、101kPa,丙烷、丙烯、氢气的燃烧热分别为
 、
、 、
、 ,则直接脱氢反应
,则直接脱氢反应 的
的
 ,该反应在
,该反应在(2)
 催化下,丙烷直接脱氢反应历程与相对能量及活化能如下图所示(*表示吸附在催化剂表面的物种,TS表示过渡态,e、f未标注)。
催化下,丙烷直接脱氢反应历程与相对能量及活化能如下图所示(*表示吸附在催化剂表面的物种,TS表示过渡态,e、f未标注)。
②压强分别为0.1MPa和0.01MPa,平衡时丙烷和丙烯的物质的量分数与温度的关系如图所示。其中,表示0.1MPa时丙烯的物质的量分数的曲线是

 和
和 ,发生直接脱氢和氧化脱氢反应,起始时容器内压强为
,发生直接脱氢和氧化脱氢反应,起始时容器内压强为 ,反应
,反应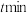 时达到平衡状态,测得丙烯(
时达到平衡状态,测得丙烯( )、CO的分压分别为
)、CO的分压分别为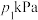 、
、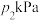 ,则
,则 内用丙烷表示的反应速率
内用丙烷表示的反应速率
 ,用分压表示的丙烯氧化脱氢反应的平衡常数
,用分压表示的丙烯氧化脱氢反应的平衡常数
 (用含
(用含 、
、 、
、 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
3 . 氮气转化为氮的化合物对于工业制备硝酸有着重要的意义。回答下列问题:
(1)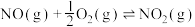
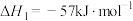


某反应的平衡常数表达式为 ,则该反应的热化学方程式为
,则该反应的热化学方程式为_______ 。
(2)已知反应 的速率方程为
的速率方程为 ,
,
 ,其中
,其中 、
、 是正、逆反应的速率常数,且只受温度影响,并随温度升高而增大。
是正、逆反应的速率常数,且只受温度影响,并随温度升高而增大。 时,在2L恒容密闭容器中充入
时,在2L恒容密闭容器中充入 气体发生反应
气体发生反应 ,不同时刻测得容器中
,不同时刻测得容器中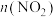 如下表所示:
如下表所示:
①1~4s该反应的平均速率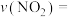
_______ 。
② 温度达到化学平衡时,该反应
温度达到化学平衡时,该反应
_______ 。
③若将容器的温度改为 ,其他条件不变,当
,其他条件不变,当 时,则
时,则
_______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(3)对于反应
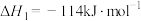 。保持其他初始条件不变,催化反应相同时间内测得NO转化率与温度的关系如图所示。随温度的升高,NO的转化率先增大后减小,理由是
。保持其他初始条件不变,催化反应相同时间内测得NO转化率与温度的关系如图所示。随温度的升高,NO的转化率先增大后减小,理由是_______ ;图中A点如果延长反应时间能_______ (填“提高”“降低”或“不影响”)NO转化率;图中B点如果增加 的浓度能
的浓度能_______ (填“提高”“降低”或“不影响”)NO转化率。
(1)
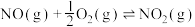
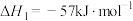


某反应的平衡常数表达式为
 ,则该反应的热化学方程式为
,则该反应的热化学方程式为(2)已知反应
 的速率方程为
的速率方程为 ,
,
 ,其中
,其中 、
、 是正、逆反应的速率常数,且只受温度影响,并随温度升高而增大。
是正、逆反应的速率常数,且只受温度影响,并随温度升高而增大。 时,在2L恒容密闭容器中充入
时,在2L恒容密闭容器中充入 气体发生反应
气体发生反应 ,不同时刻测得容器中
,不同时刻测得容器中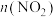 如下表所示:
如下表所示:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
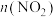 (mol) (mol) | 2.0 | 1.6 | 1.3 | 1.1 | 1.0 | 1.0 |
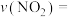
②
 温度达到化学平衡时,该反应
温度达到化学平衡时,该反应
③若将容器的温度改为
 ,其他条件不变,当
,其他条件不变,当 时,则
时,则
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(3)对于反应

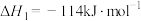 。保持其他初始条件不变,催化反应相同时间内测得NO转化率与温度的关系如图所示。随温度的升高,NO的转化率先增大后减小,理由是
。保持其他初始条件不变,催化反应相同时间内测得NO转化率与温度的关系如图所示。随温度的升高,NO的转化率先增大后减小,理由是 的浓度能
的浓度能
您最近一年使用:0次
4 . 按要求回答下列问题:
(1)下列变化属于吸热反应的是______ (填序号)。
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤ 固体溶于水
固体溶于水
(2)强酸与强碱的稀溶液发生中和反应生成1mol 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为______ 。(结果保留小数点后一位)
(3)已知1g 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为______ ,试写出该反应的热化学方程式为______ 。
(4)试比较反应热的大小:
①



则
______  (填“>”或“<”,下同)。
(填“>”或“<”,下同)。
②已知常温时红磷比白磷稳定。
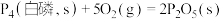

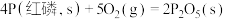

则
______  。
。
(5)已知:25℃、101kPa时,
①

②

③
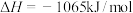
则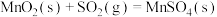

______ 。
(1)下列变化属于吸热反应的是
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤
 固体溶于水
固体溶于水(2)强酸与强碱的稀溶液发生中和反应生成1mol
 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为(3)已知1g
 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为(4)试比较反应热的大小:
①




则

 (填“>”或“<”,下同)。
(填“>”或“<”,下同)。②已知常温时红磷比白磷稳定。
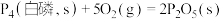

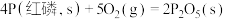

则

 。
。(5)已知:25℃、101kPa时,
①


②


③

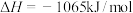
则

您最近一年使用:0次
2024-05-17更新
|
251次组卷
|
2卷引用:云南省临沧市沧源佤族自治县民族中学2022-2023学年高二上学期第一次月考化学试题
解题方法
5 . 选择性催化还原(SCR)脱硝技术可用于减少工业生产中氮氧化物( )的排放量,主要技术原理如下,回答下列问题:
)的排放量,主要技术原理如下,回答下列问题:
Ⅰ.CO―SCR技术
使用某催化剂时,反应机理如下表:
(1)反应

___________ ,副反应化学方程式为___________ 。
(2)将含NO的尾气按一定流速通到不同催化剂表面,不同温度下在气体出口处测得NO的转化率、 的选择性、
的选择性、 的生成量随温度变化关系如下图:
的生成量随温度变化关系如下图:___________ ,应选择的最佳催化剂为___________ ,选用合适的催化剂还能抑制催化剂表面出现铵盐结晶现象,结晶会导致___________ 。
Ⅱ.H2―SCR技术
主反应: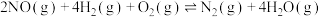
副反应:
(3)恒温下,向容积为1L的容器中充入2mol NO、4mol 、1mol
、1mol ,发生主、副反应,达到平衡后,测得压强为初始压强的
,发生主、副反应,达到平衡后,测得压强为初始压强的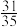 ,且
,且 与
与 的体积分数相等,NO的转化率为
的体积分数相等,NO的转化率为___________ ,主反应的
___________ (列出计算式即可)。
(4)除以上技术外,还可用电解纸化吸收法将工业尾气中的 转变为
转变为 。向
。向 NaCl溶液(起始pH调至9)中通入NO,测得电流强度与NO的去除率的关系如图甲所示,溶液中相关成分的浓度变化与电流强度的关系如图乙所示:
NaCl溶液(起始pH调至9)中通入NO,测得电流强度与NO的去除率的关系如图甲所示,溶液中相关成分的浓度变化与电流强度的关系如图乙所示:___________ ,随着电流强度的增大,电解NaCl溶液时NO去除率下降的原因是___________ 。
 )的排放量,主要技术原理如下,回答下列问题:
)的排放量,主要技术原理如下,回答下列问题:Ⅰ.CO―SCR技术
使用某催化剂时,反应机理如下表:
| 反应方程式 | 反应热 | |
| 吸附过程 | 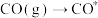 |  |
 |  | |
| 解离过程 |  |  |
| 缔结过程 | 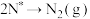 |  |
 |  | |
 | 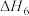 |
(1)反应


(2)将含NO的尾气按一定流速通到不同催化剂表面,不同温度下在气体出口处测得NO的转化率、
 的选择性、
的选择性、 的生成量随温度变化关系如下图:
的生成量随温度变化关系如下图: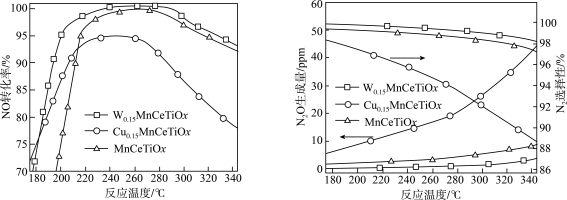
Ⅱ.H2―SCR技术
主反应:
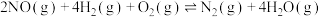
副反应:

(3)恒温下,向容积为1L的容器中充入2mol NO、4mol
 、1mol
、1mol ,发生主、副反应,达到平衡后,测得压强为初始压强的
,发生主、副反应,达到平衡后,测得压强为初始压强的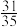 ,且
,且 与
与 的体积分数相等,NO的转化率为
的体积分数相等,NO的转化率为
(4)除以上技术外,还可用电解纸化吸收法将工业尾气中的
 转变为
转变为 。向
。向 NaCl溶液(起始pH调至9)中通入NO,测得电流强度与NO的去除率的关系如图甲所示,溶液中相关成分的浓度变化与电流强度的关系如图乙所示:
NaCl溶液(起始pH调至9)中通入NO,测得电流强度与NO的去除率的关系如图甲所示,溶液中相关成分的浓度变化与电流强度的关系如图乙所示:
您最近一年使用:0次
6 . 已知: 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、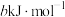 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为
 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、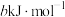 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为A. | B.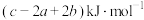 |
C.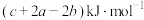 | D.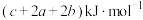 |
您最近一年使用:0次
7 . 图像更能直接地体现化学反应的伴随现象,如能量、速率、浓度等物理量的变化。下列说法错误的是

A.由图甲可知  , ,  ,则 ,则 |
B.图乙是在一定条件下,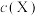 随时间t的变化,正反应 随时间t的变化,正反应 ,M点正反应速率<N点逆反应速率 ,M点正反应速率<N点逆反应速率 |
C.图丙所示反应的热化学方程式为 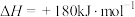 |
D.图丁中t时刻改变的条件可能是增大 的浓度,同时减小 的浓度,同时减小 的浓度 的浓度 |
您最近一年使用:0次
8 . 将 转化为
转化为 是含铅物质转化的重要途径。已知:
是含铅物质转化的重要途径。已知:
①

②

则反应 的
的 是
是
 转化为
转化为 是含铅物质转化的重要途径。已知:
是含铅物质转化的重要途径。已知:①


②


则反应
 的
的 是
是A. | B. |
C. | D. |
您最近一年使用:0次
9 . 我国科学家提出了由 和
和 直接转化为
直接转化为 的催化反应进程,该进程如图所示。则下列说法错误的是
的催化反应进程,该进程如图所示。则下列说法错误的是
 和
和 直接转化为
直接转化为 的催化反应进程,该进程如图所示。则下列说法错误的是
的催化反应进程,该进程如图所示。则下列说法错误的是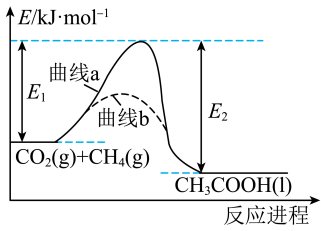
A.曲线对应总反应为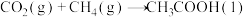 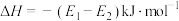 |
| B.曲线b对应的活化能小于曲线a对应的活化能 |
| C.曲线b代表使用催化剂时的能量变化曲线 |
| D.催化剂一定参与化学反应,从而改变了反应进程 |
您最近一年使用:0次
10 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的
___________  ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。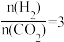 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为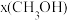 ,在
,在 ℃下的
℃下的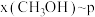 、在
、在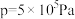 下的
下的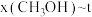 如图所示。
如图所示。
___________ ;
②图中对应等压过程的曲线是___________ ;
③当 时,
时, 的平衡转化率
的平衡转化率
___________ ,反应条件可能为___________ 或___________ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:

该反应一般认为通过如下步骤来实现:
①

②

总反应的

 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是A. 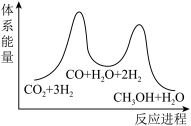 B.
B.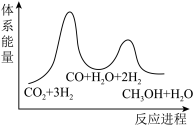
C. D.
D.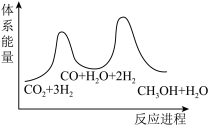
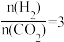 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为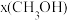 ,在
,在 ℃下的
℃下的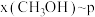 、在
、在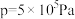 下的
下的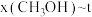 如图所示。
如图所示。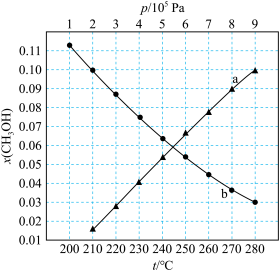

②图中对应等压过程的曲线是
③当
 时,
时, 的平衡转化率
的平衡转化率
您最近一年使用:0次



