名校
1 . 回答下列问题:
(1)(1)含有11.2 g KOH的稀溶液与1 L 0.1 mol·L-1的H2SO4溶液反应,放出11.46 kJ的热量,表示该反应中和热的热化学方程式为_______ 。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式_______ 。
(3)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1 648 kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393 kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1 480 kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是_______ 。
(4)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为_______ 。
(5)已知反应2HI(g)=H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
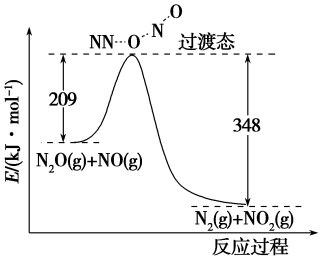
(6)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=_______ kJ·mol-1
(1)(1)含有11.2 g KOH的稀溶液与1 L 0.1 mol·L-1的H2SO4溶液反应,放出11.46 kJ的热量,表示该反应中和热的热化学方程式为
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1 648 kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393 kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1 480 kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是
(4)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为
(5)已知反应2HI(g)=H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为
(6)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=

您最近一年使用:0次
2021-10-15更新
|
66次组卷
|
2卷引用:黑龙江省肇东市第四中学2021-2022学年高二上学期期中考试化学试题
2 . 根据热化学的相关知识,进行填空:
(1)煤燃烧的反应热可通过以下两个途径计算得到:a.煤在充足的空气中直接燃烧;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程涉及的热化学方程式为
a.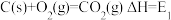 ①
①
b. ②
②
c.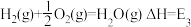 ③
③
d.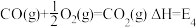 ④
④
E1、E2、E3、E4之间的关系可表示为E2=___________ ;
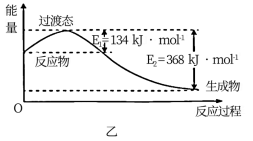
(2)图乙为常温常压下1molNO2和1molCO完全反应生成CO2和NO过程中的能量变化示意图,该反应为___________ (填“放热反应”或“吸热反应”);请写出NO2和CO反应的热化学方程式:___________ ;
(3)化学反应的焓变与反应物和生成物的键能有关。已知某些化学键的键能数据如下表所示:
则反应 的焓变
的焓变
___________ 。
(4)实验室用5mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定混合液温度升高的情况计算中和反应的反应热。

该装置缺少一种玻璃仪器,该仪器的名称为___________ ;实验室提供了0.50mol/L和0.55mol/L两种浓度的NaOH溶液,应选择___________ mol/L的溶液进行实验。
(1)煤燃烧的反应热可通过以下两个途径计算得到:a.煤在充足的空气中直接燃烧;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程涉及的热化学方程式为
a.
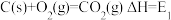 ①
①b.
 ②
②c.
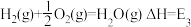 ③
③d.
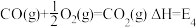 ④
④E1、E2、E3、E4之间的关系可表示为E2=
(2)图乙为常温常压下1molNO2和1molCO完全反应生成CO2和NO过程中的能量变化示意图,该反应为

(3)化学反应的焓变与反应物和生成物的键能有关。已知某些化学键的键能数据如下表所示:
| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ/mol) | 436 | 247 | 434 |
则反应
 的焓变
的焓变
(4)实验室用5mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定混合液温度升高的情况计算中和反应的反应热。

该装置缺少一种玻璃仪器,该仪器的名称为
您最近一年使用:0次
2021高三·全国·专题练习
名校
3 . 回答下列问题
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。
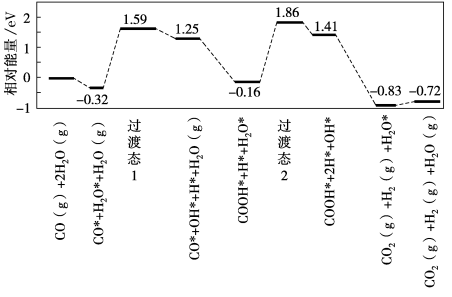
可知水煤气变换的ΔH___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV。
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是___________ 。
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用___________ 反应的ΔH。
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。

可知水煤气变换的ΔH
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用
您最近一年使用:0次
2021-08-18更新
|
1467次组卷
|
6卷引用:黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题
黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题(已下线)第15讲 化学反应的热效应(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷
4 . 某温度时,VIA元素单质与H2反应生成气态H2X的热化学方程式如下:
①H2(g)+ O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1
②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
(2)2gH2完全燃烧生成气态水,放出的热量为_______ 。
(3)请写出O2与H2S反应生成S的热化学方程式_______ 。
(4)根据下图写出热化学方程式_______ 。
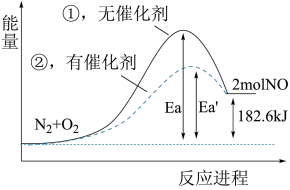
(5)加入催化剂该反应的反应热∆H是否发生了改变_______ (填“是”或“否”)。
(6)请写出H2燃烧热的热化学方程式_______ 。
①H2(g)+
 O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2gH2完全燃烧生成气态水,放出的热量为
(3)请写出O2与H2S反应生成S的热化学方程式
(4)根据下图写出热化学方程式

(5)加入催化剂该反应的反应热∆H是否发生了改变
(6)请写出H2燃烧热的热化学方程式
您最近一年使用:0次
名校
5 . 按要求书写下列方程式:
(1)制备粗硅的化学方程式___________ 。
(2)碱性锌锰干电池的正极反应式___________ 。
(3)用氢氧化钠溶液处理NO2尾气的化学方程式___________ 。
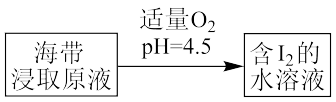
(4)海带提取碘下图所示步骤中反应的离子方程式___________ 。
(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式___________ 。
(1)制备粗硅的化学方程式
(2)碱性锌锰干电池的正极反应式
(3)用氢氧化钠溶液处理NO2尾气的化学方程式
(4)海带提取碘下图所示步骤中反应的离子方程式

(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式
您最近一年使用:0次
名校
6 . 氮的化合物种类繁多,性质也各不相同。请回答下列问题:
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=_______ 。
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
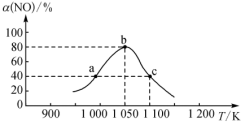
图中a、b、c三点中,达到平衡的点是_______ ;温度为1100K时,N2的平衡体积分数为_______ 。
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。
①实际生产中NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是_______ 。
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=_______ mol·L-1·min-1,500℃时该反应的平衡常数Kp=_______ MPa(用含p0的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。①实际生产中NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=
您最近一年使用:0次
2021-07-13更新
|
3549次组卷
|
8卷引用:黑龙江省大庆铁人中学2021-2022学年高二上学期开学考试化学试题
名校
解题方法
7 . 工业合成氨的反应N2+3H2=2NH3的能量变化如图所示,请回答有关问题:
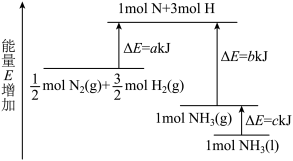
(1)合成1molNH3(l)___________ (填“吸收”或“放出”)___________ kJ的热量。(用字母表示)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为___________ kJ。
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)___________ (填“吸收”或“放出”)的热量___________ (填“多”或“少”)。

(1)合成1molNH3(l)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)
您最近一年使用:0次
2021-05-03更新
|
300次组卷
|
8卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题
黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题江西省南昌市八一中学、洪都中学等七校2020-2021学年高一下学期期中联考化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题江西省赣州市南康区第三中学2020-2021学年高一下学期期中考试化学试题山西省朔州市应县第一中学校2019-2020学年高一下学期期中考试化学试题(已下线)练习3 化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版)云南省昌宁县第一中学2021-2022学年高一 3月月考化学试题陕西省渭南市华州区咸林中学2022-2023学年高一下学期期中考试化学试题
8 . 某温度时,ⅥA元素单质与H2反应生成气态H2X的热化学方程式如下:
①H2(g)+ O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1
②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
请回答:
(1)上述反应中属于放热反应的是___________ (填序号,下同),属于吸热反应的是___________ 。
(2)2g H2完全燃烧生成气态水,放出的热量为___________ 。
(3)请写出O2与H2S反应生成S的热化学方程式___________ 。
(4)根据下图写出热化学方程式___________ 。
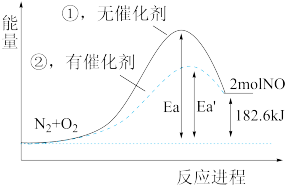
(5)加入催化剂该反应的反应热 H是否发生了改变
H是否发生了改变___________ (填“是”或“否”)。
①H2(g)+
 O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
请回答:
(1)上述反应中属于放热反应的是
(2)2g H2完全燃烧生成气态水,放出的热量为
(3)请写出O2与H2S反应生成S的热化学方程式
(4)根据下图写出热化学方程式

(5)加入催化剂该反应的反应热
 H是否发生了改变
H是否发生了改变
您最近一年使用:0次
2021-03-11更新
|
1410次组卷
|
4卷引用:黑龙江省大庆中学2020—2021学年高二上学期期末考试化学试题
9 . (1)已知:①NaHCO3(s)=NaHCO3(aq)△H=+18.81kJ·mol-1
②Na2CO3(s)=Na2CO2(aq)△H=-16.44 k J· mol-1
③2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(1)△H=+92.34kJ·mol-1
资料显示,NaHCO3固体加热到100℃发生分解,但是加热NaHCO3溶液不到80℃就有大量CO2气体放出。写出碳酸氢钠溶液分解的热化学方程式_______ ,并从反应热角度说明原因_________ 。
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s)⇌N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
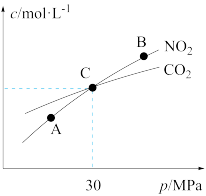
①A、B两点的浓度平衡常数关系:Kc(A)___________ Kc(B)(填“<”“>”或“=”)
②A、B、C三点中NO2的转化率最低的是___________ (填“A”“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=___________ (Kp是用平衡分压代替平衡浓度计算)
②Na2CO3(s)=Na2CO2(aq)△H=-16.44 k J· mol-1
③2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(1)△H=+92.34kJ·mol-1
资料显示,NaHCO3固体加热到100℃发生分解,但是加热NaHCO3溶液不到80℃就有大量CO2气体放出。写出碳酸氢钠溶液分解的热化学方程式
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s)⇌N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最低的是
③计算C点时该反应的压强平衡常数Kp(C)=
您最近一年使用:0次
名校
10 . 在某温度时,A+B⇌2C反应达到平衡。
(1)如果B为气态,增加体系的压强时,B的含量增加,则A为______ 态或______ 态,C为______ 态。
(2)如果升高温度,C的平衡浓度增大,则正反应方向是______ 热反应。
(3)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
H2O2(l)= H2O(l)+ 1/2O2(g) ΔH=-98.23kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______ 。
(1)如果B为气态,增加体系的压强时,B的含量增加,则A为
(2)如果升高温度,C的平衡浓度增大,则正反应方向是
(3)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
H2O2(l)= H2O(l)+ 1/2O2(g) ΔH=-98.23kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次



