名校
解题方法
1 . 工业上以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇。回答下列问题:
(1)已知:I.
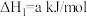
II.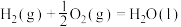
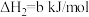
III.

则碳与水蒸气反应 的
的
_______ kJ/ mol(用含a、b、c的代数式表示)。
(2)工业上可以利用反应 得到的
得到的 和
和 进一步合成甲醇,反应方程式为
进一步合成甲醇,反应方程式为
 。
。
①工业生产过程中 的转化率
的转化率_______ (填“大于”“等于”或“小于”) 的转化率。
的转化率。
②为了提高甲醇的平衡产率可以采取的措施是_______ (填一条即可)。
(3)在一恒温恒容密闭容器中充人1 mol 和3 mol
和3 mol 进行上述合成甲醇的反应。测得
进行上述合成甲醇的反应。测得 和
和 的浓度随时间的变化如图所示:
的浓度随时间的变化如图所示:
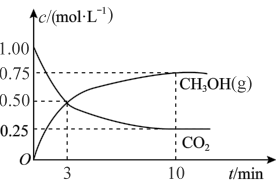
①3min时,v(正)_______ v(逆)(填“>”、“=”或“<”)
②该温度下的平衡常数为_______  (保留三位有效数字)。
(保留三位有效数字)。
(4)起始温度为 ℃时,在2L密闭容器中发生反应
℃时,在2L密闭容器中发生反应
 ,反应过程中部分数据如下表所示:
,反应过程中部分数据如下表所示:
①达到平衡时,反应I、II对比:平衡常数K(I)_______ (填“>”、“<”或“=”)K(II)。
②对于反应I,前10min内的平均反应速率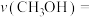
_______ mol/(L·min);若30min时向容器中再充入1 mol 和1 mol
和1 mol ,则平衡
,则平衡_______ (填“正向”、“逆向”或“不”)移动。
(1)已知:I.

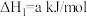
II.
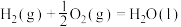
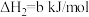
III.


则碳与水蒸气反应
 的
的
(2)工业上可以利用反应
 得到的
得到的 和
和 进一步合成甲醇,反应方程式为
进一步合成甲醇,反应方程式为
 。
。①工业生产过程中
 的转化率
的转化率 的转化率。
的转化率。②为了提高甲醇的平衡产率可以采取的措施是
(3)在一恒温恒容密闭容器中充人1 mol
 和3 mol
和3 mol 进行上述合成甲醇的反应。测得
进行上述合成甲醇的反应。测得 和
和 的浓度随时间的变化如图所示:
的浓度随时间的变化如图所示:
①3min时,v(正)
②该温度下的平衡常数为
 (保留三位有效数字)。
(保留三位有效数字)。(4)起始温度为
 ℃时,在2L密闭容器中发生反应
℃时,在2L密闭容器中发生反应
 ,反应过程中部分数据如下表所示:
,反应过程中部分数据如下表所示:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应I、II对比:平衡常数K(I)
②对于反应I,前10min内的平均反应速率
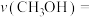
 和1 mol
和1 mol ,则平衡
,则平衡
您最近一年使用:0次
2 . 我国提出争取在2030年前实现碳峰值、2060年前实现碳中和,这对于改善环境、实现绿色发展至关重要。将CO2 转化为清洁能源是促进碳中和最直接有效的方法。
(1)H2还原CO2制取CH4的部分反应如下:
①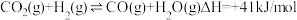
②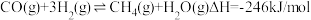
③
反应2C(s)+2H2O(g)=CH4(g)+CO2(g)的∆H=___________ kJ/mol。
(2)恒温条件下,向2L恒容密闭容器中充入1molCO和2molH2,只发生如下反应:CO(g)+3H2 (g)=CH4(g)+H2O(g),反应4min后,测得CO的物质的量为0.8mol,下列有关说法正确的是___________ (填字母。)
A. 利用合适的催化剂可增大该反应的平衡常数
B. 容器内气体的平均相对分子质量保持不变,说明该反应达到平衡状态
C. 用 H2表示该反应4min内的平均速率为0.075mol·L-1·s-1
D. 其它条件不变,升高温度,CO的平衡转化率降低
(3)在一定条件下,向某0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应:
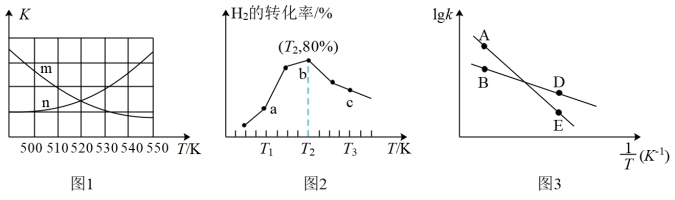
①图1中能表示该反应的平衡常数K与温度T之间的变化关系的是曲线___________ (填“m” 或“n”),判断依据是___________ 。
②若x=2、y=3,测得在相同时间内,不同温度下H 2的转化率如图2所示,v(a) 逆___________ v(c) 逆(填“>”、<”或“=”);T2时,起始压强为2.5MPa,则Kp=___________ MPa-2(保留二位小数;K p为以分压表示的平衡常数,分压=总压×物质的量分数)。
③已知速率方程 v正=k正·c(CO2)·c3(H2),v逆=k逆·c(CH3OH)·c(H2O),k正、k逆是速率常数,只受温度影响。图3表示速率常数的对数lgk与温度的倒数 之间的关系,A、B、D、E分别代表图2中a点、c点的lgk,其中表示c点的lgk逆的是
之间的关系,A、B、D、E分别代表图2中a点、c点的lgk,其中表示c点的lgk逆的是___________ (填“A”、“B”、“D”或“E”)。
(1)H2还原CO2制取CH4的部分反应如下:
①
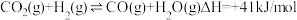
②
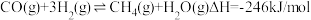
③

反应2C(s)+2H2O(g)=CH4(g)+CO2(g)的∆H=
(2)恒温条件下,向2L恒容密闭容器中充入1molCO和2molH2,只发生如下反应:CO(g)+3H2 (g)=CH4(g)+H2O(g),反应4min后,测得CO的物质的量为0.8mol,下列有关说法正确的是
A. 利用合适的催化剂可增大该反应的平衡常数
B. 容器内气体的平均相对分子质量保持不变,说明该反应达到平衡状态
C. 用 H2表示该反应4min内的平均速率为0.075mol·L-1·s-1
D. 其它条件不变,升高温度,CO的平衡转化率降低
(3)在一定条件下,向某0.5L恒容密闭容器中充入xmolCO2和ymolH2,发生反应:


①图1中能表示该反应的平衡常数K与温度T之间的变化关系的是曲线
②若x=2、y=3,测得在相同时间内,不同温度下H 2的转化率如图2所示,v(a) 逆
③已知速率方程 v正=k正·c(CO2)·c3(H2),v逆=k逆·c(CH3OH)·c(H2O),k正、k逆是速率常数,只受温度影响。图3表示速率常数的对数lgk与温度的倒数
 之间的关系,A、B、D、E分别代表图2中a点、c点的lgk,其中表示c点的lgk逆的是
之间的关系,A、B、D、E分别代表图2中a点、c点的lgk,其中表示c点的lgk逆的是
您最近一年使用:0次
2022-04-09更新
|
1123次组卷
|
6卷引用:湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题
湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题吉林省长春市2022届高三质量监测线上考试(三)理综化学试题(已下线)【奋进985】05-备战2022年高考化学名校进阶模拟卷(通用版)湖南省浏阳市第一中学2022届高三下学期期中考试化学试题江西省重点校2022-2023学年高三上学期第三次联考化学试题.(已下线)化学反应速率和化学平衡
3 . 含碳物质的价值型转化,有利于“减碳”和可持续发展。回答下列问题:
(1)科学家用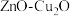 做催化剂,可将
做催化剂,可将 和
和 转化为甲烷。已知有关化学反应的能量变化如图所示,则该转化反应的热化学方程式为
转化为甲烷。已知有关化学反应的能量变化如图所示,则该转化反应的热化学方程式为___________ 。

(2)用惰性电极电解 溶液,可将空气中的
溶液,可将空气中的 转化为甲酸根(
转化为甲酸根( ),然后进一步可制得化工原料甲酸。
),然后进一步可制得化工原料甲酸。 发生反应的电极反应式为
发生反应的电极反应式为___________ ,若电解过程中转移1mol电子,阳极生成氧气的体积(标准状况)为___________ L。
(3)乙苯催化脱氢制取苯乙烯的反应为: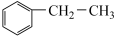 (g)+CO2(g)
(g)+CO2(g)
 (g)+H2O(g)+CO(g),其反应历程如下:
(g)+H2O(g)+CO(g),其反应历程如下:
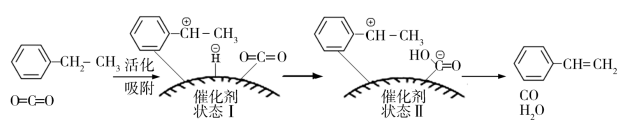
①由原料到“状态Ⅰ”___________ (填“放出”或“吸收”)能量。
②一定温度下,向恒容密闭容器中充入2mol乙苯和 ,起始压强为
,起始压强为 ,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
,平衡时容器内气体总物质的量为5mol,乙苯的转化率为___________ ,用平衡分压代替平衡浓度表示的化学平衡常数
___________ 。
③乙苯平衡转化率与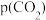 的关系如图所示,乙苯平衡转化率随着
的关系如图所示,乙苯平衡转化率随着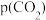 变化的原因是
变化的原因是___________ 。

(1)科学家用
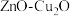 做催化剂,可将
做催化剂,可将 和
和 转化为甲烷。已知有关化学反应的能量变化如图所示,则该转化反应的热化学方程式为
转化为甲烷。已知有关化学反应的能量变化如图所示,则该转化反应的热化学方程式为
(2)用惰性电极电解
 溶液,可将空气中的
溶液,可将空气中的 转化为甲酸根(
转化为甲酸根( ),然后进一步可制得化工原料甲酸。
),然后进一步可制得化工原料甲酸。 发生反应的电极反应式为
发生反应的电极反应式为(3)乙苯催化脱氢制取苯乙烯的反应为:
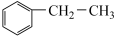 (g)+CO2(g)
(g)+CO2(g)
 (g)+H2O(g)+CO(g),其反应历程如下:
(g)+H2O(g)+CO(g),其反应历程如下:
①由原料到“状态Ⅰ”
②一定温度下,向恒容密闭容器中充入2mol乙苯和
 ,起始压强为
,起始压强为 ,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
③乙苯平衡转化率与
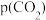 的关系如图所示,乙苯平衡转化率随着
的关系如图所示,乙苯平衡转化率随着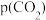 变化的原因是
变化的原因是
您最近一年使用:0次
解题方法
4 . 2017年5月18日中共中央国务院公开致电祝贺南海北部神狐海域进行的“可燃冰”试采成功。“可燃冰”是天然气水合物,外形像冰,在常温常压下迅速分解释放出甲烷,被称为未来新能源。
(1)“可燃冰”作为能源的优点是__________ (回答一条即可)。
(2)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷,氧气和水蒸气,发生的主要化学反应如下:
回答下列问题:
①在初始阶段,甲烷蒸汽重整的反应速率______ (填“大于”“小于”或“等于”)甲烷氧化的反应速率。
②反应CH4(g)+H2O(g) CO(g)+3H2(g) 的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g) 的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。

该反应在图中A点的平衡常数Kp=________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),图中压强(p1、p2、p3、p4)由大到小的顺序为___________ 。
③从能量角度分析,甲烷自热重整方法的先进之处在于___________ 。
④如果进料中氧气量过大,最终会导致H2物质量分数降低,原因是__________ 。
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和开境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。

①过程II中第二步反应的化学方程式为_____________ 。
②只有过程I投料比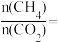
_______ ,过程II中催化剂组成才会保持不变。
③该技术总反应的热化学方程式为______________ 。
(1)“可燃冰”作为能源的优点是
(2)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷,氧气和水蒸气,发生的主要化学反应如下:
| 反应过程 | 化学方程式 | 焓变△H(kJ.mol-l) | 活化能E.(kJ.mol-1) |
| 甲烷氧化 | CH4(g)+  O2(g) O2(g)  CO2(g)+2H2O(g) CO2(g)+2H2O(g) | -802.6 | 125.6 |
CH4(g)+O2(g)  CO2(g)+2H2(g) CO2(g)+2H2(g) | -322.0 | 172. 5 | |
| 蒸气重整 | CH4(g)+H2O(g)  CO(g)+3H2(g) CO(g)+3H2(g) | +206.2 | 240.1 |
CH4(g)+2H2O(g)  CO2(g)+4H2(g) CO2(g)+4H2(g) | + 158. 6 | 243.9 |
①在初始阶段,甲烷蒸汽重整的反应速率
②反应CH4(g)+H2O(g)
 CO(g)+3H2(g) 的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g) 的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
该反应在图中A点的平衡常数Kp=
③从能量角度分析,甲烷自热重整方法的先进之处在于
④如果进料中氧气量过大,最终会导致H2物质量分数降低,原因是
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和开境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。

①过程II中第二步反应的化学方程式为
②只有过程I投料比
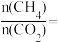
③该技术总反应的热化学方程式为
您最近一年使用:0次
2018-02-05更新
|
1022次组卷
|
2卷引用:湖北省十堰市2018届高三元月调研考试理综化学试题
名校
5 . 2017年5月18日,中国国土资源部地质调查局宣布,我国在南海进行的可燃冰试采获得成功,成为全球第一个海域试采可燃冰成功的国家,可燃冰即天然气水合物,甲烷含量占80%至99.9%。化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇或合成氨,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g)=CO(g)+2H2(g) △H1=-36kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,每生产lmolCO,转移电子的数目为__________ 。
(2)甲醇是一种用途广泛的化工原料,工业上常用下列两种反应制备甲醇:
CO(g)+2H2(g)=CH3OH(g) △H1=-90kJ·mol-1K1
CO2(g)+3H2(g)= CH3OH(g)+H2O(l) △H2K2
已知: CO(g)+H2O(g)= CO2(g)+H2(g) △H3=-41.1kJ·mol-1K3
H2O(l)=H2O(g) △H4=+44.0kJ·mol-1K4
则△H2=______ K2=_______ (用含K1、K3、K 4的代数式表示)
(3)在一恒温恒容密闭容器中充入1molCO2和3molH2模拟工业合成甲醇的反应:CO2(g)十3H2(g) CH3OH(g)十H2O(g)
CH3OH(g)十H2O(g)
①下列能说明该反应已达到平衡状态的是______________________ 。
A.混合气体平均相对分子质量不变 B.混合气体密度不变
C.容器内压强恒定不变 D.反应速率满足以下关系:V正(CO2)=3V逆(H2)
E.CO2、H2、CH3OH、H2O物质的量浓度之比为1:3:1:1
F.单位时间内断裂3NAH-H键的同时形成2molH-O键
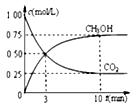
②模拟过程中测得CO2和CH3OH(g)浓度随时间变化如图所示,若此时容器内压强为P,则用平衡分压代替平衡浓度表示的化学平衡常数KP为_____________ (用含P的代数式表示,数值保留两位小数),若此时再向容器内充入0.25molCO2和0.25molCH3OH的混合气体,则平衡______ (填“正向“逆向“不”)移动。(已知:气体分压=气体总压×体积分数)
(4)甲醇可在电解银催化作用下制甲醛,从贵金属阳极泥中可提取“粗银”“粗银”(含Ag、Cu、Au)可用电解槽电解精炼,纯银作阴极,采用AgNO3和稀HNO3的混合液作电解液,阴极的主要电极反应式为_____ 。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为_______ 。硝酸浓度不能过大,其原因是___________________________________________ 。
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g)=CO(g)+2H2(g) △H1=-36kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,每生产lmolCO,转移电子的数目为
(2)甲醇是一种用途广泛的化工原料,工业上常用下列两种反应制备甲醇:
CO(g)+2H2(g)=CH3OH(g) △H1=-90kJ·mol-1K1
CO2(g)+3H2(g)= CH3OH(g)+H2O(l) △H2K2
已知: CO(g)+H2O(g)= CO2(g)+H2(g) △H3=-41.1kJ·mol-1K3
H2O(l)=H2O(g) △H4=+44.0kJ·mol-1K4
则△H2=
(3)在一恒温恒容密闭容器中充入1molCO2和3molH2模拟工业合成甲醇的反应:CO2(g)十3H2(g)
 CH3OH(g)十H2O(g)
CH3OH(g)十H2O(g)①下列能说明该反应已达到平衡状态的是
A.混合气体平均相对分子质量不变 B.混合气体密度不变
C.容器内压强恒定不变 D.反应速率满足以下关系:V正(CO2)=3V逆(H2)
E.CO2、H2、CH3OH、H2O物质的量浓度之比为1:3:1:1
F.单位时间内断裂3NAH-H键的同时形成2molH-O键
②模拟过程中测得CO2和CH3OH(g)浓度随时间变化如图所示,若此时容器内压强为P,则用平衡分压代替平衡浓度表示的化学平衡常数KP为

(4)甲醇可在电解银催化作用下制甲醛,从贵金属阳极泥中可提取“粗银”“粗银”(含Ag、Cu、Au)可用电解槽电解精炼,纯银作阴极,采用AgNO3和稀HNO3的混合液作电解液,阴极的主要电极反应式为
您最近一年使用:0次
名校
解题方法
6 . CO是现代化工生产的基础原料,下列有关问题都和CO的使用有关。
(1)工业上可利用CO生产乙醇:
2CO(g)+4H2(g)⇌CH3CH2OH(g)+H2O(g) ΔH1
又已知:H2O(l)= H2O(g) ΔH2
CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(l) ΔH
则:ΔH与ΔH1、ΔH2、ΔH3之间的关系是:ΔH=_______________________ 。
(2)一定条件下,H2、CO在体积固定的密闭容器中发生如下反应:
4H2(g)+2CO(g)⇌CH3OCH3(g)+H2O(g),
下列选项能判断该反应达到平衡状态的依据的有____。
(3)工业可采用CO与H2反应合成再生能源甲醇,反应如下:
CO(g)+ 2H2(g) CH3OH(g)
CH3OH(g)
在一容积可变的密闭容器中充有10molCO和20mol H2,
在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如(图1)所示。
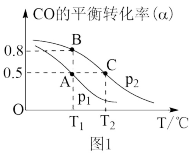
①合成甲醇的反应为_____ (填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为_________ 。
③若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为______________ L。
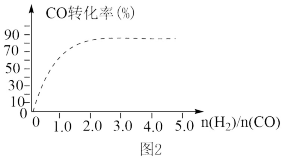
④(图2)中虚线为该反应在使用催化剂条件下关于起始氢气与CO投料比和CO平衡转化率的关系图。当其条件完全相同时,用实线画出不使用催化剂情况下CO平衡转化率的示意图______________ .
⑤CO的平衡转化率(α)与温度(T)、压强(p)的关系如(图3)所示,实际生产时条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是________ 。

(1)工业上可利用CO生产乙醇:
2CO(g)+4H2(g)⇌CH3CH2OH(g)+H2O(g) ΔH1
又已知:H2O(l)= H2O(g) ΔH2
CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(l) ΔH
则:ΔH与ΔH1、ΔH2、ΔH3之间的关系是:ΔH=
(2)一定条件下,H2、CO在体积固定的密闭容器中发生如下反应:
4H2(g)+2CO(g)⇌CH3OCH3(g)+H2O(g),
下列选项能判断该反应达到平衡状态的依据的有____。
| A.2v(H2)= v(CO) |
| B.CO的消耗速率等于CH3OCH3的生成速率 |
| C.容器内的压强保持不变 |
| D.混合气体的密度保持不变 |
| E.混合气体的平均相对分子质量不随时间而变化 |
CO(g)+ 2H2(g)
 CH3OH(g)
CH3OH(g)在一容积可变的密闭容器中充有10molCO和20mol H2,
在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如(图1)所示。

①合成甲醇的反应为
②A、B、C三点的平衡常数KA、KB、KC的大小关系为
③若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为
④(图2)中虚线为该反应在使用催化剂条件下关于起始氢气与CO投料比和CO平衡转化率的关系图。当其条件完全相同时,用实线画出不使用催化剂情况下CO平衡转化率的示意图

⑤CO的平衡转化率(α)与温度(T)、压强(p)的关系如(图3)所示,实际生产时条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是

您最近一年使用:0次
2016-12-09更新
|
1018次组卷
|
3卷引用:2015-2016学年湖北武汉第二中学高二上期中考试化学试卷



