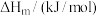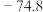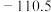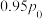名校
解题方法
1 . 除去废水中Cr(Ⅵ)的方法有多种。请按要求回答下列问题。
(1)室温下,含Cr(Ⅵ)的微粒在水溶液中存在如下平衡:
H2CrO4(aq) H+(aq)+
H+(aq)+ (aq) ΔH1
(aq) ΔH1
 (aq)
(aq) H+(aq)+
H+(aq)+ (aq) ΔH2
(aq) ΔH2
2 (aq)
(aq) H2O(l)+
H2O(l)+ (aq) ΔH3
(aq) ΔH3
①室温下,反应2 (aq)+2H+(aq)
(aq)+2H+(aq)
 (aq)+H2O(l)的ΔH=
(aq)+H2O(l)的ΔH=___________ (用含ΔH1、ΔH2或ΔH3的代数式表示)。
②室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c( )随c(H+)的变化如图。
)随c(H+)的变化如图。 +2H+
+2H+
 +H2O的K=
+H2O的K=___________ ,下列关于该反应的说法正确的是___________ 。
A.加水稀释,平衡正向移动
B.若达到A点的时间为5s,则v( )=0.1mol/(L·s)
)=0.1mol/(L·s)
C.若升高温度,溶液中 的平衡转化率减小,则该反应的ΔH>0
的平衡转化率减小,则该反应的ΔH>0
(2)NaHSO3与熟石灰除Cr(Ⅵ)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
①实验中的NaHSO3作用是___________ 。
②Cr(Ⅲ)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(Ⅲ)去除率下降的原因可用离子方程式表示为___________ 。
①用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)的废水时,Cr(Ⅵ)去除率随温度的变化如图2所示。55℃时,Cr(Ⅵ)的去除率很低的原因是___________ 。___________ 。
(1)室温下,含Cr(Ⅵ)的微粒在水溶液中存在如下平衡:
H2CrO4(aq)
 H+(aq)+
H+(aq)+ (aq) ΔH1
(aq) ΔH1 (aq)
(aq) H+(aq)+
H+(aq)+ (aq) ΔH2
(aq) ΔH22
 (aq)
(aq) H2O(l)+
H2O(l)+ (aq) ΔH3
(aq) ΔH3①室温下,反应2
 (aq)+2H+(aq)
(aq)+2H+(aq)
 (aq)+H2O(l)的ΔH=
(aq)+H2O(l)的ΔH=②室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(
 )随c(H+)的变化如图。
)随c(H+)的变化如图。
 +2H+
+2H+
 +H2O的K=
+H2O的K=A.加水稀释,平衡正向移动
B.若达到A点的时间为5s,则v(
 )=0.1mol/(L·s)
)=0.1mol/(L·s)C.若升高温度,溶液中
 的平衡转化率减小,则该反应的ΔH>0
的平衡转化率减小,则该反应的ΔH>0(2)NaHSO3与熟石灰除Cr(Ⅵ)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
①实验中的NaHSO3作用是
②Cr(Ⅲ)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(Ⅲ)去除率下降的原因可用离子方程式表示为
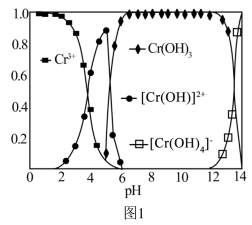
①用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)的废水时,Cr(Ⅵ)去除率随温度的变化如图2所示。55℃时,Cr(Ⅵ)的去除率很低的原因是

您最近一年使用:0次
7日内更新
|
111次组卷
|
3卷引用:湖北省武昌实验中学2023届高三下学期高考适应性考试化学试题
2 . 近两年来,碳中和连续成为两会期间最受关注的议题之一, 的回收和利用对于改善环境,实现绿色发展至关重要。
的回收和利用对于改善环境,实现绿色发展至关重要。
(1) 甲烷化反应最早由化学家PaulSabatier提出。已知:
甲烷化反应最早由化学家PaulSabatier提出。已知:
反应Ⅰ.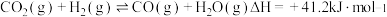
反应Ⅱ.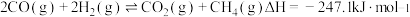
① 的结构式为
的结构式为_______ 。
② 甲烷化反应是
甲烷化反应是_______ (填“吸热”或“放热”)反应。
③反应Ⅰ的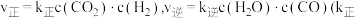 和
和 为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
_______ (填“增大”、“不变”或“减小”)。
(2)一定条件下, 与
与 反应可合成乙烯:
反应可合成乙烯: 。该反应分两步进行:
。该反应分两步进行:
ⅰ.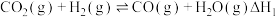
ⅱ.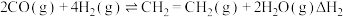
 ,压强恒定为
,压强恒定为 时,将
时,将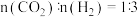 的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。
的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。
 的平衡转化率为
的平衡转化率为_______ ,反应ⅰ的平衡常数
_______ ( 是以分压表示的平衡常数,分压
是以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(3)一种以 和甲醇为原料,利用
和甲醇为原料,利用 和
和 纳米片
纳米片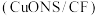 作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。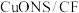 为
为_______ 极,电解过程中阴极的电极反应式为_______ 。
②设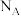 为阿伏加德罗常数的值,当电路中转移
为阿伏加德罗常数的值,当电路中转移 电子时,装置中生成
电子时,装置中生成 和
和 的数目共为
的数目共为_______ 。
 的回收和利用对于改善环境,实现绿色发展至关重要。
的回收和利用对于改善环境,实现绿色发展至关重要。(1)
 甲烷化反应最早由化学家PaulSabatier提出。已知:
甲烷化反应最早由化学家PaulSabatier提出。已知:反应Ⅰ.
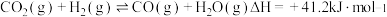
反应Ⅱ.
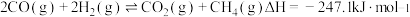
①
 的结构式为
的结构式为②
 甲烷化反应是
甲烷化反应是③反应Ⅰ的
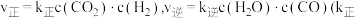 和
和 为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
(2)一定条件下,
 与
与 反应可合成乙烯:
反应可合成乙烯: 。该反应分两步进行:
。该反应分两步进行:ⅰ.
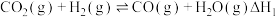
ⅱ.
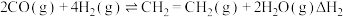
 ,压强恒定为
,压强恒定为 时,将
时,将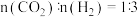 的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。
的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。| 组分 |  |  |  |
物质的量分数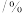 | 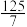 | 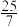 | 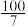 |
 的平衡转化率为
的平衡转化率为
 是以分压表示的平衡常数,分压
是以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。(3)一种以
 和甲醇为原料,利用
和甲醇为原料,利用 和
和 纳米片
纳米片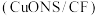 作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。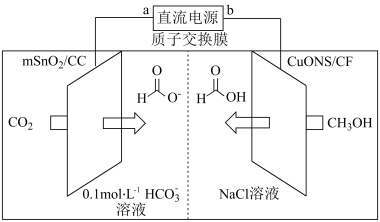
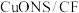 为
为②设
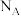 为阿伏加德罗常数的值,当电路中转移
为阿伏加德罗常数的值,当电路中转移 电子时,装置中生成
电子时,装置中生成 和
和 的数目共为
的数目共为
您最近一年使用:0次
名校
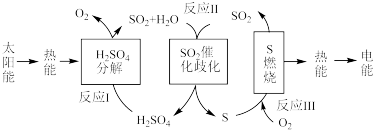
3 . 新质生产力本身就是绿色生产力,开展绿色低碳技术攻关,实现“双碳”目标, 催化加氢的主要过程包括如下反应:
催化加氢的主要过程包括如下反应:
 .
.
 kJ⋅mol
kJ⋅mol
 .
.
 kJ⋅mol
kJ⋅mol
 .
.

回答下列问题:
(1)利用焦炉气中的 作为原料,需要清除其中的硫化物,其目的是
作为原料,需要清除其中的硫化物,其目的是___________ 。
(2)
___________ kJ⋅mol 。
。
(3)温度对上述化学反应平衡常数的影响如图所示,其中 对应的曲线是
对应的曲线是___________ (填标号)。 作催化剂的条件下,以
作催化剂的条件下,以 的原料比通入反应物,
的原料比通入反应物, 的转化率和
的转化率和 的选择性随温度的变化如图所示[甲醇的选择性
的选择性随温度的变化如图所示[甲醇的选择性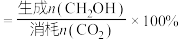 ]。
]。 的选择性下降,可能的原因是
的选择性下降,可能的原因是___________ 。
②200∼280°C范围内随温度升高, 的产率先增大后减小,其原因是
的产率先增大后减小,其原因是___________ 。
③P点时, 的分压是
的分压是___________ MPa,
___________ 。
 催化加氢的主要过程包括如下反应:
催化加氢的主要过程包括如下反应: .
.
 kJ⋅mol
kJ⋅mol
 .
.
 kJ⋅mol
kJ⋅mol
 .
.

回答下列问题:
(1)利用焦炉气中的
 作为原料,需要清除其中的硫化物,其目的是
作为原料,需要清除其中的硫化物,其目的是(2)

 。
。(3)温度对上述化学反应平衡常数的影响如图所示,其中
 对应的曲线是
对应的曲线是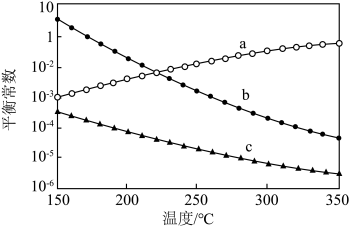
 作催化剂的条件下,以
作催化剂的条件下,以 的原料比通入反应物,
的原料比通入反应物, 的转化率和
的转化率和 的选择性随温度的变化如图所示[甲醇的选择性
的选择性随温度的变化如图所示[甲醇的选择性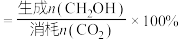 ]。
]。
 的选择性下降,可能的原因是
的选择性下降,可能的原因是②200∼280°C范围内随温度升高,
 的产率先增大后减小,其原因是
的产率先增大后减小,其原因是③P点时,
 的分压是
的分压是
您最近一年使用:0次
解题方法
4 . 甲烷干重整反应可以强化碳酸钙分解.
I.碳酸钙分解: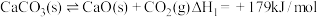
Ⅱ.甲烷干重整: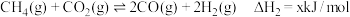
(1)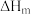 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
___________ .
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.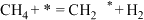 Ⅱ.
Ⅱ.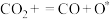
Ⅲ.___________ IV. V.
V.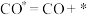
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量 和
和 ;
;
①下列能说明反应达到平衡状态的是___________ (填字母);
a. b.
b. 和
和 的体积比保持不变
的体积比保持不变
c.每生成 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变
②反应达到平衡时, 的转化率为
的转化率为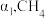 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
___________ ;(用含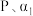 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下: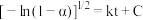 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在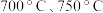 得到的
得到的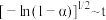 的曲线如图所示:
的曲线如图所示: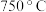 的曲线是曲线
的曲线是曲线___________ ,用碰撞理论解释原因___________ ;
(5)在某温度下,催化剂活性良好,加入一定量的 ,通入
,通入 ,和
,和 的流速为
的流速为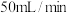 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是___________ 。
I.碳酸钙分解:
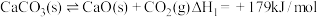
Ⅱ.甲烷干重整:
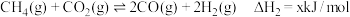
(1)
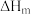 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
|
|
|
| |
|
|
|
| 0 |
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.
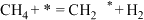 Ⅱ.
Ⅱ.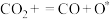
Ⅲ.
 V.
V.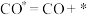
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量
 和
和 ;
;①下列能说明反应达到平衡状态的是
a.
 b.
b. 和
和 的体积比保持不变
的体积比保持不变c.每生成
 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变②反应达到平衡时,
 的转化率为
的转化率为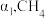 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
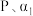 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下:
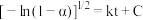 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在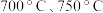 得到的
得到的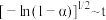 的曲线如图所示:
的曲线如图所示: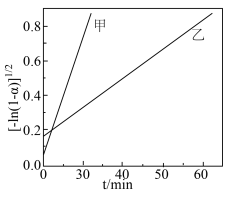
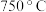 的曲线是曲线
的曲线是曲线(5)在某温度下,催化剂活性良好,加入一定量的
 ,通入
,通入 ,和
,和 的流速为
的流速为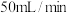 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是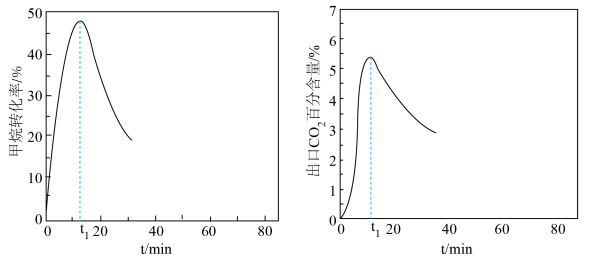
您最近一年使用:0次
名校
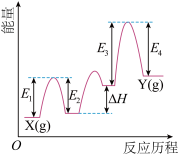
5 . (Ⅰ)铬及其化合物在催化、金属防腐等方面具有重要应用。 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为___ (列式表示)。
(2)该反应
_______ 0(填“>”或“=”或“<”)。
(Ⅱ)2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(3)火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。已知:①
和水蒸气。已知:①
 kJ/mol②
kJ/mol②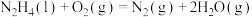
 kJ/mol请写出
kJ/mol请写出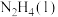 与
与 反应的热化学方程式
反应的热化学方程式_______ 。③
 ,
, 与
与 进行大小比较:
进行大小比较:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)二甲醚( )是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和
)是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和 合成二甲醚的反应为:
合成二甲醚的反应为:
 kJ/mol。
kJ/mol。
①改变下列“量”,一定会引起 发生变化的是
发生变化的是_______ (填代号)。
a.化学计量数 b.反应物浓度 c.催化剂
②采用新型催化剂(主要成分是Cu-Mn的合金)制备二甲醚。催化剂中 对合成二甲醚的影响情况如下图所示。当
对合成二甲醚的影响情况如下图所示。当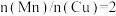 时,二甲醚的选择性(选择性
时,二甲醚的选择性(选择性 )为85.8%,此时二甲醚的产率为
)为85.8%,此时二甲醚的产率为_______ 。(保留3位有效数字)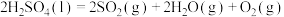
 kJ·mol
kJ·mol
反应III:
 kJ·mol
kJ·mol
在反应Ⅱ中,若标准状况下有33.6 L 气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为
气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为______ kJ。
 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为(2)该反应

(Ⅱ)2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(3)火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。已知:①
和水蒸气。已知:①
 kJ/mol②
kJ/mol②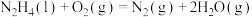
 kJ/mol请写出
kJ/mol请写出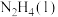 与
与 反应的热化学方程式
反应的热化学方程式
 ,
, 与
与 进行大小比较:
进行大小比较:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)二甲醚(
 )是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和
)是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和 合成二甲醚的反应为:
合成二甲醚的反应为:
 kJ/mol。
kJ/mol。①改变下列“量”,一定会引起
 发生变化的是
发生变化的是a.化学计量数 b.反应物浓度 c.催化剂
②采用新型催化剂(主要成分是Cu-Mn的合金)制备二甲醚。催化剂中
 对合成二甲醚的影响情况如下图所示。当
对合成二甲醚的影响情况如下图所示。当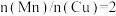 时,二甲醚的选择性(选择性
时,二甲醚的选择性(选择性 )为85.8%,此时二甲醚的产率为
)为85.8%,此时二甲醚的产率为 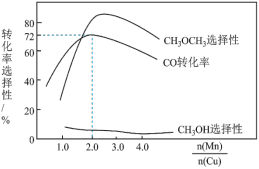
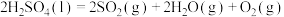
 kJ·mol
kJ·mol
反应III:

 kJ·mol
kJ·mol
在反应Ⅱ中,若标准状况下有33.6 L
 气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为
气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为
您最近一年使用:0次
6 . 环氧乙烷( ,简称
,简称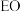 )是有机合成常用的试剂。
)是有机合成常用的试剂。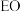 常温下易燃易爆,其爆炸极限为
常温下易燃易爆,其爆炸极限为 。工业上常用乙烯、氧气、氮气混合气投料的乙烯氧化法制备
。工业上常用乙烯、氧气、氮气混合气投料的乙烯氧化法制备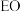 。涉及反应有:
。涉及反应有:

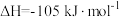
副反应:

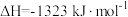
(1)主反应的活化能
 (正)
(正) (逆)(填“>”、“<”或“=”)。
(逆)(填“>”、“<”或“=”)。(2)已知
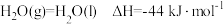 ,则
,则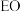 的燃烧热为
的燃烧热为
 。
。(3)在温度为T,压强为
 的环境下,欲提高乙烯的平衡转化率,理论上需
的环境下,欲提高乙烯的平衡转化率,理论上需(4)以Ag为催化剂的反应机理如下:
反应I:
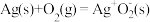 慢
慢反应Ⅱ:
 快
快反应Ⅲ:
 快
快①一定能够提高主反应反应速率的措施有
A.移出
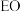 B.增大
B.增大 浓度 C.降低温度 D.增大
浓度 C.降低温度 D.增大 浓度
浓度②加入
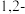 二氯乙烷会发生反应
二氯乙烷会发生反应 。一定条件下,反应经过一定时间后,
。一定条件下,反应经过一定时间后,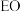 产率及选择性[
产率及选择性[ ]与
]与 二氯乙烷浓度关系如图。
二氯乙烷浓度关系如图。
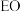 产率先增加后降低的原因可能是
产率先增加后降低的原因可能是(5)一定温度下,假定体系内只发生主反应,设
 的平衡分压为p,
的平衡分压为p, 的平衡转化率为x,用含p和x的代数式表示主反应的
的平衡转化率为x,用含p和x的代数式表示主反应的
您最近一年使用:0次
2024-04-29更新
|
52次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
7 . 氙及其化合物在工业生产中有重要用途。
(1)1962年,化学家巴特利特合成了氙的第一个化合物 ,其在熔化时电离出
,其在熔化时电离出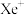 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为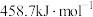 。
。
②Xe的第一电离能为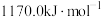 。
。
③
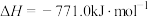 。
。
根据以上信息,计算反应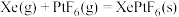

___________  。
。
(2)不久,在三个不同实验室里又分别合成了 、
、 、
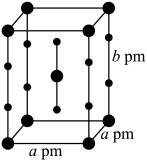
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为___________ ,中心原子的价层电子对数为___________ ,晶体密度为___________  。
。 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
已知:分压=总压×该组分物质的量分数;
对于反应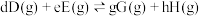
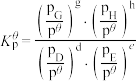
其中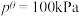 ,
,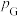 、
、 、
、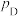 、
、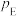 为各组分的平衡分压。
为各组分的平衡分压。
①
___________ 0(填“>”或“<”)。为提高平衡混合物中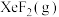 的含量,应
的含量,应___________ 投料比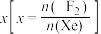 (填“增大”或“减小”)。
(填“增大”或“减小”)。
②673K时充入23.77molXe和 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:
则 平衡转化率
平衡转化率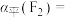
___________ (保留三位有效数字),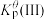
___________ 。
(1)1962年,化学家巴特利特合成了氙的第一个化合物
 ,其在熔化时电离出
,其在熔化时电离出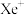 和
和 。Xe和
。Xe和 混合制得
混合制得 的反应可以表示如下:
的反应可以表示如下: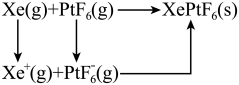
 )和1mol气态阴离子(
)和1mol气态阴离子( )所需要的能量叫做晶格能,
)所需要的能量叫做晶格能, 的晶格能为
的晶格能为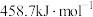 。
。②Xe的第一电离能为
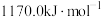 。
。③

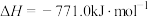 。
。根据以上信息,计算反应
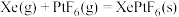

 。
。(2)不久,在三个不同实验室里又分别合成了
 、
、 、
、 三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°, 表示阿伏伽德罗常数的值。则该化合物的化学式为
表示阿伏伽德罗常数的值。则该化合物的化学式为 。
。
 混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
混合气体,反应体系中存在的平衡及相应部分数据如下表所示。已知:分压=总压×该组分物质的量分数;
对于反应
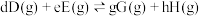
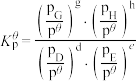
其中
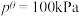 ,
,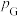 、
、 、
、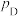 、
、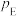 为各组分的平衡分压。
为各组分的平衡分压。标准压强平衡常数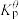 反应平衡 | 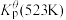 | 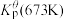 |
反应I: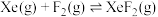  | 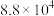 | 360 |
反应II: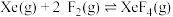  | ||
反应III: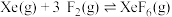  | 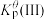 |

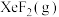 的含量,应
的含量,应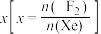 (填“增大”或“减小”)。
(填“增大”或“减小”)。②673K时充入23.77molXe和
 ,达平衡时容器内总压强
,达平衡时容器内总压强 ,各产物的物质的量如下表所示:
,各产物的物质的量如下表所示:| 化学式 |  |  |  |
| 物质的量/mol | 3.60 | 19.80 | 0.36 |
 平衡转化率
平衡转化率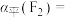
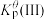
您最近一年使用:0次
2024-04-29更新
|
357次组卷
|
2卷引用:湖北省第九届2023-2024学年高三下学期4月四调(三模)考试化学试卷
8 . 含氮化合物广泛存在于自然界,是一类常见的化合物。
(1)汽车尾气是城市空气的主要污染物之一,汽车内燃机工作时发生反应:N2(g)+O2(g)=2NO(g),H2可以催化还原NO以达到消除污染的目的。
已知反应Ⅰ、N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ·mol-1;
Ⅱ、2H2(g)+O2(g)=2H2O(1)ΔH=-571.6kJ·mol-1。
写出H2(g)与NO(g)反应生成N2(g)和H2O(1)的热化学方程式:___________ ,该反应自发进行的条件为___________ (填“高温”或“低温”)。
(2)已知当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。如图所示为其他条件不变时,反应2NO(g)+2CO(g) 2CO2(g)+N2(g)中c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线:
2CO2(g)+N2(g)中c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线:
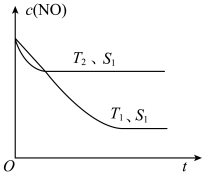
①该反应的ΔH___________ (填“>”或“<”)0。
②若催化剂的表面积S1>S2,在该图中画出该反应在T1、S2条件下达到平衡过程中c(NO)的变化曲线___________ 。
(3)尿素是一种重要的化工原料,工业上可用氨和二氧化碳合成尿素:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),ΔH<0,一定条件下,向10L恒容密闭容器中充入2molNH3和1molCO2。
CO(NH2)2(s)+H2O(g),ΔH<0,一定条件下,向10L恒容密闭容器中充入2molNH3和1molCO2。
①该反应10min后达到平衡,测得容器中气体密度为4.8g·L-1,则平衡常数K=___________ 。
②达到平衡后,再向容器中加入2molNH3(g)和1molCO2(g),则再次达到平衡时反应物NH3的转化率___________ (填“增大”“减小”或“不变”)。
③下列说法中,可以说明该反应已经达到平衡状态的有___________ (填序号)。
A.NH3和CO2的浓度之比为2∶1 B.2v正(NH3)=v逆(H2O)
C.气体的密度不变 D.容器内总压强不变
(4)N2O5是一种新型绿色硝化剂,其制备可以采用电解法。图甲是NaBH4燃料电池,图乙是电解制备N2O5装置,已知电解时电极a与电极d相连,电极c的反应式为___________ ,若制得10.8g N2O5,则消耗NaBH4的质量为___________ g。

(1)汽车尾气是城市空气的主要污染物之一,汽车内燃机工作时发生反应:N2(g)+O2(g)=2NO(g),H2可以催化还原NO以达到消除污染的目的。
已知反应Ⅰ、N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ·mol-1;
Ⅱ、2H2(g)+O2(g)=2H2O(1)ΔH=-571.6kJ·mol-1。
写出H2(g)与NO(g)反应生成N2(g)和H2O(1)的热化学方程式:
(2)已知当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。如图所示为其他条件不变时,反应2NO(g)+2CO(g)
 2CO2(g)+N2(g)中c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线:
2CO2(g)+N2(g)中c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线:
①该反应的ΔH
②若催化剂的表面积S1>S2,在该图中画出该反应在T1、S2条件下达到平衡过程中c(NO)的变化曲线
(3)尿素是一种重要的化工原料,工业上可用氨和二氧化碳合成尿素:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),ΔH<0,一定条件下,向10L恒容密闭容器中充入2molNH3和1molCO2。
CO(NH2)2(s)+H2O(g),ΔH<0,一定条件下,向10L恒容密闭容器中充入2molNH3和1molCO2。①该反应10min后达到平衡,测得容器中气体密度为4.8g·L-1,则平衡常数K=
②达到平衡后,再向容器中加入2molNH3(g)和1molCO2(g),则再次达到平衡时反应物NH3的转化率
③下列说法中,可以说明该反应已经达到平衡状态的有
A.NH3和CO2的浓度之比为2∶1 B.2v正(NH3)=v逆(H2O)
C.气体的密度不变 D.容器内总压强不变
(4)N2O5是一种新型绿色硝化剂,其制备可以采用电解法。图甲是NaBH4燃料电池,图乙是电解制备N2O5装置,已知电解时电极a与电极d相连,电极c的反应式为

您最近一年使用:0次
9 . 联氨(又称肼,N2H4无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子是___________ 分子(填“极性”或“非极性”),其中氮的杂化方式为___________ 。
(2)①2O2(g)+N2(g)=N2O4(1) H1
H1
②N2(g)+2H2(g)=N2H4(1) H2
H2
③O2(g)+2H2(g)=2H2O(g) H3
H3
④2N2H4(1)+N2O4(1)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mo1
上述反应热效应之间的关系式为△H4=___________ ,联氨和N2O4可作为火箭推进剂的主要原因为___________ 。
(3)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________ (已知:N2H4+H+
 的K=8.7×107;Kw=1.0×10-14);联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;Kw=1.0×10-14);联氨与硫酸形成的酸式盐的化学式为___________ 。
(4)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并有气泡产生﹐发生的化学方程式为___________ 。联氨可用于处理高压锅炉水中的氧。防止锅炉被腐蚀。理论上2kg的联氨可除去水中溶解的O2___________ kg。
(1)联氨分子是
(2)①2O2(g)+N2(g)=N2O4(1)
 H1
H1②N2(g)+2H2(g)=N2H4(1)
 H2
H2③O2(g)+2H2(g)=2H2O(g)
 H3
H3④2N2H4(1)+N2O4(1)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mo1
上述反应热效应之间的关系式为△H4=
(3)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为

 的K=8.7×107;Kw=1.0×10-14);联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;Kw=1.0×10-14);联氨与硫酸形成的酸式盐的化学式为(4)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并有气泡产生﹐发生的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 我国科学家成功利用光伏发电,将电解水获得的 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
(1) 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。 的
的
__________ (用含 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)有学者结合实验和计算机模拟结果,得出 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为__________ ;TS3对应的步骤适合在__________ (填“高温”或“低温”)条件下进行。 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。 的生成速率
的生成速率__________ (填“>”“<”或“=”,下同) 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2__________ Cat1。
②b点之后 的转化率降低,可能的原因是
的转化率降低,可能的原因是__________ 。
(4)已知 催化加氢的主要反应如下:
催化加氢的主要反应如下:
反应Ⅰ.
反应Ⅱ.
①230℃时,将 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
平衡时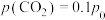 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
__________  (用含
(用含 的代数式表示)。
的代数式表示)。
②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当__________ 。
 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:(1)
 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。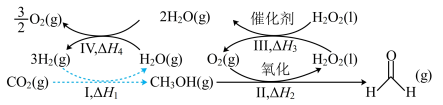
 的
的
 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。(2)有学者结合实验和计算机模拟结果,得出
 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为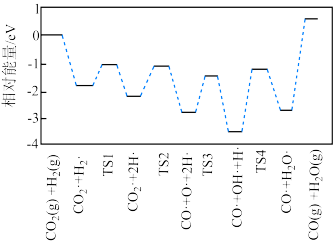
 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。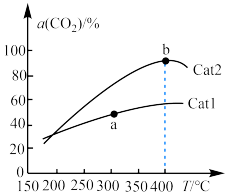
 的生成速率
的生成速率 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2②b点之后
 的转化率降低,可能的原因是
的转化率降低,可能的原因是(4)已知
 催化加氢的主要反应如下:
催化加氢的主要反应如下:反应Ⅰ.

反应Ⅱ.

①230℃时,将
 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。时间/min | 0 | 20 | 40 | 60 | 80 |
压强/MPa |
|
|
|
|
|
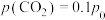 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当
您最近一年使用:0次
2024-03-30更新
|
385次组卷
|
5卷引用:湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷