名校
解题方法
1 . 氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取Cu2O。已知反应:
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
| A.−11kJ·mol−1 | B.+11kJ·mol−1 | C.+22kJ·mol−1 | D.−22kJ·mol−1 |
您最近一年使用:0次
2021-07-15更新
|
1388次组卷
|
22卷引用:海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题
海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题湖南省长沙市周南中学2020-2021学年高一年级下学期期末考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期期末考试化学试题安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题海南省屯昌县屯昌中学2021-2022学年高二上学期10月月考化学试题云南省昭通市镇雄县第四中学2021-2022学年高二上学期第一次月考化学试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题北京市第一五九中学2021-2022学年高二上学期期中考试化学试题【区级联考】北京市东城区2018-2019学年高二上学期期末检测化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020届高三12月月考化学试题安徽省亳州市第二中学2020届高三上学期第五次月考化学试题海南省海口市灵山中学2020-2021学年高二上学期期中考试化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题浙江省宁波市奉化区2021-2022学年高二上学期期末联考化学试题新疆叶城县第八中学2021-2022学年高二上学期期末考试化学(理)试题 吉林省长春市北师大附属学校2021-2022学年高二上学期期末考试化学试题天津市和平区2022-2023学年高二上学期期末质量调查化学试卷天津市和平区2022-2023学年高二上学期期末质量检测化学试题 吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题北京汇文中学2022-2023学年高二下学期期中考试化学试题河南省信阳高级中学2023-2024学年高二上学期开学考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题
名校
解题方法
2 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
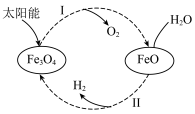
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2023-09-19更新
|
367次组卷
|
26卷引用:河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题
河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题辽源市第五中学2019-2020学年高一下学期第二次月考化学试题(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题河北省沧州市泊头市第一中学2021-2022学年高二上学期第一次月考化学试题山东省烟台市招远第一中学2022-2023学年高一下学期期中考试化学(等级考)试题河南省洛阳市宜阳县第一高级中学清北园2023-2024学年高一上学期第七次能力达标测试化学试卷(已下线)北京市第四中学2023-22024学年高一下学期期中考试 化学试题【区级联考】北京市石景山区2019届高三第一学期期末考试化学试题辽宁省锦州市滨海实验中学2019-2020学年高三上学期期末考试化学试题海南省海南中学2019-2020学年高二上学期期末考试化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题(已下线)专题九 化学能与热能(提分特训)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节综合训练高中必刷题高二选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 第二节综合训练河北省沧州市泊头市第一中学2020-2021学年高二上学期第一次月考化学试题山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题湖南省中方一中2020-2021学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)题型98 结合反应能量图示或物质循环图示书写热化学方程式(已下线)章末综合评价(六)
名校
3 . 物质E在一定条件下可发生一系列转化,由图判断下列关系错误的是
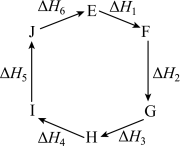

| A.E→J,ΔH=-ΔH6 |
| B.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=1 |
| C.G→J,|ΔH|=|ΔH1+ΔH2+ΔH6| |
| D.|ΔH1+ΔH2+ΔH3|=|ΔH4+ΔH5+ΔH6| |
您最近一年使用:0次
2022-07-22更新
|
399次组卷
|
10卷引用:吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题
吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题(资助班)山东省枣庄市第八中学(东校区)2020-2021学年高二上学期9月月考化学试题(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)(已下线)1.2.2 化学反应焓变的计算-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省哈尔滨市宾县第二中学2021-2022学年高二下学期开学考试化学试题辽宁省协作校2022-2023学年高二上学期期中考试化学试题辽宁省辽南2022-2023学年高二上学期期中考试化学试题辽宁省鞍山市岫岩满族自治县2022-2023学年高二上学期11月期中考试化学试题新疆乌鲁木齐市高级中学2023-2024学年高二上学期第一次月考化学试题
4 . 已知
①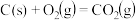
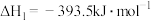
②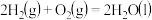
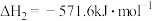
③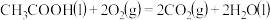
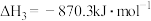
则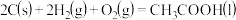 的
的 值为
值为
①
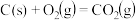
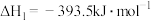
②
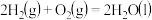
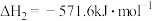
③
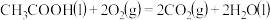
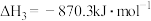
则
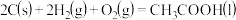 的
的 值为
值为A.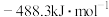 | B. |
C.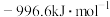 | D.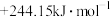 |
您最近一年使用:0次
2021-07-22更新
|
889次组卷
|
3卷引用:四川省成都市龙泉驿区2020-2021学年高一下学期末学业质量监测联考化学试题
5 . H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是
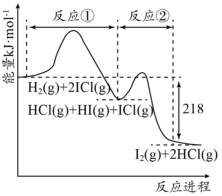

| A.反应①、反应②均为放热反应 |
| B.反应①、反应②均为氧化还原反应 |
| C.H2与ICl的总反应速率快慢取决于反应② |
| D.反应H2(g)+2ICl(g)=I2(g)+2HCl(g)的ΔH=-218kJ·mol-1 |
您最近一年使用:0次
2021-01-29更新
|
787次组卷
|
3卷引用:山东省日照市莒县2020-2021学年高一下学期期中考试化学试题
名校
解题方法
6 .  催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。

下列说法不正确 的是
 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法
| A.由图1推知反应物断键吸收的能量小于生成物成键释放的能量 |
B.图2中,若生成的 为液态,则能量变化曲线为① 为液态,则能量变化曲线为① |
C. |
D.制备 的反应使用催化剂时,其 的反应使用催化剂时,其 不变 不变 |
您最近一年使用:0次
2021-05-10更新
|
807次组卷
|
8卷引用:北京一零一中学2020-2021学年高一下学期期末考试化学试题
北京一零一中学2020-2021学年高一下学期期末考试化学试题北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)湖南省五市十校教研教改共同体2021-2022学年高一下学期期末考试化学试题河南省中原名校2022-2023学年高二上学期第一次联考化学试题(已下线)题型14 从吸热与放热角度突破反应热图像北京交通大学附属中学2023-2024学年高三上学期12月月考化学试题 北京市第十二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 最新一期国际学术期刊《自然纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇 .
.
(1)该法利用 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下:
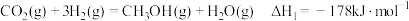
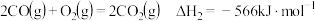
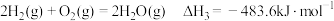
已知:i.断开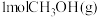 中的化学键共吸收
中的化学键共吸收 的能量
的能量
ⅱ.反应①中部分化学键键能数据如下:
由此计算断开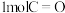 需要吸收
需要吸收_______  的能量,
的能量,
______  。
。
(2)将甲醇完全燃烧生成液态水的反应设计成原电池,以 为电解质.工作时负极的电极反应式
为电解质.工作时负极的电极反应式_____________________ 。
 .
.(1)该法利用
 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下: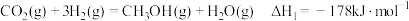
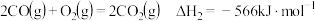
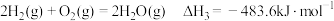
已知:i.断开
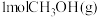 中的化学键共吸收
中的化学键共吸收 的能量
的能量ⅱ.反应①中部分化学键键能数据如下:
化学键 |
|
|
键能 | 436 | 463 |
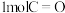 需要吸收
需要吸收 的能量,
的能量,
 。
。(2)将甲醇完全燃烧生成液态水的反应设计成原电池,以
 为电解质.工作时负极的电极反应式
为电解质.工作时负极的电极反应式
您最近一年使用:0次
8 . 按要求填空:
(1)相对分子质量为72的烷烃的分子式为___________ ,结构有___________ 种,分别写出它们的结构简式___________ 。
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;___________ (填序号)
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式___________ 。
(4)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
②2Al(s)+ O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
Al和FeO发生反应的热化学方程式是___________ 。
(1)相对分子质量为72的烷烃的分子式为
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式
(4)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1②2Al(s)+
 O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1Al和FeO发生反应的热化学方程式是
您最近一年使用:0次
9 . 科学家致力于二氧化碳甲烷化研究,期待早日实现“碳中和”的愿景。下列关于二氧化碳甲烷化技术的说法错误的是
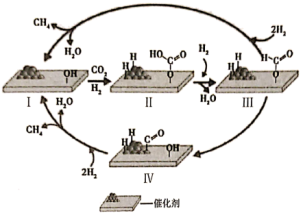

A.I→II的反应方程式为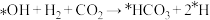 ( ( 代表吸附态) 代表吸附态) |
| B.II→III的过程中有C—O键的断裂也有O—H键形成 |
| C.III→I存在两种路径,这两种路径中III与I的能量差值不同 |
D.每生成1mol 转移电子数为8 转移电子数为8 |
您最近一年使用:0次
2021-07-08更新
|
745次组卷
|
3卷引用:福建省厦门市2020-2021学年高一下学期期末考试化学试题
解题方法
10 . 回答下列问题:
(1)2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
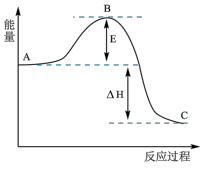
图中A、C分别表示_____ 、_____ ,E的大小对该反应的反应热_____ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点_____ (填“变大”、“变小”或“不变”)。
(2)已知下列热化学方程式:2Zn(s)+O2(g)=2ZnO(s) ∆H1=-702.2 kJ/mol
2Hg(l)+O2(g)=2HgO(s) ∆H2=-181.4 kJ/mol
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)的∆H是_____ 。
(3)在25℃、101 kPa下,1 g硫粉完全燃烧放出9kJ的热量,写出表示该反应燃烧热的热化学方程式为_____ 。
(4)已知拆开1 mol H-H键,1 mol Cl-Cl键,1 mol H-Cl键,分别需要的能量是436 kJ、243 kJ、431 kJ,则Cl2与H2反应生成HCl的热化学方程式为_____ 。
(5)同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ∆H1①,2H2(g)+O2(g)=2H2O(l) ∆H2②,则∆H1_____ ∆H2填“>”、“<”或“=”)。
(1)2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。

图中A、C分别表示
(2)已知下列热化学方程式:2Zn(s)+O2(g)=2ZnO(s) ∆H1=-702.2 kJ/mol
2Hg(l)+O2(g)=2HgO(s) ∆H2=-181.4 kJ/mol
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)的∆H是
(3)在25℃、101 kPa下,1 g硫粉完全燃烧放出9kJ的热量,写出表示该反应燃烧热的热化学方程式为
(4)已知拆开1 mol H-H键,1 mol Cl-Cl键,1 mol H-Cl键,分别需要的能量是436 kJ、243 kJ、431 kJ,则Cl2与H2反应生成HCl的热化学方程式为
(5)同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ∆H1①,2H2(g)+O2(g)=2H2O(l) ∆H2②,则∆H1
您最近一年使用:0次
2022-12-19更新
|
323次组卷
|
3卷引用:陕西省延安市富县高级中学2020-2021学年高一下学期期中考试化学试题






