解题方法
1 . 我国科学家采用磷化硼(BP)纳米颗粒成功地实现了高选择性电工化还原CO2制CH3OH,CO2在阴极催化剂表面的变化及反应历程如图所示:
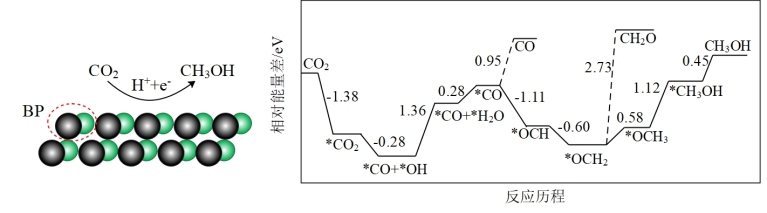
下列说法正确的是( )

下列说法正确的是( )
| A.制备CH3OH过程中得到相对较多的副产物是CH2O |
| B.在催化剂上生成CH3OH的电极反应式为CO2+6H++6e-=CH3OH+H2O |
| C.在催化剂上生成CH3OH的过程中有极性键和非极性键的断裂和生成 |
| D.*CO+*OH=*CO+*H2O为放热过程 |
您最近一年使用:0次
名校
解题方法
2 . 科研工作者通过计算机模拟和数学计算,设计出三条在含[Pt-O]结构的化合物中插入CO的反应路径,其相对能量变化如图所示,下列说法正确的是
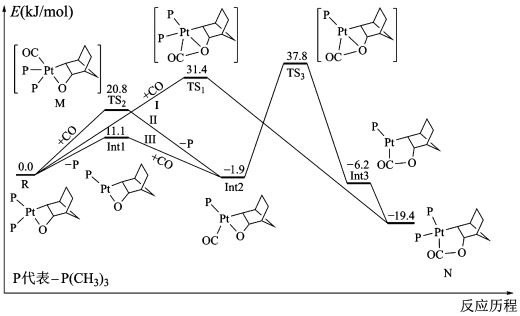
| A.反应II中,活化能最大的能垒为39.7kJ/mol |
| B.根据图像分析,该历程应按照路径Ⅲ进行 |
| C.在该反应中,CO是反应的催化剂 |
| D.该反应为吸热反应 |
您最近一年使用:0次
2022-05-04更新
|
668次组卷
|
12卷引用:化学(福建B卷)-学易金卷:2023年高考第一次模拟考试
(已下线)化学(福建B卷)-学易金卷:2023年高考第一次模拟考试(已下线)选择题6-10辽宁省辽南协作体2022届高三第二次模拟考试化学试题(已下线)专项10 化学反应与能量-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)三轮冲刺卷3-【赢在高考黄金20卷】备战2022年高考化学模拟卷(辽宁专用)(已下线)专题07 化学反应中的能量变化-2022年高考真题模拟题分项汇编湖南省株洲市攸县第一中学2022-2023学年高三上学期第二次月考化学试题河北省邯郸市第一中学2022-2023学年高三上学期一轮复习收官考试(二)化学试题湖南省株洲市九方中学2022-2023学年高三上学期第五次月考化学试题湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题河北省保定市2022-2023学年高三上学期12月月考化学试题陕西省咸阳市实验中学2022-2023学年高三上学期第二次月考化学试题
3 . 以CO2生产甲醇(CH3OH)是实现“碳中和”的重要途径。其原理是CO2(g) + 3H2(g) CH3OH(g) + H2O(g)。
CH3OH(g) + H2O(g)。
(1)该反应的能量变化如图所示,该反应为_______ (填“放热”或“吸热”)反应。
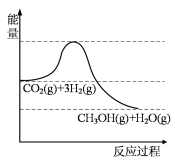
(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_______。
(3)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2、CH3OH的物质的量随时间变化如图。从反应开始到3 min末,用H2浓度变化表示的平均反应速率v(H2)=_______ ;反应达到平衡状态,此时H2的转化率为_______ 。
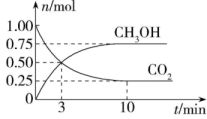
(4)在相同温度、容积不变的条件下,不能 说明该反应已达平衡状态的是_______。
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图。
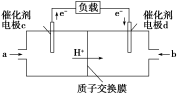
①则电极c是_______ (填“正极” 或“负极”),电极d的电极反应式_______ 。
②若线路中转移1 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。
 CH3OH(g) + H2O(g)。
CH3OH(g) + H2O(g)。(1)该反应的能量变化如图所示,该反应为
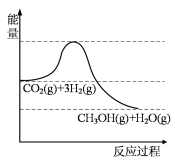
(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_______。
| A.升高温度 | B.充入He | C.加入合适的催化剂 | D.降低压强 |

(4)在相同温度、容积不变的条件下,
| A.CO2、H2的浓度均不再变化 |
| B.体系压强不变 |
| C.n(CH3OH)∶n(H2O)=1∶1 |
| D.H2的消耗速率与CH3OH的生成速率之比为3∶1 |

①则电极c是
②若线路中转移1 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
2022-04-22更新
|
665次组卷
|
3卷引用:福建省福州第十五中学2022-2023学年高三上学期11月线上限时训练化学试题
4 . 苯与Br2的催化反应历程如下图所示。下列说法正确的是
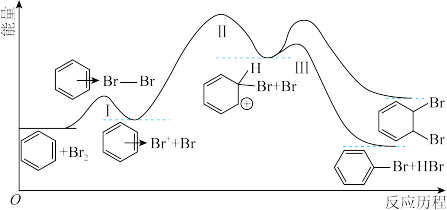

A.苯与Br2生成 的反应为吸热反应 的反应为吸热反应 |
| B.上图中,苯与Br2的催化反应生成了溴苯、邻二溴苯 |
C.从图中第III步反应所给信息看,生成 为主要反应 为主要反应 |
D.由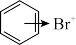 转化为 转化为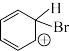 的过程中有极性键的断裂与形成 的过程中有极性键的断裂与形成 |
您最近一年使用:0次
2022-04-20更新
|
499次组卷
|
6卷引用:化学(福建A卷)-学易金卷:2023年高考第一次模拟考试
(已下线)化学(福建A卷)-学易金卷:2023年高考第一次模拟考试重庆市主城区2022届高三第二次学业教学质量抽测化学试题(已下线)专题07 化学反应中的能量变化-2022年高考真题模拟题分项汇编(已下线)考点34 芳香烃-备战2023年高考化学一轮复习考点帮(全国通用)湖南省株洲市南方中学2022-2023学年高三上学期第五次月考化学试题黑龙江省鹤岗市第一中学2021-2022学年高二下学期期中考试化学试题
5 . 苯与 的催化反应历程如图所示。关于该反应历程,下列说法正确的是
的催化反应历程如图所示。关于该反应历程,下列说法正确的是
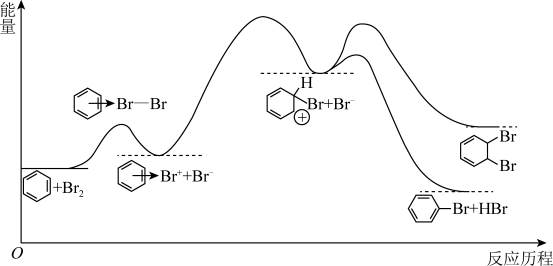
 的催化反应历程如图所示。关于该反应历程,下列说法正确的是
的催化反应历程如图所示。关于该反应历程,下列说法正确的是
A.苯与 的催化反应为放热反应 的催化反应为放热反应 |
B.该反应历程,苯与 的催化反应可生成溴苯、邻二溴苯 的催化反应可生成溴苯、邻二溴苯 |
C.苯与 的催化反应决速步伴随着极性键的断裂与形成 的催化反应决速步伴随着极性键的断裂与形成 |
| D.从反应速率角度,苯与Br2,的催化反应主反应为取代反应,原因是该反应活化能更低 |
您最近一年使用:0次
2022-03-05更新
|
1212次组卷
|
5卷引用:福建省福州市2022届高中毕业班(3月)第二次质量检测化学试题
福建省福州市2022届高中毕业班(3月)第二次质量检测化学试题(已下线)专题07 化学反应中的能量变化及反应机理-三年(2020-2022)高考真题分项汇编(已下线)专题08 化学反应与能量-备战2023年高考化学母题题源解密(全国通用)(已下线)第17讲 化学能与热能(练)-2023年高考化学一轮复习讲练测(全国通用)湖南省岳阳市岳阳县2022-2023学年高三下学期6月期末化学试题
6 . 利用化学链将高炉废气中CO2转化为CO的示意图如下。下列说法不正确的是


| A.Fe3O4和CaO可循环利用 |
| B.反应④为吸热反应 |
C.该化学链的总反应是 |
| D.该方法可降低分离CO和N2所需的能耗 |
您最近一年使用:0次
2022-03-04更新
|
1024次组卷
|
4卷引用:福建省厦门市2022届高三毕业班第二次质量检测化学试题
福建省厦门市2022届高三毕业班第二次质量检测化学试题(已下线)专题07 化学反应中的能量变化及反应机理-三年(2020-2022)高考真题分项汇编(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)江苏省苏州市吴江中学2023-2024学年高二上学期10月月考化学试题
解题方法
7 . 乙烯水合制乙醇的反应机理及能量与反应进程的关系如图所示。下列叙述错误的是


| A.乙烯转化为乙醇的过程中,H+起催化作用 |
| B.总反应为放热反应 |
| C.总反应速率由第①步反应决定 |
| D.第②步逆反应的活化能大于第③步逆反应的活化能 |
您最近一年使用:0次
8 . 某化学兴趣小组进行了实验:向2支试管中分别加入0.5 g Na2CO3固体和0.5 gNaHCO3固体,再分别加入30 mL 0.3 mol·L-1盐酸,充分反应后,用手触摸试管,明显感觉到加Na2CO3固体的试管变热了,加NaHCO3固体的试管变冷了。甲同学由此得出结论:CO (aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO
(aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO (aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?_____ (填“甲”或“乙”) ,理由是_______ 。
(2)查阅资料:
反应I :CO (aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
(aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
反应II :HCO (aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
(aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
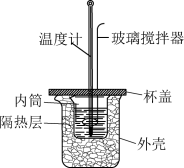
(3)该化学兴趣小组用如图所示装置设计了实验,验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。
表格一:
表格二:
表格三:
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是_______________ 。
②表格二对应实验得出的结论是________________ 。
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1______ (填“>”、“< ”或“=”,下同) △H3,△H2______ △H4。
 (aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO
(aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO (aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?
(2)查阅资料:
反应I :CO
 (aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
(aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;反应II :HCO
 (aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
(aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
A.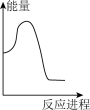 | B.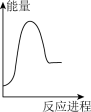 | C.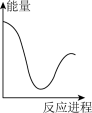 | D.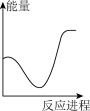 |

表格一:
试剂1 | 试剂2混合前温度/℃ | 混合后温度/℃ |
0.5 g Na2CO3 | 40mL HCl 19.0 | 21.7 |
0.5 g NaHCO3 | 40 mL HCl 19.0 | 18.1 |
表格二:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22. 3 | 19.0 | 10mL H2O 19.0 | 19.0 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL H2O 19.0 | 19.0 |
表格三:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22.3 | 19.0 | 10mL HCl 19.0 | 20.5 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL HCl19.0 | 18.3 |
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是
②表格二对应实验得出的结论是
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1
您最近一年使用:0次
9 . 已知反应 ( aq)+2I-(aq)
( aq)+2I-(aq) 2
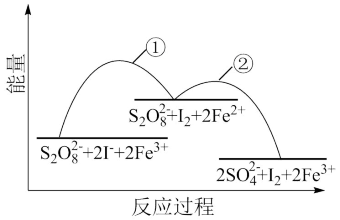
2 (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
①2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
②2Fe2+( aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
 ( aq)+2I-(aq)
( aq)+2I-(aq) 2
2 (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是①2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)②2Fe2+( aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
| A.反应①和反应②相比,反应②更快 |
| B.Fe3+是该反应的催化剂 |
| C.增大Fe3+的浓度,能够加快反应速率 |
| D.若不加Fe3+,正反应的活化能比逆反应的活化能大 |
您最近一年使用:0次
2022-01-22更新
|
729次组卷
|
18卷引用:福建省泉州实验中学2021-2022学年上学期高三10月月考化学试题
福建省泉州实验中学2021-2022学年上学期高三10月月考化学试题湖北省新高考联考协作体2021-2022学年高三上学期起点考试化学试题(已下线)专题21 化学反应速率(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练 山西省太原市2021-2022学年高三上学期期末考试化学试题福建省厦门第一中学2022-2023学年高二上学期第一次月考化学试题(已下线)易错点20 化学反应机理-备战2023年高考化学考试易错题(已下线)专题13 反应机理图(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题二 化学反应机理图象(讲)天津北京师范大学静海附属学校2021-2022学年高二上学期第一次调研测试化学试题黑龙江省齐齐哈尔市第八中学2021-2022学年高二上学期期中考试化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第二学程考试化学试题(已下线)专题强化练2 反应历程与活化能(已下线)第07讲 活化能(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)广东省江门市培英高级中学2022-2023学年高二上学期10月月考化学试题甘肃省平凉市第一中学2022-2023学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高二上学期第一次月考化学试题甘肃省民勤县第四中学2021-2022学年高二上学期期中考试(实验班)化学试题
10 . 二维锑片(Sb)是一种新型的CO2电化学还原催化剂。酸性条件下人工固碳装置中CO2气体在Sb表面发生三种催化竞争反应,其反应历程如下图所示(*表示吸附态中间体)。下列说法不正确 的是
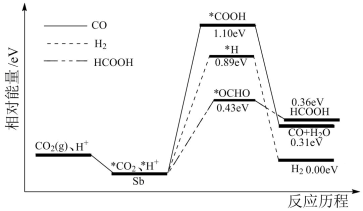

| A.生成HCOOH吸收的能量最多 |
| B.使用Sb改变了反应的路径 |
| C.Sb电极表面生成CO的反应为:*CO2+2e-+H2O = CO+2OH- |
| D.Sb对三种催化竞争反应的选择效果为HCOOH>H2>CO |
您最近一年使用:0次
2022-01-11更新
|
1240次组卷
|
10卷引用:福建省三明第一中学2023-2024学年高三上学期10月月考化学试题
福建省三明第一中学2023-2024学年高三上学期10月月考化学试题江苏省南京市、盐城市2021-2022学年高三第一次模拟考试化学试题湖南师范大学附属中学2022届高三月考(七)化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)湖南省衡阳市衡东县第一中学2022届高三下学期期中考试化学试题湖南省长沙市长郡中学2023届高三月考(六)化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题11-14)湖南省醴陵市第一中学2023届高三第六次月考化学试题湖南省常德市第一中学2023届高三第五次月考化学试题广东省华南师范大学附属中学2022届高三下学期押题预测(一)化学试题



