13. 自从1902年德国化学家哈伯研究出合成氨的方法以来,氨在工农业生产中应用广泛,可由N
2、H
2合成NH
3。
(1)天然气蒸汽转化法是目前获取原料气中H
2的主流方法。CH
4经过两步反应完全转化为H
2和CO
2,其能量变化示意图如图:
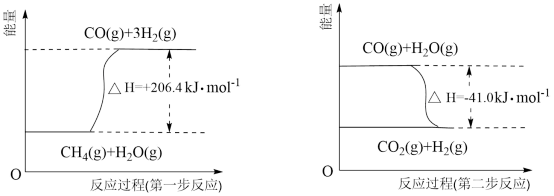
结合图象,写出1molCH
4通过蒸汽转化为CO
2和H
2的
△H=
___kJ·mol
-1。
(2)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H
+)为介质,用吸附在它内外表面上的金属钯多晶薄膜作电极,通过电解实现高温常压下的电化学合成氨。其示意图如图所示,阴极的电极反应式为
___。
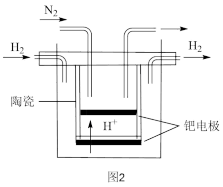
(3)甲小组模拟工业合成氨在一恒温恒容的密闭容器中发生反应:N
2(g)+3H
2(g)

2NH
3(g)
△H<0。如t
1min时达到平衡,在
t2min时改变某一条件,其反应过程如图所示,下列说法正确的是
____。

A.
t2min时改变的条件可以是向密闭容器中加N
2B.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:
KⅠ<
KⅡC.Ⅰ、Ⅱ两过程达到平衡的标志可以是混合气体的平均相对分子质量不再发生变化
(4)乙小组模拟不同条件下的合成氨反应,向容器中充入3mol N
2和9mol H
2,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图。
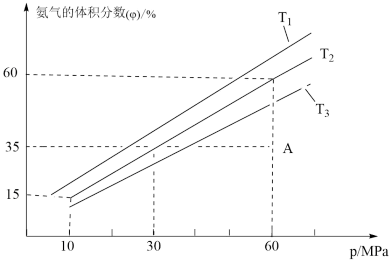
①T
1、T
2、T
3由大到小的排序为
___。
②在T
2、60MPa条件下,A点v
正___v
逆(填“>”“<”或“=”),理由是
__。
③计算T
2、60MPa平衡体系的平衡常数K
p=
___MPa
-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果保留两位有效数字)