解题方法
1 . 在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。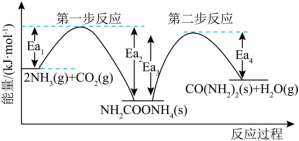

您最近一年使用:0次
2 . 据报道,在300℃和70MPa条件下由二氧化碳和氢气合成乙醇已成现实,其反应的化学方程式为: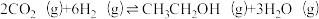 ,下列叙述错误的是
,下列叙述错误的是
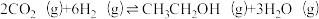 ,下列叙述错误的是
,下列叙述错误的是| A.使用Cu-Zn-Fe催化剂可提高CO2转化率 |
| B.由反应需在300℃进行可推测该反应是吸热反应 |
| C.平衡时,3v正(CO2)=v逆(H2) |
| D.从平衡气体中分离出CH3CH2OH和H2O,可提高CO2和H2的利用率 |
您最近一年使用:0次
名校
3 . 某反应过程中体系的能量变化如图所示,下列说法错误的是
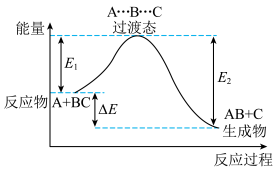
A.反应过程可表示为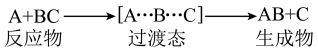 |
B. 为反应物的能量与过渡态的能量差,称为正反应的活化能 为反应物的能量与过渡态的能量差,称为正反应的活化能 |
C.正反应的热效应为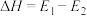 ,且 ,且 ,所以正反应为放热反应 ,所以正反应为放热反应 |
D.此图中逆反应的热效应为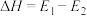 ,逆反应为吸热反应 ,逆反应为吸热反应 |
您最近一年使用:0次
名校
解题方法
4 . 已知298K、101kPa条件下:①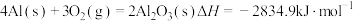 ;②
;②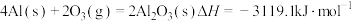 。由此得出的正确结论是
。由此得出的正确结论是
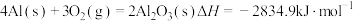 ;②
;②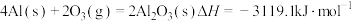 。由此得出的正确结论是
。由此得出的正确结论是| A.O3比O2稳定,由O2变O3为放热反应 |
| B.O3比O2稳定,由O2变O3为吸热反应 |
| C.等质量的O2比O3能量高,由O2变O3为放热反应 |
| D.等质量的O2比O3能量低,由O2变O3为吸热反应 |
您最近一年使用:0次
名校
解题方法
5 . 硫酸工业生产的核心阶段是转化,转化率越高,则硫的利用率越高,对环境影响也越小。
1.转化阶段发生的反应: (放热反应),上述反应中,反应物的总能量
(放热反应),上述反应中,反应物的总能量___________ (选填“大于”或“小于”)生成物的总能量。
2.为合理利用反应中产生的热量,热交换器在硫酸工业中与下列___________设备合为一体。
3.如图中,Y处的气体是___________。
1.转化阶段发生的反应:
 (放热反应),上述反应中,反应物的总能量
(放热反应),上述反应中,反应物的总能量2.为合理利用反应中产生的热量,热交换器在硫酸工业中与下列___________设备合为一体。
| A.沸腾炉 | B.净化器 | C.接触室 | D.吸收塔 |
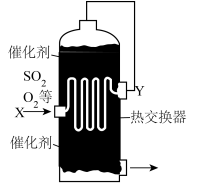
A.低温的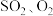 | B.低温的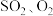 和 和 |
C.高温的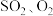 | D.高温的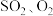 和 和 |
您最近一年使用:0次
名校
6 . 某反应的微观历程及反应过程中的能量变化如图下左所示。其中 分别表示
分别表示 、
、 、
、 及催化剂。
及催化剂。
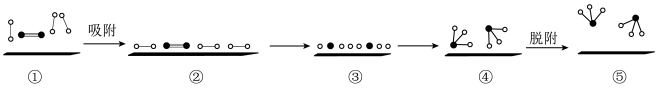
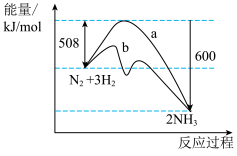
A.该反应为: |
| B.①-②过程中催化剂与气体之间形成离子键 |
| C.②→③过程中,需要吸收能量 |
| D.上右图说明该反应中,断裂反应物化学键所吸收的能量大于形成生成物化学键所放出的能量 |
您最近一年使用:0次
解题方法
7 . 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示。下列说法正确的是
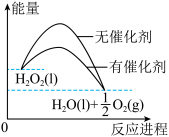
| A.H2O2分解属于吸热反应 |
| B.加入催化剂,减小了反应的焓变 |
| C.加入催化剂,可提高反应的活化能 |
| D.反应物的焓高于生成物的焓 |
您最近一年使用:0次
名校
8 . 填空
(1)氢气燃烧放出能量,生成物总能量_____ 反应物总能量(高于、低于)
下列反应中,也放出能量的是_____ 。
①断裂化学键②分解反应③碳与 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应
(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应: 的放出热量=
的放出热量=_____ 。(用a、b、c表示)
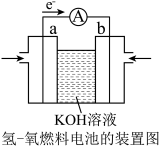
(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的_____ (a或b)极。
(1)氢气燃烧放出能量,生成物总能量
下列反应中,也放出能量的是
①断裂化学键②分解反应③碳与
 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应:
 的放出热量=
的放出热量=(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的
您最近一年使用:0次
名校
解题方法
9 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
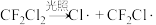 反应①
反应①
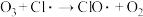 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
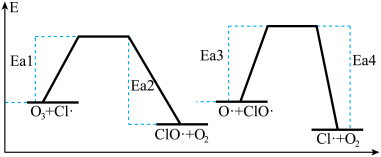
(2)利用上图数据计算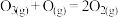 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)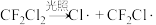 反应①
反应①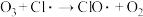 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
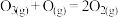 的
的
您最近一年使用:0次
名校
解题方法
10 . “铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如下装置实现:
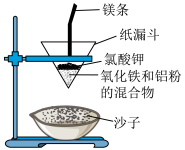
(1)写出该反应的化学方程式_______ 。
(2)实验中能观察到的现象有_______ 、_______ (例举两点)。
(3)可表示铝与氧化铁反应的热效应的图是
A .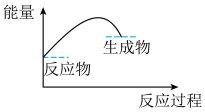 B.
B.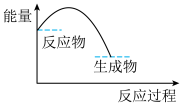 C.
C.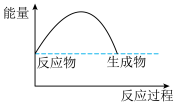
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
(5)以下实验中属于放热反应的是_______
A.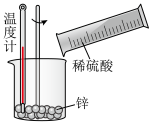 B.
B.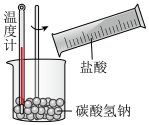 C.
C.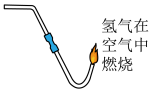

(1)写出该反应的化学方程式
(2)实验中能观察到的现象有
(3)可表示铝与氧化铁反应的热效应的图是
A .
 B.
B. C.
C.
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
| A.铝还原性较强 | B.锰、钒熔点高 | C.铝能形成多种合金 | D.反应放出大量热 |
(5)以下实验中属于放热反应的是
A.
 B.
B. C.
C.
您最近一年使用:0次



