23-24高二上·上海·期末
1 . 已知: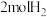 与足量
与足量 充分燃烧生成液态水时放出
充分燃烧生成液态水时放出 热量。
热量。
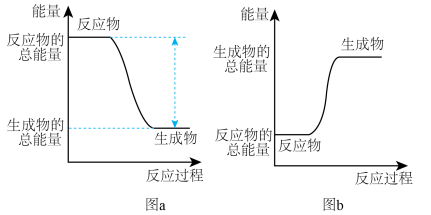
(1)该反应的能量变化可用图中的___________ (填字母)表示。
(2)写出 燃烧生成液态水的热化学反应方程式
燃烧生成液态水的热化学反应方程式___________ 。
(3)关于热化学方程式: 的说法正确的是___________。
的说法正确的是___________。
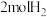 与足量
与足量 充分燃烧生成液态水时放出
充分燃烧生成液态水时放出 热量。
热量。
(1)该反应的能量变化可用图中的
(2)写出
 燃烧生成液态水的热化学反应方程式
燃烧生成液态水的热化学反应方程式(3)关于热化学方程式:
 的说法正确的是___________。
的说法正确的是___________。| A.热化学方程式中化学计量数表示分子数 |
B.该反应 大于零 大于零 |
C.该反应的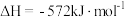 |
D.该反应可表示 水分解时的热效应 水分解时的热效应 |
您最近一年使用:0次
名校
解题方法
2 . 在能源绿色低碳转型行动中,天然气发挥着重要作用。管道天然气实行“应改尽改、能改全改”,预计到2025年,管道天然气普及率达到95%以上。
(1)天然气的主要成分是_______ (写电子式),该分子的空间构型是_______ 。
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要_______ (填“调小”或“调大”)风门。
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.
Ⅱ.链传递: ,
,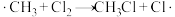 ,……
,……
Ⅲ.链终止: ,
, ……
……
为探究光照对 与
与 反应的影响,实验如下。
反应的影响,实验如下。
①由B和D得出的结论是_______ 。
②根据上述机理,解释C中几乎没有氯代甲烷的原因_______ 。
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷_______ (填“有”或“没有”)同分异构体。
(4)丙烷氯代反应中链传递的一步反应能量变化如下。
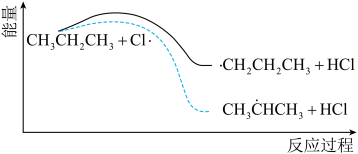
推知断裂 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量_______ (填“大”或“小”)。
(1)天然气的主要成分是
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.

Ⅱ.链传递:
 ,
,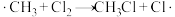 ,……
,……Ⅲ.链终止:
 ,
, ……
……为探究光照对
 与
与 反应的影响,实验如下。
反应的影响,实验如下。| 编号 | 操作 | 结果 |
| A | 将Cl2与CH4混合后,光照 | 得到氯代甲烷 |
| B | 将Cl2先用光照,然后迅速在黑暗中与CH4混合 | 得到氯代甲烷 |
| C | 将Cl2先用光照,然后在黑暗中放置一段时间,再与CH4混合 | 几乎无氯代甲烷 |
| D | 将CH4先用光照,然后迅速在黑暗中与Cl2混合 | 几乎无氯代甲烷 |
②根据上述机理,解释C中几乎没有氯代甲烷的原因
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷
(4)丙烷氯代反应中链传递的一步反应能量变化如下。

推知断裂
 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量
您最近一年使用:0次
名校
3 . 下列反应中生成物总能量高于反应物总能量的是
| A.氧化钙溶于水 | B.铁粉与硫粉共热 |
| C.强酸强碱中和 | D.氢氧化钡晶体与氯化铵晶体的反应 |
您最近一年使用:0次
2023-11-27更新
|
165次组卷
|
3卷引用:上海市复兴高级中学2022-2023学年高二上学期期中考试化学(等级考)试题
4 . 如图是 的能量示意图。下列说法正确的是
的能量示意图。下列说法正确的是
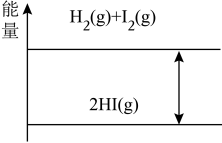
 的能量示意图。下列说法正确的是
的能量示意图。下列说法正确的是
| A.该反应是吸热反应 | B.该反应物总能量高于生成物总能量 |
| C.放热反应的发生都不需要加热 | D.该反应中H2为氧化剂 |
您最近一年使用:0次
名校
5 . 实验室研究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3>0
不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。回答问题
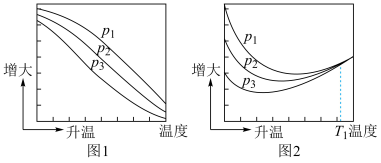
(1)图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是______ 。
(2)图1中,压强p1、p2、p3由大到小的顺序为______ 。
(3)图2中T1温度时,三条曲线几乎交于一点的原因是______ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为______。
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3>0
不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。回答问题

(1)图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是
(2)图1中,压强p1、p2、p3由大到小的顺序为
(3)图2中T1温度时,三条曲线几乎交于一点的原因是
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为______。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
名校
解题方法
6 . 电喷雾电离等方法得到的M+(Fe+、Co+或Ni+等)匀O3反应可得MO+在一定条件下,MO++CH4=M++CH3OH,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。MO+与CH4或CT4体系的能量随反应进程的变化如图所示,下列说法错误的是
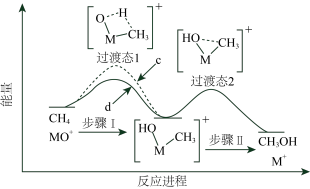

| A.该反应是放热反应 |
| B.步骤Ⅰ和步骤Ⅱ中氢原子的成键方式均发生了变化 |
| C.MO+与CT4反应的能量变化为曲线c |
| D.相同情况下,MO+与CHT3反应,氚代甲醇CT3OH的产量大于CHT2OT |
您最近一年使用:0次
2023-10-28更新
|
485次组卷
|
3卷引用:上海市青浦高中2023-2024学年高二上学期期末考试化学模拟试卷
上海市青浦高中2023-2024学年高二上学期期末考试化学模拟试卷重庆市第八中学校2023-2024学年高三上学期10月期中考试化学试题(已下线)题型06 反应热的判断及计算-2024年高考化学答题技巧与模板构建
名校
7 . 化学反应过程中释放或吸收的热量在生活、生产、科技及科研中应用广泛,回答下列问题。
(1)制作冷敷袋可利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”为生活带来便利,它可利用下面___________(填字母)反应放热加热食物。
(3)神舟系列火箭用偏二甲肼 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。
已知:反应1: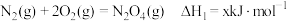
反应2: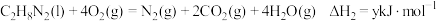
写出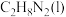 和
和 反应生成
反应生成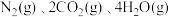 的热化学方程式:
的热化学方程式:___________
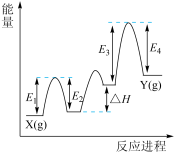
(4)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则 过程中的焓变为
过程中的焓变为___________ (列式表示)。
(5)已知,在 和
和 下,部分化学键的键能数据如表所示。
下,部分化学键的键能数据如表所示。
在 和
和 下,工业合成氨,每生成
下,工业合成氨,每生成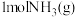 就会放出
就会放出 热量,在该条件下,向某容器中加入
热量,在该条件下,向某容器中加入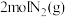 、
、 及合适的催化剂,充分反应后测得其放出的热量小于
及合适的催化剂,充分反应后测得其放出的热量小于 ,原因可能是
,原因可能是________ 表中的
___________ 。
(1)制作冷敷袋可利用
(2)“即热饭盒”为生活带来便利,它可利用下面___________(填字母)反应放热加热食物。
| A.浓硫酸和水 | B.生石灰和水 | C.纯碱和水 | D.食盐和白醋 |
(3)神舟系列火箭用偏二甲肼
 作燃料,
作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。已知:反应1:
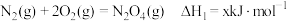
反应2:
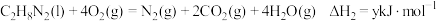
写出
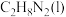 和
和 反应生成
反应生成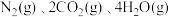 的热化学方程式:
的热化学方程式:(4)已知某金属氧化物催化丙烷脱氢过程中,部分反应进程如图,则
 过程中的焓变为
过程中的焓变为
(5)已知,在
 和
和 下,部分化学键的键能数据如表所示。
下,部分化学键的键能数据如表所示。| 化学键 |  |  |  |  |  |  |  |  |
键能/ | 436 | 391 |  | 498 | 414 | 803 | 462 | 193 |
 和
和 下,工业合成氨,每生成
下,工业合成氨,每生成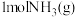 就会放出
就会放出 热量,在该条件下,向某容器中加入
热量,在该条件下,向某容器中加入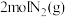 、
、 及合适的催化剂,充分反应后测得其放出的热量小于
及合适的催化剂,充分反应后测得其放出的热量小于 ,原因可能是
,原因可能是
您最近一年使用:0次
解题方法
8 . 已知该产业链中,有炭参与的某反应平衡常数表达式为:K=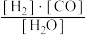 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:________ ,若该反应只有在持续高温下才能自发进行,则该反应为________ (“吸热”或“放热”)反应。
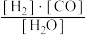 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:
您最近一年使用:0次
名校
解题方法
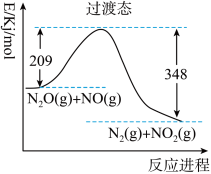
9 . 由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法错误的是

| A.使用催化剂可以降低过渡态的能量 |
| B.反应物能量之和大于生成物能量之和 |
| C.N2O(g)+NO(g)→N2(g)+NO2(g)+139kJ |
| D.断键吸收能量之和大于成键释放能量之和 |
您最近一年使用:0次
2023-09-30更新
|
210次组卷
|
4卷引用:上海市徐汇区徐汇中学2022-2023学年高三上学期11月期中考试化学试题
上海市徐汇区徐汇中学2022-2023学年高三上学期11月期中考试化学试题(已下线)专题02 反应热的测量和计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)(已下线)寒假作业01 化学反应的热效应-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)浙江省舟山市2023-2024学年高二上学期1月期末考试化学试题
10 . 以煤炭为原料制备氢气是一种常用的方法,总反应为: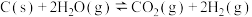 (正反应为吸热反应)
(正反应为吸热反应)
(1)上述反应中,反应物的总能量___________ 生成物的总能量。
A.大于 B.小于 C.等于
(2)下列措施中,能加快上述反应的反应速率的是___________。
(3)能说明上述反应一定达到化学平衡状态的是
(4)一定温度下,在2L密闭容器中加入足量的C(s)和3molH2O(g),反应至5min时,H2O(g)的物质的量变为1mol,0~5min内H2O(g)的平均反应速率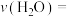
___________ 。
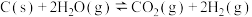 (正反应为吸热反应)
(正反应为吸热反应)(1)上述反应中,反应物的总能量
A.大于 B.小于 C.等于
(2)下列措施中,能加快上述反应的反应速率的是___________。
| A.将煤炭粉碎 | B.通入氦气 | C.降低温度 | D.加入催化剂 |
A. 保持不变 保持不变 | B.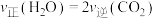 |
| C.物质的总质量不变 | D.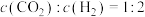 |
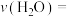
您最近一年使用:0次



