解题方法
1 . 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示。下列说法正确的是
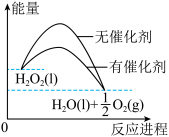
| A.H2O2分解属于吸热反应 |
| B.加入催化剂,减小了反应的焓变 |
| C.加入催化剂,可提高反应的活化能 |
| D.反应物的焓高于生成物的焓 |
您最近一年使用:0次
名校
2 . 填空
(1)氢气燃烧放出能量,生成物总能量_____ 反应物总能量(高于、低于)
下列反应中,也放出能量的是_____ 。
①断裂化学键②分解反应③碳与 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应
(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应: 的放出热量=
的放出热量=_____ 。(用a、b、c表示)
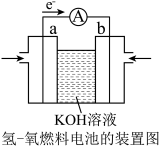
(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的_____ (a或b)极。
(1)氢气燃烧放出能量,生成物总能量
下列反应中,也放出能量的是
①断裂化学键②分解反应③碳与
 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应:
 的放出热量=
的放出热量=(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的
您最近一年使用:0次
名校
解题方法
3 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
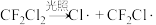 反应①
反应①
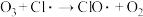 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
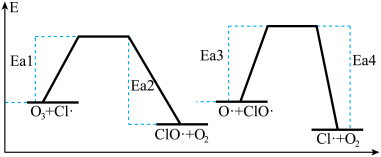
(2)利用上图数据计算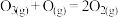 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)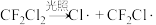 反应①
反应①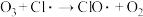 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
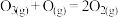 的
的
您最近一年使用:0次
名校
解题方法
4 . “铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如下装置实现:
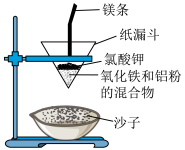
(1)写出该反应的化学方程式_______ 。
(2)实验中能观察到的现象有_______ 、_______ (例举两点)。
(3)可表示铝与氧化铁反应的热效应的图是
A .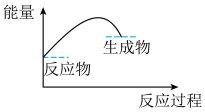 B.
B.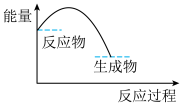 C.
C.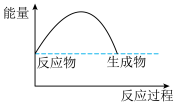
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
(5)以下实验中属于放热反应的是_______
A.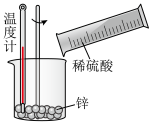 B.
B.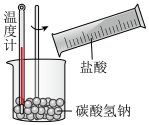 C.
C.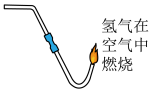

(1)写出该反应的化学方程式
(2)实验中能观察到的现象有
(3)可表示铝与氧化铁反应的热效应的图是
A .
 B.
B. C.
C.
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
| A.铝还原性较强 | B.锰、钒熔点高 | C.铝能形成多种合金 | D.反应放出大量热 |
(5)以下实验中属于放热反应的是
A.
 B.
B. C.
C.
您最近一年使用:0次
5 . 化学反应过程中释放或吸收的热量在生活、生产、科技及科研中应用广泛。
(1)制作冷敷袋可利用______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”为生活带来便利,它可利用下面______ (填字母)反应放热加热食物。
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的______ (填字母)表示。
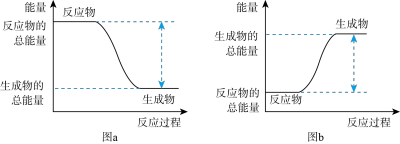
②写出H2燃烧生成液态水的热化学反应方程式____________ 。
(4)某反应过程中能量变化如图所示,下列有关叙述正确的是______。
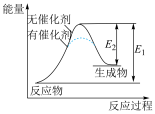
(5)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
计算可得:H2(g)+Cl2(g)=2HCl(g) ΔH =______ kJ/mol
②通过盖斯定律计算。已知:
2Na(s)+ O2(g)=Na2O (s) ΔH=-414kJ/mol
O2(g)=Na2O (s) ΔH=-414kJ/mol
2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ/mol
写出Na2O2与Na反应生成Na2O的热化学方程式:__________________ 。
(6)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。
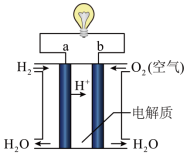
在这个燃料电池中,正极的电极反应为____________ 。若在标况下,消耗了33.6L的氢气,此时电路中转移的电子数目为______ 个(用阿伏加德罗常数表示)。
(1)制作冷敷袋可利用
(2)“即热饭盒”为生活带来便利,它可利用下面______ (填字母)反应放热加热食物。
| A.浓硫酸和水 | B.生石灰和水 | C.纯碱和水 | D.食盐和白醋 |
(3)已知:2molH2与足量O2充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的

②写出H2燃烧生成液态水的热化学反应方程式
(4)某反应过程中能量变化如图所示,下列有关叙述正确的是______。

| A.该反应为放热反应 |
| B.催化剂改变了化学反应的热效应 |
| C.催化剂不改变化学反应过程 |
| D.反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
(5)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |
②通过盖斯定律计算。已知:
2Na(s)+
 O2(g)=Na2O (s) ΔH=-414kJ/mol
O2(g)=Na2O (s) ΔH=-414kJ/mol 2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ/mol
写出Na2O2与Na反应生成Na2O的热化学方程式:
(6)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。

在这个燃料电池中,正极的电极反应为
您最近一年使用:0次
名校
6 . 下列实验操作或装置能达到目的的是
| 选项 | A | B | C | D |
| 操作或装置 | 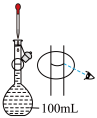 | 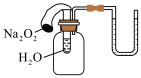 | 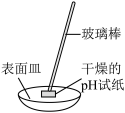 | 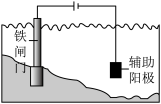 |
| 目的 | 配制100mLFeCl3溶液 | 验证Na2O2和H2O反应为放热反应 | 测定84消毒液的pH | 保护铁闸门不被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . (一)Na2O2是一种重要的物质,可用作漂白剂、消毒剂、氧化剂及供氧剂。某研究性学习小组在探究淡黄色Na2O2与H2O反应时物质变化与能量变化时,设计了如图所示的Ⅰ和Ⅱ两组实验装置。
(1)①中Na2O2的电子式___________ ,其中正负离子个数比为___________ 。
(2)②中的大量气泡主要成分是___________ 。
(3)③中溶液变红,说明反应混合液呈___________。
(4)写出 Na2O2与H2O反应的化学方程式___________ 。
(5)根据④和⑤中的现象分析,对反应过程的推测合理的是___________。
(二)在Ⅱ中把小试管套在带支管的试管内,在小试管里加入1g淡黄色Na2O2。在U形管内加入少量红墨水。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面。再夹紧螺旋夹,把水滴入小试管内,可观察到U形管右侧的液面立即下降,左侧的液面上升。
(6)由此推知,Na2O2与H2O反应过程中,能量转化形式为___________ 。
(7)可以用来表示Na2O2与H2O反应的图像是___________。
(8)从化学反应过程中旧键断裂和新键形成角度,分析Ⅱ中“U形管右侧的液面立即下降,左侧的液面上升”的原因:___________ 。
(9)分析 Na2O2与H2O反应时的物质转化关系,试推测16gCH4完全燃烧的产物通入足量的Na2O2中,Na2O2增重应为___________ 。
Ⅰ.
Ⅱ.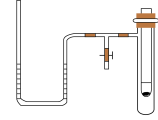
(1)①中Na2O2的电子式
(2)②中的大量气泡主要成分是
(3)③中溶液变红,说明反应混合液呈___________。
| A.酸性 | B.碱性 | C.中性 | D.不确定 |
(4)写出 Na2O2与H2O反应的化学方程式
(5)根据④和⑤中的现象分析,对反应过程的推测合理的是___________。
| A.反应过程中可能生成了一种中间过渡产物H2O2 |
| B.④→⑤发生的反应肯定属于氧化还原反应 |
| C.MnO2的主要作用是降低了水中氧气的溶解度 |
| D.⑤红色褪去说明溶液碱性减弱,反滴入NaOH溶液红色再现 |
(二)在Ⅱ中把小试管套在带支管的试管内,在小试管里加入1g淡黄色Na2O2。在U形管内加入少量红墨水。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面。再夹紧螺旋夹,把水滴入小试管内,可观察到U形管右侧的液面立即下降,左侧的液面上升。
(6)由此推知,Na2O2与H2O反应过程中,能量转化形式为
(7)可以用来表示Na2O2与H2O反应的图像是___________。
A.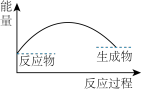 | B. |
C.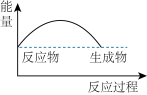 | D.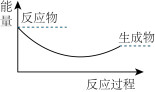 |
(8)从化学反应过程中旧键断裂和新键形成角度,分析Ⅱ中“U形管右侧的液面立即下降,左侧的液面上升”的原因:
(9)分析 Na2O2与H2O反应时的物质转化关系,试推测16gCH4完全燃烧的产物通入足量的Na2O2中,Na2O2增重应为
您最近一年使用:0次
名校
8 . I.肼可作氢气“储蓄罐”。Ni-Pt/La2O3是一种高选择性的肼分解制氢催化剂,催化反应机理如图所示,反应如下:

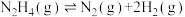
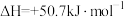
(1)根据上述信息,推测Ni-Pt/La2O3___________。
Ⅱ.肼类燃烧剂曾是火箭的“粮食”,但会造成污染,正逐渐被淘汰。新一代运载火箭采用全新配方——低温液氢液氧推进剂,让火箭飞得更稳健。已知一定条件下:
①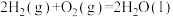
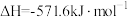 '
'
②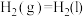

③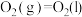
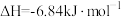
④

(2)请写出相同条件下液氢和液氧生成气态水的热化学方程式:___________ 。
(3)根据上述信息,以下说法正确的是___________。

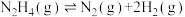
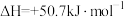
(1)根据上述信息,推测Ni-Pt/La2O3___________。
| A.能够有效降低制氢反应的反应热 |
| B.同时提高制氢正反应和逆反应的速率 |
| C.改变了制氢反应的反应历程 |
| D.不参与化学反应,使用一段时间后无需补加 |
Ⅱ.肼类燃烧剂曾是火箭的“粮食”,但会造成污染,正逐渐被淘汰。新一代运载火箭采用全新配方——低温液氢液氧推进剂,让火箭飞得更稳健。已知一定条件下:
①
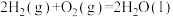
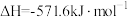 '
'②
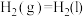

③
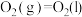
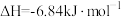
④


(2)请写出相同条件下液氢和液氧生成气态水的热化学方程式:
(3)根据上述信息,以下说法正确的是___________。
| A.变化④为低温自发的过程 |
| B.液氢液氧不点燃观察不到水生成,故该反应无法自发进行 |
| C.0.5mol液态氢气的能量高于0.5mol气态氢气的能量 |
| D.液氢和液氧作为火箭推进剂符合绿色化学理念 |
您最近一年使用:0次
名校
9 . I.铁触媒催化合成氨经历下图所示①~⑥步基元反应(从状态I至状态VII):___________ 步基元反应,“脱附”过程是___________ (填“吸热”或“放热”)过程。
(2)根据上图计算合成氨反应的焓变:

___________ 。
(3)上述反应的 ___________0(填“>”、“<”或“=”)。
___________0(填“>”、“<”或“=”)。
(4)已知: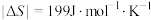 。合成氨反应能自发进行的温度是___________。
。合成氨反应能自发进行的温度是___________。
Ⅱ.为模拟上述工业合成氨的过程,向体积恒为2L的密闭容器(温度恒为T℃)中充入1mol N2和3mol H2发生上述反应,测得N2的体积分数 (N2)随时间(t)的变化如下表所示:
(N2)随时间(t)的变化如下表所示:
(5)40min时,N2的物质的量浓度是___________  (保留三位有效数字)。
(保留三位有效数字)。
(6)0~40min内,用H2表示该反应的平均速率为___________  。
。
(7)用 %表示N2的平衡转化率,则关于上述平衡体系的下列判断正确的是___________。
%表示N2的平衡转化率,则关于上述平衡体系的下列判断正确的是___________。
(8)T℃时,按下表数据向另一2L恒容容器中投料。则该时刻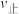 (N2)
(N2)___________  (N2)(选填“>”、“<”或“=”)。
(N2)(选填“>”、“<”或“=”)。
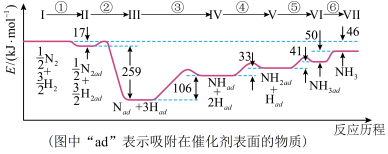
(2)根据上图计算合成氨反应的焓变:


(3)上述反应的
 ___________0(填“>”、“<”或“=”)。
___________0(填“>”、“<”或“=”)。| A.> | B.< | C.= | D.无法判断 |
(4)已知:
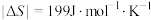 。合成氨反应能自发进行的温度是___________。
。合成氨反应能自发进行的温度是___________。| A.25℃ | B.125℃ | C.225℃ | D.325℃ |
Ⅱ.为模拟上述工业合成氨的过程,向体积恒为2L的密闭容器(温度恒为T℃)中充入1mol N2和3mol H2发生上述反应,测得N2的体积分数
 (N2)随时间(t)的变化如下表所示:
(N2)随时间(t)的变化如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
 (N2) (N2) | 0.250 | 0.225 | 0.210 | 0.203 | 0.200 | 0.200 |
(5)40min时,N2的物质的量浓度是
 (保留三位有效数字)。
(保留三位有效数字)。(6)0~40min内,用H2表示该反应的平均速率为
 。
。(7)用
 %表示N2的平衡转化率,则关于上述平衡体系的下列判断正确的是___________。
%表示N2的平衡转化率,则关于上述平衡体系的下列判断正确的是___________。A.若向恒温恒容的平衡体系中充入N2,则 %一定增大 %一定增大 |
| B.若向恒温恒压的平衡体系中充入He,则K一定减小 |
| C.若K减小,则温度一定升高 |
D.若 %减小,则K一定减小 %减小,则K一定减小 |
(8)T℃时,按下表数据向另一2L恒容容器中投料。则该时刻
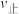 (N2)
(N2) (N2)(选填“>”、“<”或“=”)。
(N2)(选填“>”、“<”或“=”)。| 物质 | 物质的量/mol |
| N2 | 4 |
| H2 | 10 |
| NH3 | 6 |
您最近一年使用:0次
名校
10 . 回答下列问题。
(1)下列变化过程,属于放热是___________ 。
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g) =-437.3kJ/mol
=-437.3kJ/mol
②H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol
③CO(g)+ O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol
固态碳和水蒸气反应生成CO和H2的热化学方程式为___________ 。
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热 为
为___________ 。
(4)标准状况下,3.36L仅由C、H元素组成的某气体质量4.5g完全燃烧生成CO2(g)和H2O(l)时,放出233.97kJ的热量。该气体的分子式为___________ ,热值为___________ kJ/g,该气体燃烧热的热化学方程式为___________ 。
(1)下列变化过程,属于放热是
A.碳酸钙分解 B.氢气在氯气中燃烧 C.Ba(OH)2·8H2O与NH4Cl
D.铝热反应 E.酸碱中和反应 F.FeCl3水解
(2)①C(s)+O2(g)=CO2(g)
 =-437.3kJ/mol
=-437.3kJ/mol②H2(g)+
 O2(g)=H2O(g)
O2(g)=H2O(g)  =-285.8 kJ/mol
=-285.8 kJ/mol③CO(g)+
 O2(g)=CO2(g)
O2(g)=CO2(g)  =-283.0 kJ/mol
=-283.0 kJ/mol固态碳和水蒸气反应生成CO和H2的热化学方程式为
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热
 为
为| 化学键 | C-H | C-F | H-F | F-F |
| 键能kJ/mol | 414 | 489 | 565 | 155 |
您最近一年使用:0次



