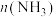1 . 下列反应中属于氧化还原反应且生成物的总能量高于反应物的总能量的是
| A.Na加热与氧气反应 | B.盐酸与碳酸氢钠反应 |
| C.氨气的催化氧化反应 | D.高温下,炭与 反应 反应 |
您最近一年使用:0次
2024·江西景德镇·二模
2 . 丙醛是一种重要的有机原料,在许多领域都有广泛的应用。在铑催化剂作用下,乙烯羰基合成丙醛涉及的反应如下:
主反应Ⅰ.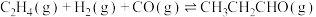

副反应Ⅱ.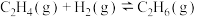

(1)
_____ 0 (填:“>”或“<)。
(2)保持温度不变,在恒容反应器中,按照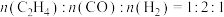 投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时
投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时 的转化率为80%,
的转化率为80%, 的选择性为25%,则
的选择性为25%,则 的转化率为
的转化率为______ %,
_____ kPa/min,反应Ⅰ的
_____  。(用含p的代数式表示,
。(用含p的代数式表示, 的选择性=
的选择性= )。
)。
(3)在装有相同催化剂的。相同恒压容器中,按照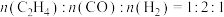 投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下
投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 的转化率(
的转化率( )如图所示。则B、D两点的平均反应速率v(B)
)如图所示。则B、D两点的平均反应速率v(B)_____ v(D)(填“>”、“=”、“<”),产生这一结果的原因可能是______ 。
(4)T℃时,向恒温恒容的甲容器中,通入1mol 、1mol CO和2mol
、1mol CO和2mol  ;向绝热恒容的乙容器中通入1mol
;向绝热恒容的乙容器中通入1mol  、1mol CO、2mol
、1mol CO、2mol  ,若只发生上述反应Ⅰ。则甲乙容器中
,若只发生上述反应Ⅰ。则甲乙容器中 的平衡转化率
的平衡转化率
____  (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是_____ 。
主反应Ⅰ.
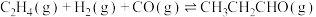

副反应Ⅱ.
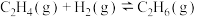


(1)

(2)保持温度不变,在恒容反应器中,按照
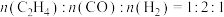 投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时
投料,发生反应Ⅰ和Ⅱ,初始压强为4p kPa,反应t min达到平衡,平衡时 的转化率为80%,
的转化率为80%, 的选择性为25%,则
的选择性为25%,则 的转化率为
的转化率为

 。(用含p的代数式表示,
。(用含p的代数式表示, 的选择性=
的选择性= )。
)。(3)在装有相同催化剂的。相同恒压容器中,按照
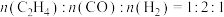 投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下
投料,发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 的转化率(
的转化率( )如图所示。则B、D两点的平均反应速率v(B)
)如图所示。则B、D两点的平均反应速率v(B)(4)T℃时,向恒温恒容的甲容器中,通入1mol
 、1mol CO和2mol
、1mol CO和2mol  ;向绝热恒容的乙容器中通入1mol
;向绝热恒容的乙容器中通入1mol  、1mol CO、2mol
、1mol CO、2mol  ,若只发生上述反应Ⅰ。则甲乙容器中
,若只发生上述反应Ⅰ。则甲乙容器中 的平衡转化率
的平衡转化率
 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是
您最近一年使用:0次
3 . 丙烯酸是非常重要的化工原料之一,可由甘油催化转化制得,过程如下:甘油(C3H8O3)→丙烯醛(C3H4O)→丙烯酸(C3H4O2)。甘油常压下沸点为290℃,工业生产选择反应温度为300℃常压下进行。下列说法错误的是
已知:反应I:C3H8O3(g) C3H4O(g)+2H2O(g) △H1>0 K1
C3H4O(g)+2H2O(g) △H1>0 K1
反应II:2C3H4O(g)+O2(g) 2C3H4O2(g) △H2<0 K2
2C3H4O2(g) △H2<0 K2
已知:反应I:C3H8O3(g)
 C3H4O(g)+2H2O(g) △H1>0 K1
C3H4O(g)+2H2O(g) △H1>0 K1反应II:2C3H4O(g)+O2(g)
 2C3H4O2(g) △H2<0 K2
2C3H4O2(g) △H2<0 K2A.反应I的平衡常数K1=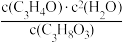 |
| B.反应Ⅱ是焓减、熵减的反应 |
| C.丙烯醛有毒,可选择适用反应Ⅱ且对反应I几乎无影响的高效催化剂 |
| D.若改变条件增大反应Ⅱ的K2,反应Ⅱ平衡移动过程中逆反应速率先增大后减小 |
您最近一年使用:0次
4 . 能量、速率与限度是认识和研究化学反应的重要视角。
Ⅰ.为了探究原电池的工作原理,设计如下装置。________ 。
(2)当乙装置中的负极质量减少1.8g时,正极产生气体________ L(标准状况下); 向
向________ (填“Mg”或“Al”)电极移动。
Ⅱ. 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(3)反应过程中的能量变化如图所示:________ (填“放热”或“吸热”)反应。
(4)300℃时,向容积为2L的恒容密闭容器中,充入 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为________ (填“a”、“b”或“c”);在M点,
________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是________ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
③下列叙述不能说明该反应达到平衡状态的是________ 。
A.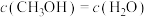
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成 ,同时消耗
,同时消耗
Ⅰ.为了探究原电池的工作原理,设计如下装置。
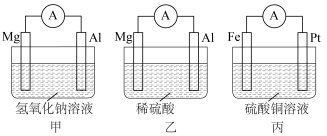
(2)当乙装置中的负极质量减少1.8g时,正极产生气体
 向
向Ⅱ.
 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(3)反应过程中的能量变化如图所示:

(4)300℃时,向容积为2L的恒容密闭容器中,充入
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: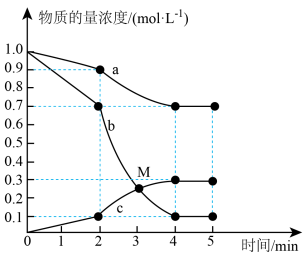
 的浓度随时间变化曲线为
的浓度随时间变化曲线为
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂③下列叙述不能说明该反应达到平衡状态的是
A.
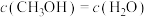
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成
 ,同时消耗
,同时消耗
您最近一年使用:0次
5 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图示:________ 。
(2)若上述反应中X、Y、Z分别为 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入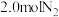 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率
________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为________ kJ/mol。
(4)CO与 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。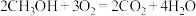 ,则c电极是
,则c电极是________ (填“正极”或“负极”)。若外电路中转移2mol电子,则上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为________ L。
(5)下列反应中,属于吸热反应的是________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥ 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应

(2)若上述反应中X、Y、Z分别为
 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入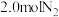 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.36 | 0.48 | 0.50 | 0.50 |

(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成
 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为(4)CO与
 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。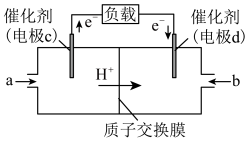
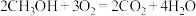 ,则c电极是
,则c电极是 在标准状况下的体积为
在标准状况下的体积为(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥
 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应
您最近一年使用:0次
6 . 已知反应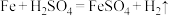 ,下列叙述不正确的是
,下列叙述不正确的是
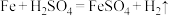 ,下列叙述不正确的是
,下列叙述不正确的是
| A.可将该反应设计成如图甲所示的原电池 |
| B.反应过程中能量关系可用图乙表示 |
| C.若Fe不纯(含有杂质碳),该反应的化学反应速率要减慢 |
D.图甲装置中, 在铜表面被还原产生气泡 在铜表面被还原产生气泡 |
您最近一年使用:0次
7 . 高附加值产品 的合成催化反应历程如图所示。下列说法错误的是
的合成催化反应历程如图所示。下列说法错误的是
 的合成催化反应历程如图所示。下列说法错误的是
的合成催化反应历程如图所示。下列说法错误的是
A.第一电离能和电负性均为: |
B.反应物→ 过程中,有 过程中,有 键和 键和 键的断裂 键的断裂 |
| C.①→②过程吸收能量,且E为该过程正向的活化能 |
| D.该反应总反应的原子利用率为100% |
您最近一年使用:0次
8 . 回答下列问题
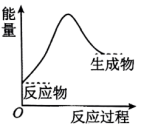
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是________ (填序号)。
b.盐酸与碳酸氢钠
c.碳酸钙分解
d. 固体与
固体与 固体
固体
e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼( )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:
该反应属于________ 反应(填“放热”或“吸热”), 和
和 的总能量
的总能量________ (填“>”“=”或“<”) 和
和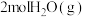 的总能量。
的总能量。
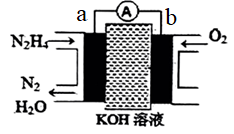
(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。________ (填化学式),负极的电极反应式为________ 。
②电池工作时, 移向
移向________ 电极(填“a”或“b”)。
③当b电极上消耗标况下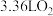 时,电路中转移的电子数为
时,电路中转移的电子数为________ 。
(4)肼( )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式________ 。
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是
b.盐酸与碳酸氢钠
c.碳酸钙分解
d.
 固体与
固体与 固体
固体e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼(
 )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:化学键 | N-H | N-N | N≡N | O=O | O-H |
能量 | 391 | 154 | 942 | 500 | 463 |
 和
和 的总能量
的总能量 和
和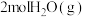 的总能量。
的总能量。(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。
②电池工作时,
 移向
移向③当b电极上消耗标况下
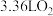 时,电路中转移的电子数为
时,电路中转移的电子数为(4)肼(
 )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
您最近一年使用:0次
9 .  催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现在以
催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现在以 为主的催化剂上发生的反应过程如图2所示。下列说法正确的是
为主的催化剂上发生的反应过程如图2所示。下列说法正确的是
 催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现在以
催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现在以 为主的催化剂上发生的反应过程如图2所示。下列说法正确的是
为主的催化剂上发生的反应过程如图2所示。下列说法正确的是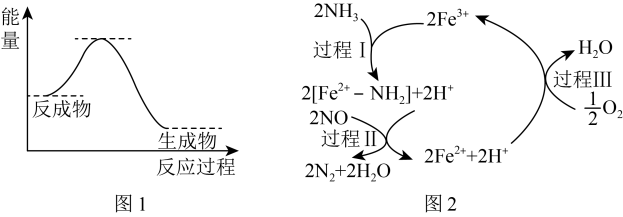
A. 催化还原NO的反应为吸热反应 催化还原NO的反应为吸热反应 |
| B.过程Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
C.由过程Ⅰ可知 中N元素的化合价为-3价 中N元素的化合价为-3价 |
D.图2烟气脱硝的总反应为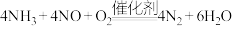 |
您最近一年使用:0次
名校
10 . 下列说法正确的是
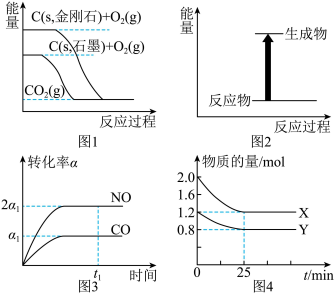
| A.由图1可知,金刚石比石墨稳定 |
| B.图2可表示碳酸氢钠和盐酸反应的能量变化 |
C.由图3可知,对于反应 ,当NO和CO转化率之比为2∶1时,可判断该反应已达到平衡状态 ,当NO和CO转化率之比为2∶1时,可判断该反应已达到平衡状态 |
D.由图4可知,对于反应 ,在0~25min内,用X表示的平均反应速率为0.032 ,在0~25min内,用X表示的平均反应速率为0.032 |
您最近一年使用:0次