名校
解题方法
1 . 甲苯与乙酰氯(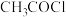 )在无水
)在无水 催化下发生反应,部分反应机理如图所示。下列说法错误的是
催化下发生反应,部分反应机理如图所示。下列说法错误的是
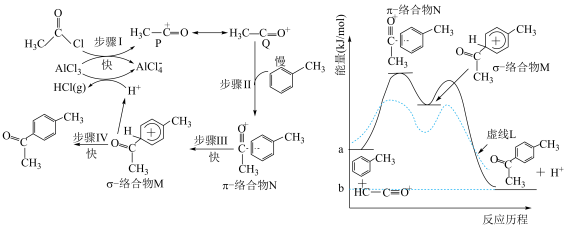
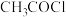 )在无水
)在无水 催化下发生反应,部分反应机理如图所示。下列说法错误的是
催化下发生反应,部分反应机理如图所示。下列说法错误的是
A. 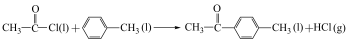 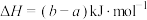 |
| B.该反应的决速步是步骤Ⅱ |
C.甲苯与乙酰氯反应过程中有反应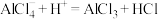 发生 发生 |
D.已知稳定性: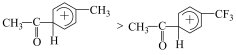 ,则虚线可表示 ,则虚线可表示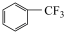 ,与 ,与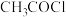 的反应历程 的反应历程 |
您最近一年使用:0次
2024-02-24更新
|
201次组卷
|
2卷引用:山东省日照市校际联合2023-2024学年高三上学期1月期末考试化学试题
名校
解题方法
2 . 人类利用化学反应不仅可以创造新物质,还可以获取能量或实现不同形式能量之间的转化。回答下列问题:
(1)氨气是重要的化工原料,工业合成氨反应:N2 (g)+ 3H2(g) 2NH3(g)。已知在25℃、
2NH3(g)。已知在25℃、 时,拆开
时,拆开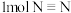 键、
键、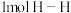 键和
键和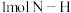 键所需能量分别为946kJ、436kJ、和391kJ。
键所需能量分别为946kJ、436kJ、和391kJ。
①根据上述数据判断,合成氨的反应是___________ 反应(填“吸热”或“放热”)。
②每消耗0.3molN2,反应放出或吸收的热量Q1=___________ kJ。
③将0.5molN2和4.5molH2充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2___________ Q1 (填“>”“<”或“=”),理由是___________ 。
(2)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。
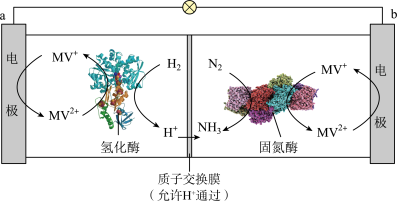
①b电极为___________ (填“正极”或“负极”),电极反应式为___________ 。
②电池工作时在固氮酶表面发生的反应为___________ 。
(1)氨气是重要的化工原料,工业合成氨反应:N2 (g)+ 3H2(g)
 2NH3(g)。已知在25℃、
2NH3(g)。已知在25℃、 时,拆开
时,拆开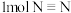 键、
键、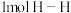 键和
键和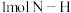 键所需能量分别为946kJ、436kJ、和391kJ。
键所需能量分别为946kJ、436kJ、和391kJ。①根据上述数据判断,合成氨的反应是
②每消耗0.3molN2,反应放出或吸收的热量Q1=
③将0.5molN2和4.5molH2充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2
(2)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。

①b电极为
②电池工作时在固氮酶表面发生的反应为
您最近一年使用:0次
3 . 常温下,1mol化学键形成(或断裂)的能量变化用E表示。根据表中信息判断,下列说法错误的是
| 共价键 | H-H | Cl-Cl | H-Cl |
| E(kJ•mol-1) | 436 | 243 | 431 |
| A.断裂1mol H-H键吸收436 kJ的能量 |
B.H(g)+Cl(g)→HCl(g)  =-431 kJ•mol-1 =-431 kJ•mol-1 |
C.H2(g)+Cl2(g)=2HCl(g)  =+248 kJ•mol-1 =+248 kJ•mol-1 |
| D.1 mol H2(g)与1mol Cl2(g)的总能量高于2 molHCl(g)的总能量 |
您最近一年使用:0次
名校
解题方法
4 . 科学家正在研究 纳米材料作为光催化剂催化
纳米材料作为光催化剂催化 和
和 实现
实现 耦联合成尿素
耦联合成尿素 的方法。该反应主要有两个过程:
的方法。该反应主要有两个过程:
ⅰ. 放热快反应
放热快反应
ⅱ. 吸热慢反应
吸热慢反应
下列图象能正确表示这两个过程能量(E)变化历程的是
 纳米材料作为光催化剂催化
纳米材料作为光催化剂催化 和
和 实现
实现 耦联合成尿素
耦联合成尿素 的方法。该反应主要有两个过程:
的方法。该反应主要有两个过程:ⅰ.
 放热快反应
放热快反应ⅱ.
 吸热慢反应
吸热慢反应下列图象能正确表示这两个过程能量(E)变化历程的是
A. | B.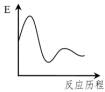 | C.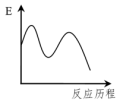 | D.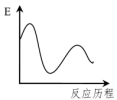 |
您最近一年使用:0次
2024-02-04更新
|
74次组卷
|
2卷引用:山东省东营市2023-2024学年高二期末考试化学试题
解题方法
5 .  与
与 的干法重整(DRM)反应为
的干法重整(DRM)反应为 。向体积为
。向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,在不同温度
,在不同温度 、
、 下测得
下测得 随时间变化的曲线如图。下列说法错误的是
随时间变化的曲线如图。下列说法错误的是
 与
与 的干法重整(DRM)反应为
的干法重整(DRM)反应为 。向体积为
。向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,在不同温度
,在不同温度 、
、 下测得
下测得 随时间变化的曲线如图。下列说法错误的是
随时间变化的曲线如图。下列说法错误的是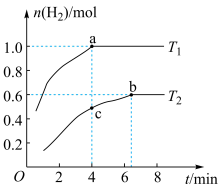
| A.该反应是吸热反应 |
B.a、b点平衡常数: |
C. 时, 时, 的平衡转化率是30% 的平衡转化率是30% |
D.化学反应速率: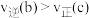 |
您最近一年使用:0次
2024-02-02更新
|
92次组卷
|
3卷引用:山东省济南市2023-2024学年高二上学期1月期末化学试题
名校
解题方法
6 .  合成尿素的反应为
合成尿素的反应为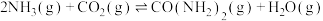
 ,具体反应机理及能量变化(单位:
,具体反应机理及能量变化(单位: )如图所示,TS表示过渡态,表示在催化剂表面的反应,下列说法错误的是
)如图所示,TS表示过渡态,表示在催化剂表面的反应,下列说法错误的是

 合成尿素的反应为
合成尿素的反应为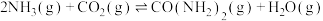
 ,具体反应机理及能量变化(单位:
,具体反应机理及能量变化(单位: )如图所示,TS表示过渡态,表示在催化剂表面的反应,下列说法错误的是
)如图所示,TS表示过渡态,表示在催化剂表面的反应,下列说法错误的是
| A.该反应历程中包含3个基元反应 |
| B.反应前后碳元素、氮元素化合价不变 |
C.反应的焓变 |
D.反应最快的化学方程式为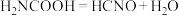 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验无法达到实验目的的是
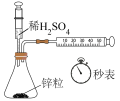 | 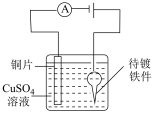 | 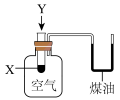 | 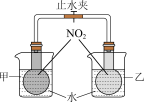 |
| A.测定一定时间内生成H2的反应速率 | B.在铁制钥匙上镀铜 | C.探究X与Y反应的热效应 | D.探究温度对平衡的影响,左池加入NH4NO3晶体;右池加入生石灰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-18更新
|
263次组卷
|
2卷引用:山东省实验中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
8 . 水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。下列说法不正确的是
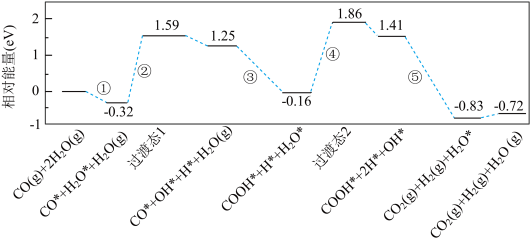

| A.步骤②存在O-H键的形成 |
| B.水煤气变换反应的△H<0 |
| C.该反应的决速步是步骤④ |
| D.步骤③的化学方程式为:CO*+OH*+H2O(g)=COOH*+H2O* |
您最近一年使用:0次
名校
解题方法
9 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在碳酸钙中加入硝酸,并将产生的气体通入Na2SiO3溶液中 | Na2SiO3溶液变浑浊 | 非金属性:C>Si |
| B | 在装有NaHCO3溶液的试管中加入柠檬酸,用手摸试管外壁 | 产生气泡,试管外壁变凉 | 柠檬酸的酸性比碳酸强,该反应是放热反应 |
| C | 向PCl5中通入水蒸气 | 产生的气体能使紫色石蕊试液变红 | PCl5发生了氧化还原反应 |
| D | 向分别装有粗锌和纯锌的两支试管中各加入5mL稀硫酸 | 单位时间内,装有粗锌的试管中产生的气泡更多 | 粗锌与硫酸构成微电池,原电池能加快反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-06更新
|
232次组卷
|
2卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期1月份阶段性考试化学试题
10 . 过渡态理论认为:化学反应不是通过反应物分子的简单碰撞完成的。在反应物分子生成产物分子的过程中,首先生成一种高能量的活化配合物,高能量的活化配合物再进一步转化为产物分子。按照过渡态理论, 的反应历程如下,下列有关说法正确的是
的反应历程如下,下列有关说法正确的是
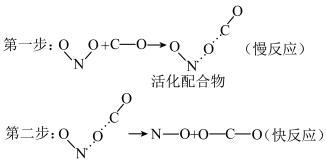
 的反应历程如下,下列有关说法正确的是
的反应历程如下,下列有关说法正确的是
| A.第二步活化配合物之间的碰撞一定是有效碰撞 |
| B.活化配合物的能量越高,第一步的反应速率越快 |
| C.第一步反应需要吸收能量 |
| D.该反应的反应速率主要取决于第二步反应 |
您最近一年使用:0次
2024-01-03更新
|
242次组卷
|
9卷引用:山东省济宁市兖州区2023-2024学年高二上学期期中考试化学试题
山东省济宁市兖州区2023-2024学年高二上学期期中考试化学试题浙江省宁波市咸祥中学2021-2022学年高二上学期期中考试化学试题福建省德化一中、永安一中、漳平一中三校协作2021-2022学年高一下学期5月联考化学试题浙江省精诚联盟2022-2023学年高二上学期10月联考化学试题天津市第一中学2022-2023学年高三上学期期末考试(第三次月考)化学试题(已下线)第七章 化学反应速率与化学平衡 第40练 化学反应速率重庆市大足中学2021-2022学年高二上学期第一次月考化学试题天津市第一中学2022-2023学年高三上学期1月期末质量检测化学试题(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)



