名校
解题方法
1 . 2022年中国航天在诸多领域实现重大突破。空间站一种处理 的重要方法是对
的重要方法是对 进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为:
进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为:_______ 。
(2)Sabatier反应
已知:H2(g)、CH4(g)的燃烧热分别为285.8kJ•mol-1、890.3kJ•mol-1,H2O(l)=H2O(g) ΔH = +44kJ•mol-1。
①则反应Ⅰ:CO2(g) +4H2(g) CH4(g) +2H2O(g) 的ΔH =
CH4(g) +2H2O(g) 的ΔH =_____ kJ•mol-1。
②科学家研究Sabatier反应,部分历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中错误的是_______ 。
B.该转化反应的速率取决于Ts1的能垒
C.·HOCO转化为·CO和·OH的反应ΔH<0
D.催化剂能降低反应的活化能,提高反应物的平衡转化率
③空间站的反应器内,通常采用反应器前段加热,后段冷却的方法以提高CO2的转化效率,原因是_______ 。
④在CO2催化加氢制甲烷过程中存在竞争性的反应Ⅱ:CO2(g)+ H2(g) CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=
CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)= ______ mol•L-1•min-1;反应Ⅱ的平衡常数Kp=______ (Kp是用分压表示的平衡常数,用各组分的分压代替浓度)。
 的重要方法是对
的重要方法是对 进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为:
进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为: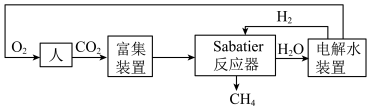
(2)Sabatier反应
已知:H2(g)、CH4(g)的燃烧热分别为285.8kJ•mol-1、890.3kJ•mol-1,H2O(l)=H2O(g) ΔH = +44kJ•mol-1。
①则反应Ⅰ:CO2(g) +4H2(g)
 CH4(g) +2H2O(g) 的ΔH =
CH4(g) +2H2O(g) 的ΔH =②科学家研究Sabatier反应,部分历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中错误的是

B.该转化反应的速率取决于Ts1的能垒
C.·HOCO转化为·CO和·OH的反应ΔH<0
D.催化剂能降低反应的活化能,提高反应物的平衡转化率
③空间站的反应器内,通常采用反应器前段加热,后段冷却的方法以提高CO2的转化效率,原因是
④在CO2催化加氢制甲烷过程中存在竞争性的反应Ⅱ:CO2(g)+ H2(g)
 CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=
CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=
您最近一年使用:0次
2024-01-22更新
|
45次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高三下学期4月月考化学试题
名校
解题方法
2 . 科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中*表示催化剂表面吸附位。下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中*表示催化剂表面吸附位。下列说法正确的是
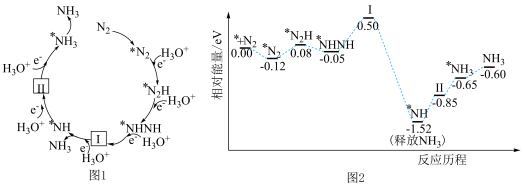
 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中*表示催化剂表面吸附位。下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中*表示催化剂表面吸附位。下列说法正确的是
A.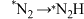 过程中发生非极性键的断裂与形成 过程中发生非极性键的断裂与形成 |
B.Ⅰ转化为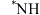 和 和 的过程中会生成 的过程中会生成 |
C.Ⅱ表示的微粒符号是 |
D.反应历程中放热最多的反应是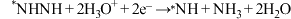 |
您最近一年使用:0次
2024-01-22更新
|
1164次组卷
|
7卷引用:2024年1月安徽普通高等学校招生考试适应性测试化学试题
2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)选择题11-14(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)选择题11-15(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市丰城市第九中学2023-2024学年高三(复读班)上学期期末考试化学试题山东省济宁市第一中学2023-2024学年高三下学期3月月考化学试题
3 . 利用太阳能等可再生能源,通过光催化、光电催化或电解水制氢来进行二氧化碳加氢制甲醇,发生的主要反应是 ,请回答下列有关问题。
,请回答下列有关问题。
(1)常压下,二氧化碳加氢制甲醇反应时的能量变化如图1所示,则该反应的反应热
___________ 。

(2)若二氧化碳加氢制甲醇反应在恒温恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 时刻达到平衡状态的是___________(填字母序号)。
时刻达到平衡状态的是___________(填字母序号)。
(3) ℃,在容积(均为2L)相同的a,b两个密闭容器中分别均投入
℃,在容积(均为2L)相同的a,b两个密闭容器中分别均投入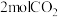 和
和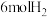 ,进行二氧化碳加氢制甲醇的反应。容器a中保持压强不变,容器b保持容积不变,容器b中甲醇的体积分数与时间关系如图2所示。
,进行二氧化碳加氢制甲醇的反应。容器a中保持压强不变,容器b保持容积不变,容器b中甲醇的体积分数与时间关系如图2所示。
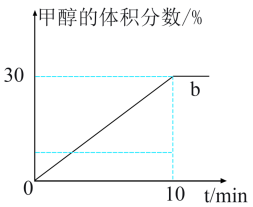
①容器b中0~10min氢气的平均反应速率
___________  ;
; ℃,反应的平衡常数为
℃,反应的平衡常数为___________ 。
②达到平衡后容器a中 的平衡转化率
的平衡转化率___________ 75%(填“>”“<”或“=”)。
③若起始时,容器b中其他条件不变,加入催化剂,则反应情况会由曲线b变为曲线c,则请在图2中画出曲线c的趋势___________ 。
(4)二氧化碳加氢制甲醇的反应历程如图3所示,方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV);其中,TS表示过渡态、*表示吸附在催化剂上的微粒。
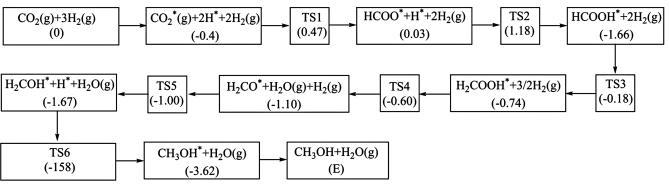
则生成甲醇的决速步骤的反应方程式为___________ 。
 ,请回答下列有关问题。
,请回答下列有关问题。(1)常压下,二氧化碳加氢制甲醇反应时的能量变化如图1所示,则该反应的反应热


(2)若二氧化碳加氢制甲醇反应在恒温恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到
 时刻达到平衡状态的是___________(填字母序号)。
时刻达到平衡状态的是___________(填字母序号)。A.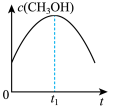 | B. | C.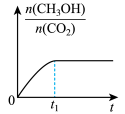 | D.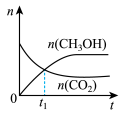 |
(3)
 ℃,在容积(均为2L)相同的a,b两个密闭容器中分别均投入
℃,在容积(均为2L)相同的a,b两个密闭容器中分别均投入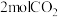 和
和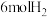 ,进行二氧化碳加氢制甲醇的反应。容器a中保持压强不变,容器b保持容积不变,容器b中甲醇的体积分数与时间关系如图2所示。
,进行二氧化碳加氢制甲醇的反应。容器a中保持压强不变,容器b保持容积不变,容器b中甲醇的体积分数与时间关系如图2所示。
①容器b中0~10min氢气的平均反应速率

 ;
; ℃,反应的平衡常数为
℃,反应的平衡常数为②达到平衡后容器a中
 的平衡转化率
的平衡转化率③若起始时,容器b中其他条件不变,加入催化剂,则反应情况会由曲线b变为曲线c,则请在图2中画出曲线c的趋势
(4)二氧化碳加氢制甲醇的反应历程如图3所示,方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV);其中,TS表示过渡态、*表示吸附在催化剂上的微粒。

则生成甲醇的决速步骤的反应方程式为
您最近一年使用:0次
名校
解题方法
4 . 已知:① 可将
可将 氧化为
氧化为 ;②直接参与化学键变化的核素被替换为更重的同位素时,反应速率会变慢。
;②直接参与化学键变化的核素被替换为更重的同位素时,反应速率会变慢。 与
与 或
或 反应时体系的能量随反应进程的变化如图所示。下列说法错误的是
反应时体系的能量随反应进程的变化如图所示。下列说法错误的是

 可将
可将 氧化为
氧化为 ;②直接参与化学键变化的核素被替换为更重的同位素时,反应速率会变慢。
;②直接参与化学键变化的核素被替换为更重的同位素时,反应速率会变慢。 与
与 或
或 反应时体系的能量随反应进程的变化如图所示。下列说法错误的是
反应时体系的能量随反应进程的变化如图所示。下列说法错误的是
| A.该反应是放热反应 |
B.步骤Ⅰ涉及 键的断裂,步骤Ⅱ涉及 键的断裂,步骤Ⅱ涉及 键的形成 键的形成 |
C. 与 与 反应的能量变化为曲线c 反应的能量变化为曲线c |
D.相同情况下, 与 与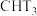 反应,氚代甲醇 反应,氚代甲醇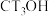 的产量大于 的产量大于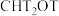 |
您最近一年使用:0次
2024-01-13更新
|
794次组卷
|
3卷引用:辽宁省锦州市2023-2024学年高三上学期1月期末化学试题
名校
解题方法
5 . 在催化剂作用下,CO和H2合成CH3OH的历程如图所示(*表示物种被吸附在催化剂表面)。下列叙述错误的是
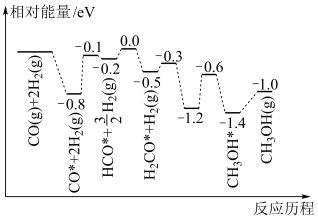

| A.合成甲醇正反应的△H<0 |
B.速控步骤为CO*+2H2(g)=HCO*+ H2(g) H2(g) |
| C.在相同条件下,CH3OH*比CH3OH(g)稳定 |
| D.总反应过程中只断裂σ键和形成σ键 |
您最近一年使用:0次
2024-01-11更新
|
368次组卷
|
5卷引用:河北省石家庄市第九中学2023-2024学年高三上学期12月联考化学试题
河北省石家庄市第九中学2023-2024学年高三上学期12月联考化学试题江西省部分学校2023-2024学年高三上学期12月月考化学试题河北省保定市部分重点高中2023-2024学年高三上学期12月期末化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省上饶市第一中学2023-2024学年高二下学期开学考试化学试题
6 . CH4超干重整CO2的催化转化如图1所示,相关反应的能量变化如图2所示:
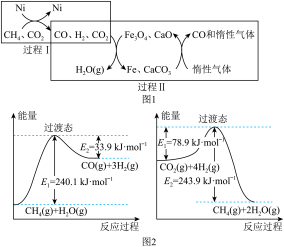
| A.过程I的热化学方程式为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4kJ•mol-1 |
| B.过程II实现了含碳物质与含氢物质的分离 |
| C.过程II中Fe3O4、CaO为中间产物 |
| D.CH4超干重整CO2的总反应为:CH4+3CO2=4CO+2H2O |
您最近一年使用:0次
名校
7 . 本次亚运会火炬燃料甲醇是利用焦炉气中的氢气(H2)与从工业尾气中捕集的二氧化碳(CO2)合成,并由远程甲醇动力重卡提供运输保障。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
Ⅰ.
Ⅱ.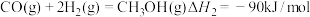
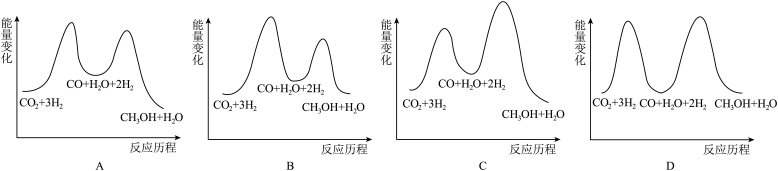
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。
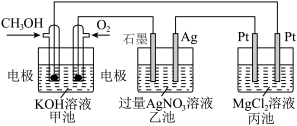
①甲池中通入 的电极电极反应方程式为
的电极电极反应方程式为___________ 。
②丙池中总反应的离子方程式为___________ 。
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗
___________  (标准状况)。
(标准状况)。
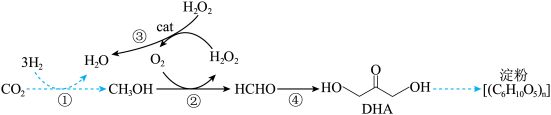
(3)回收并利用 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
(4)利用两种金属催化剂,在水溶液体系中将 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
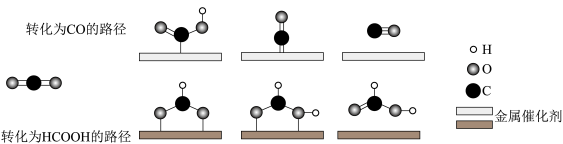
下列说法错误的是___________(填标号)。
(1)二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:Ⅰ.

Ⅱ.
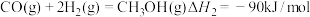
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是

(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。

①甲池中通入
 的电极电极反应方程式为
的电极电极反应方程式为②丙池中总反应的离子方程式为
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗

 (标准状况)。
(标准状况)。(3)回收并利用
 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
A.反应①中消耗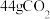 ,转移电子数为 ,转移电子数为 |
| B.淀粉与纤维素的分子式相同,互为同分异构体 |
C. 与 与 的混合物中所含氧原子数为 的混合物中所含氧原子数为 |
D.反应③中cat为催化剂,实验室常用 催化该反应 催化该反应 |
(4)利用两种金属催化剂,在水溶液体系中将
 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
下列说法错误的是___________(填标号)。
A.在转化为 的路径中,只涉及碳氧键的断裂和氧氢键的形成 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
B.在转化为 的路径中, 的路径中, 被氧化为 被氧化为 |
| C.两个转化路径均无非极性键的形成 |
| D.上述反应过程说明催化剂具有选择性 |
您最近一年使用:0次
2023-12-18更新
|
69次组卷
|
2卷引用:四川省德阳市第五中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
8 .  与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与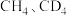 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
 与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与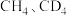 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是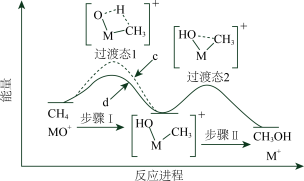
A. 与 与 反应的能量变化应为图中曲线d 反应的能量变化应为图中曲线d |
| B.步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是Ⅱ |
C. 与 与 反应,氘代甲醇的产量: 反应,氘代甲醇的产量: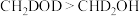 |
D.若 与 与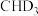 反应,生成的氘代甲醇有2种 反应,生成的氘代甲醇有2种 |
您最近一年使用:0次
2023-12-15更新
|
399次组卷
|
5卷引用:浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题
浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题河南省郑州市宇华实验学校2023-2024学年高三上学期1月期末化学试题(已下线)选择题11-15(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
解题方法
9 . 乙醇在浓硫酸做催化剂的条件下发生脱水反应,反应历程和能量变化关系图如下,下列说法正确的是。
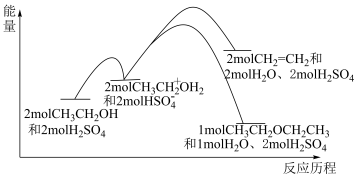
| A.采用较低温度,可获得产率更高的乙醚 |
| B.在上述相同条件下,正丙醇比异丙醇更容易反应 |
| C.为了获得更多的乙烯,温度越高越好 |
| D.选择合适的催化剂,可提高平衡时乙烯的产率 |
您最近一年使用:0次
10 . 自由基是化学键断裂时产生的含未成对电子的中间体,HNO自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是
 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是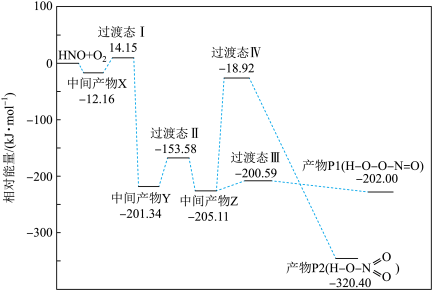
A.反应过程中,产物 的浓度先增大,后减小 的浓度先增大,后减小 |
B.过渡态能量越高,反应的活化能越高,反应的 越小 越小 |
C.其它条件相同,升高温度,达到平衡时,生成的产物中 的百分含量增大 的百分含量增大 |
D.反应过程中,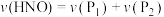 |
您最近一年使用:0次



